 是元素周期表前四周期中的四种常见元素,其相关信息如下表:
是元素周期表前四周期中的四种常见元素,其相关信息如下表: | 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且最高能级是半充满状态 |
| Y | 第三周期元素,它的单质是良好的半导体材料 |
| Z | Z和Y同周期,Z是本周期原子半径最小的主族元素 |
| W | W的一种核素的质量数为63,中子数为34 |
(2)元素Y位于元素周期表的第三周期
(3)元素Z的原子最外层共有
(4)元素Y与元素Z相比,非金属性较强的是
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
更新时间:2022-04-13 16:23:52
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
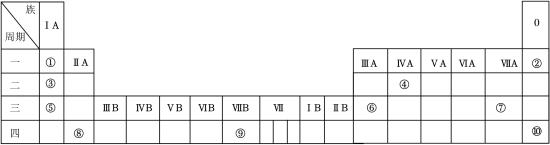
【推荐1】下表列出了①~⑩十种元素在元素周期表中的位置。
(1)⑦的单质和⑤的最高价氧化物对应的水化物反应的方程式:________ 。
(2)⑧的固态氢化物CaH2与H2O反应生成Ca(OH)2和一种可燃性气体单质____ 。(填化学式)
(3)某小组同学设计实验比较VIIA族元素的非金属性:Cl>Br>I。
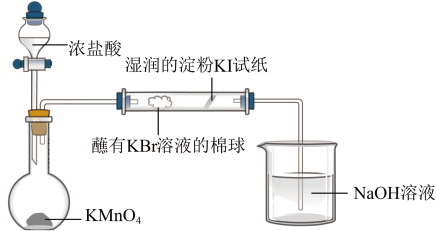
甲同学设计实验如下:打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙黄色,湿润的淀粉KI试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。____ 。
②除了利用卤素单质间的置换反应,下列可作为卤族元素非金属性递变规律的判断依据有____ 。(填字母)
A.Cl2、Br2、I2的熔点逐渐升高 B.HCl、HBr、HI的稳定性逐渐减弱
C.HCl、HBr、HI水溶液的酸性逐渐增强 D.Cl﹣、Br﹣、I﹣的还原性逐渐增强
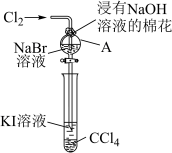
③写出圆底烧瓶中发生的化学反应方程式____ 。
(1)⑦的单质和⑤的最高价氧化物对应的水化物反应的方程式:
(2)⑧的固态氢化物CaH2与H2O反应生成Ca(OH)2和一种可燃性气体单质
(3)某小组同学设计实验比较VIIA族元素的非金属性:Cl>Br>I。
甲同学设计实验如下:打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙黄色,湿润的淀粉KI试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。
②除了利用卤素单质间的置换反应,下列可作为卤族元素非金属性递变规律的判断依据有
A.Cl2、Br2、I2的熔点逐渐升高 B.HCl、HBr、HI的稳定性逐渐减弱
C.HCl、HBr、HI水溶液的酸性逐渐增强 D.Cl﹣、Br﹣、I﹣的还原性逐渐增强
③写出圆底烧瓶中发生的化学反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某研究性学习小组设计了一组实验验证元素周期律。
(1)甲同学在a、b、c三只烧杯里分别加入50mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂、钠、钾块,观察现象。甲同学设计实验的目的是_______ ,烧杯_______ (填字母)中的反应最剧烈。
(2)乙同学利用下图所示装置验证同主族元素非金属性的变化规律。回答下列问题:
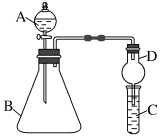
①仪器A的名称为_______ ,干燥管D的作用是_______ 。
②若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,C中加淀粉碘化钾混合溶液,实验时观察到_______ ,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用_______ 吸收尾气。
③若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加_______ 溶液(写化学式),若观察到C中的现象为_______ ,即可证明。但有的同学认为该实验存在缺陷,应在两装置间添加装有_______ 溶液的洗气瓶,目的是_______ 。
(1)甲同学在a、b、c三只烧杯里分别加入50mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂、钠、钾块,观察现象。甲同学设计实验的目的是
(2)乙同学利用下图所示装置验证同主族元素非金属性的变化规律。回答下列问题:

①仪器A的名称为
②若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,C中加淀粉碘化钾混合溶液,实验时观察到
③若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】元素周期表与元素周期律在学习、研究中有很重要的作用。下表所示为某5种元素的相关信息,已知W、X都位于第三周期。
回答下列问题:
(1)W在元素周期表中的位置为_______ ,X的最高价氧化物对应水化物的化学式为_______ 。
(2)用电子式表示X2Q的形成过程:_______ 。
(3)金属性Y_______ (填“>”或“<”)X,从原子结构角度解释原因_______ 。
(4)下列对于Z及其化合物的推断中正确的是_______(填标号)。
(5)将X元素的单质在Q元素的单质中点燃生成M,预测将M投入硫酸亚铁溶液中,主要的反应现象是_______ 。
| 元素 | 信息 |
| Q | 地壳中含量最高的元素 |
| W | 最高化合价为+7价 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃)的火焰为紫色 |
| Z | 原子结构示意图为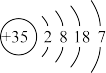 |
(1)W在元素周期表中的位置为
(2)用电子式表示X2Q的形成过程:
(3)金属性Y
(4)下列对于Z及其化合物的推断中正确的是_______(填标号)。
| A.Z的化合价中只有+7价 |
| B.Z的最高价氧化物对应水化物的酸性弱于w的最高价氧化物对应水化物的酸性 |
| C.Z元素单质的氧化性强于W元素单质的氧化性 |
| D.Z与X形成的化合物中只存在离子键 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】我国科学家研发的新型光学材料(Sn7Br10S2)可替代传统光学材料硫镓银(AgGaS2)和磷锗锌(ZnGeP2)。请回答下列问题:
(1)基态硫原子核外电子云轮廓图呈哑铃形的能级上占据的电子总数为___________ 。
(2)SF6可用作高压发电系统的绝缘气体,其分子呈正八面体结构,如图所示。
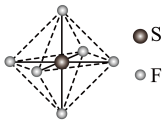
①SF6是___________ (填“极性”或“非极性”)分子。
②1molSF6分子中含___________ molσ键。
(3)HF、HCl、HBr的酸性由强到弱的顺序为___________ (填化学式,下同);沸点由高到低的顺序为___________ ;还原性由强到弱的顺序为___________ 。
(4)Ga(CH3)3和NH3在一定条件下可合成半导体材料GaN和CH4。Ga(CH3)3分子中Ga原子和C原子构成的空间构型是___________ ,碳原子的杂化类型是___________ 。
(5)四卤化锡的熔点如下表所示:
它们熔点递变的主要原因是___________ 。
(1)基态硫原子核外电子云轮廓图呈哑铃形的能级上占据的电子总数为
(2)SF6可用作高压发电系统的绝缘气体,其分子呈正八面体结构,如图所示。

①SF6是
②1molSF6分子中含
(3)HF、HCl、HBr的酸性由强到弱的顺序为
(4)Ga(CH3)3和NH3在一定条件下可合成半导体材料GaN和CH4。Ga(CH3)3分子中Ga原子和C原子构成的空间构型是
(5)四卤化锡的熔点如下表所示:
| 物质 | SnCl4 | SnBr4 | SnI4 |
| 熔点/℃ | ﹣33 | 31 | 144.5 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】锗、锡、铅均属于ⅣA族元素,它们的单质与化合物广泛应用于生活的各个领域。
Ⅰ.完成下列填空:
(1)锗元素原子核外能量最高的电子有_______ 个,它们运动所形成的电子云形状为_______ 形。
(2)氢化锗(GeH4)结构与甲烷类似,在常温常压下是具有刺激性气味的无色有毒气体。从结构角度比较GeH4与CH4沸点高低并说明理由_______ 。氢化锗的液氨溶液具有较好的导电性,主要是因为GeH4与NH3反应生成了 和
和_______ (填化学式)两种离子。
Ⅱ.三水锡酸钠(Na2SnO3·3H2O)是一种易溶于水的无色晶体,露置在空气中会逐渐转化成Na2CO3和Sn(OH)4。
(3)常温下,相同物质的量浓度的Na2SnO3溶液与Na2CO3溶液,前者pH_______ (填“大于”“小于”或“等于”)后者。
(4)写出三水锡酸钠露置在空气中发生反应的化学方程式_______ 。
Ⅲ.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、 、
、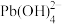 。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。
。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。

(5)Pb(NO3)2溶液中,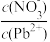
_______ 2(填“>”“=”或“<”);往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液中存在的阳离子除Na+外,还有_______ (填微粒符号)。
(6)科学家发现一种新型脱铅剂DH,能有效除去水中的痕量铅。已知DH脱铅过程中主要发生反应为:2DH(s)+Pb2+(aq) D2Pb(s)+2H+。则脱铅时最合适的pH约为
D2Pb(s)+2H+。则脱铅时最合适的pH约为_______ (选填编号)。
a.4~5 b.6~7 c.8~10 d.12~14
Ⅰ.完成下列填空:
(1)锗元素原子核外能量最高的电子有
(2)氢化锗(GeH4)结构与甲烷类似,在常温常压下是具有刺激性气味的无色有毒气体。从结构角度比较GeH4与CH4沸点高低并说明理由
 和
和Ⅱ.三水锡酸钠(Na2SnO3·3H2O)是一种易溶于水的无色晶体,露置在空气中会逐渐转化成Na2CO3和Sn(OH)4。
(3)常温下,相同物质的量浓度的Na2SnO3溶液与Na2CO3溶液,前者pH
(4)写出三水锡酸钠露置在空气中发生反应的化学方程式
Ⅲ.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、
 、
、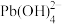 。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。
。当总含铅量一定时,各形态铅的百分比(α)与溶液pH变化的关系如图所示。
(5)Pb(NO3)2溶液中,
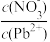
(6)科学家发现一种新型脱铅剂DH,能有效除去水中的痕量铅。已知DH脱铅过程中主要发生反应为:2DH(s)+Pb2+(aq)
 D2Pb(s)+2H+。则脱铅时最合适的pH约为
D2Pb(s)+2H+。则脱铅时最合适的pH约为a.4~5 b.6~7 c.8~10 d.12~14
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】重晶石( )作为原料制备金属钡及其他含钡化合物的方法如下图:
)作为原料制备金属钡及其他含钡化合物的方法如下图:
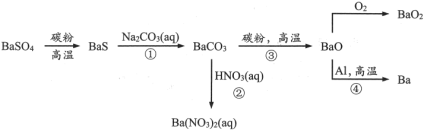
完成下列填空:
(1)Ba在元素周期表中位于第_______ 族,最外层电子的电子云形状是_______ 。图中涉及的第二周期元素原子半径由大到小的顺序是_______ ,可以判断其中两种元素非金属性强弱的反应是_______ (选填流程中的反应编号)。
(2)配平BaS与稀硝酸反应的化学方程式:_______ 。
_______ _______
_______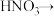 _______
_______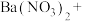 _______
_______ _______
_______ _______
_______
检验溶液中BaS是否完全反应的方法是:取少量反应液,加入_______ (填试剂),有黑色沉淀生成,则BaS未反应完全。
(3)工业上,利用反应①②而不用BaS直接与稀硝酸反应制 的原因是
的原因是_______ 。
(4)元素的金属性:Al_______ Ba(选填“>”或“<”);已知:沸点Al>Ba,反应④在真空容器中可以发生的理由是_______ 。
 )作为原料制备金属钡及其他含钡化合物的方法如下图:
)作为原料制备金属钡及其他含钡化合物的方法如下图:
完成下列填空:
(1)Ba在元素周期表中位于第
(2)配平BaS与稀硝酸反应的化学方程式:
_______
 _______
_______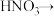 _______
_______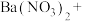 _______
_______ _______
_______ _______
_______
检验溶液中BaS是否完全反应的方法是:取少量反应液,加入
(3)工业上,利用反应①②而不用BaS直接与稀硝酸反应制
 的原因是
的原因是(4)元素的金属性:Al
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍。X原子的M能层上有4个未成对电子。请回答下列问题:
(1)写出C、D、E三种原子第一电离能由大到小的顺序为_______________ 。
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为_____________ ,根据价层电子对互斥理论预测BA2D的分子构型为____________ 。
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个BC-。与A同族且相差两个周期的元素R的离子位于立方体的恰当位置上。根据其结构特点可知该晶体的化学式为(用最简正整数表示)________
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
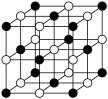
根据表格中的数据:判断KCl、MgO、TiN 三种离子晶体熔点从高到低的顺序是______________ 。MgO晶体中一个Mg2+周围和它最邻近且等距离的O2-有__________________ 个。
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是__________________ 。
(1)写出C、D、E三种原子第一电离能由大到小的顺序为
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个BC-。与A同族且相差两个周期的元素R的离子位于立方体的恰当位置上。根据其结构特点可知该晶体的化学式为(用最简正整数表示)
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:

| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】镓(31Ga)是化学史上第一种先理论预言,后在自然界中被发现并验证的元素。镓的化合物半导体广泛用于电子与微电子工业。
(1)基态Ga原子中,核外电子占据的最高能层的符号是_______ 。
(2)门捷列夫预言的“类硼”(即钪,21Sc),“类铝”(即镓,31Ga),“类硅”(即锗,32Ge)三种元素中,未成对电子数最多的是_______ (填元素符号)。
(3)氮化镓(GaN)和砷化镓(GaAs)都是新型的半导体材料,与晶体硅属于同一晶体类型。
①Ga、N、As三种元素的电负性由大到小的顺序是_______ 。
②GaN熔点(1700℃)高于GaAs熔点(1238℃)的原因是_______ 。
③GaAs可由Ga(CH3)3和AsH3在一定条件下制得,该反应的化学方程式是_______ ,Ga(CH3)3分子中Ga原子的杂化方式是_______ ,AsH3分子的空间构型是_______ 。
(4)钆镓石榴石是一种激光介质材料,其晶体结构单位简图如下。
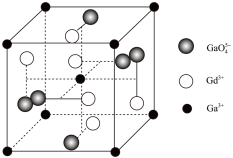
①钆镓石榴石的化学式是_______ 。
②已知晶体结构单位的边长为a nm,晶体的密度为ρ g·cm−3,则阿伏加德罗常数NA=_______ (用含a、ρ的代数式表示)。
(1)基态Ga原子中,核外电子占据的最高能层的符号是
(2)门捷列夫预言的“类硼”(即钪,21Sc),“类铝”(即镓,31Ga),“类硅”(即锗,32Ge)三种元素中,未成对电子数最多的是
(3)氮化镓(GaN)和砷化镓(GaAs)都是新型的半导体材料,与晶体硅属于同一晶体类型。
①Ga、N、As三种元素的电负性由大到小的顺序是
②GaN熔点(1700℃)高于GaAs熔点(1238℃)的原因是
③GaAs可由Ga(CH3)3和AsH3在一定条件下制得,该反应的化学方程式是
(4)钆镓石榴石是一种激光介质材料,其晶体结构单位简图如下。

①钆镓石榴石的化学式是
②已知晶体结构单位的边长为a nm,晶体的密度为ρ g·cm−3,则阿伏加德罗常数NA=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】表为元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题:
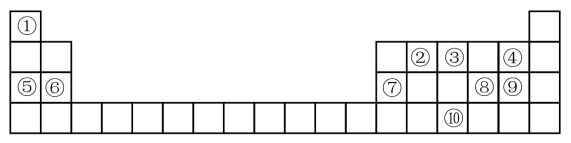
(1)元素⑩价电子排布式_______ ,⑦的原子结构示意图为_______ 。
(2)④、⑤、⑥的简单离子半径由大到小的顺序为_______ (用离子符号和“>”表示)。
(3)④⑧⑨的气态氢化物中,最稳定的是_______ (用化学式表示),最高价氧化物对应水化物中,酸性最强的是_______ (用化学式表示)。
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式_______ 。
(5)由①③⑨组成的离子化合物的化学式为_______ ,其中含有的化学键类型是_______ 。
(6)⑨原子核外电子能量最高的电子所在的能级是_______ 。
(7)基态⑩原子中,核外电子占据最高能层的符号为_______ ,该能层上有_______ 个能级,电子数为_______ 。

(1)元素⑩价电子排布式
(2)④、⑤、⑥的简单离子半径由大到小的顺序为
(3)④⑧⑨的气态氢化物中,最稳定的是
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式
(5)由①③⑨组成的离子化合物的化学式为
(6)⑨原子核外电子能量最高的电子所在的能级是
(7)基态⑩原子中,核外电子占据最高能层的符号为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
(1)基态Ni原子的价电子轨道表示式为_______ 。
(2) 的一种配离子
的一种配离子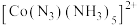 ,配位体
,配位体 中心原子杂化类型为
中心原子杂化类型为_______ 。CoO的熔点高于CoS的原因是_______ 。
(3)配合物铁氰化钾 中几种元素电离能由大到小的顺序是
中几种元素电离能由大到小的顺序是_______ 。
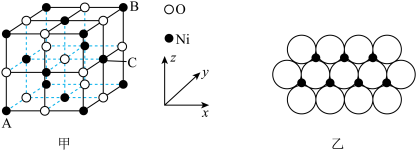
(4)NiO的晶胞结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为_______ 。一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为 作密置单层排列,
作密置单层排列, 填充其中(如图乙),已知
填充其中(如图乙),已知 的半径为apm,设阿伏加德罗常数值为
的半径为apm,设阿伏加德罗常数值为 ,每平方米面积上具有该晶体的质量为
,每平方米面积上具有该晶体的质量为_______ g(用含a、 的代数式表示)。
的代数式表示)。
(1)基态Ni原子的价电子轨道表示式为
(2)
 的一种配离子
的一种配离子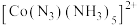 ,配位体
,配位体 中心原子杂化类型为
中心原子杂化类型为(3)配合物铁氰化钾
 中几种元素电离能由大到小的顺序是
中几种元素电离能由大到小的顺序是(4)NiO的晶胞结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为
 作密置单层排列,
作密置单层排列, 填充其中(如图乙),已知
填充其中(如图乙),已知 的半径为apm,设阿伏加德罗常数值为
的半径为apm,设阿伏加德罗常数值为 ,每平方米面积上具有该晶体的质量为
,每平方米面积上具有该晶体的质量为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
【推荐2】以粉煤灰(主要成分:Al2O3、SiO2、少量Fe2O3)为原料,制取Al2O3的部分工艺流程如下:

完成下列填空:
(1)铝原子核外有_______ 种不同能量的电子,最外层电子的轨道式是_______ ,上述流程涉及第二周期元素的原子半径由小到大的顺序是_______ 。
(2)“除铁”是将Fe3+转化为Fe(OH)3沉淀,反应的离子方程式为_______ ,检验溶液中Fe3+是否除尽的方法是_______ 。
(3)解释“结晶”过程中向AlCl3浓溶液中通入HCl气体的原因。_______
(4)上述流程可循环的物质是_______ 。
(5)工业上是通过电解熔化状态下Al2O3,而不是电解熔化状态下AlCl3来获得铝,其原因是_______ 。

完成下列填空:
(1)铝原子核外有
(2)“除铁”是将Fe3+转化为Fe(OH)3沉淀,反应的离子方程式为
(3)解释“结晶”过程中向AlCl3浓溶液中通入HCl气体的原因。
(4)上述流程可循环的物质是
(5)工业上是通过电解熔化状态下Al2O3,而不是电解熔化状态下AlCl3来获得铝,其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。NF3可在铜的催化作用下由F2和过量NH3反应得到。
(1)氟元素基态原子的价电子排布图为______________ ;NF3中心原子轨道的杂化类型为_________ 。
(2)写出制备NF3的化学方程式:____________________ 。
(3)理论上HF、NaAlO2和NaCl按6 : 1 : 2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用。该物质为配合物,其中心离子是___________ ,配位数为_____________ 。该化合物焰色反应火焰呈现___________ 色。很多金属盐都可以发生焰色反应,其原因是__________________ 。
(1)氟元素基态原子的价电子排布图为
(2)写出制备NF3的化学方程式:
(3)理论上HF、NaAlO2和NaCl按6 : 1 : 2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用。该物质为配合物,其中心离子是
您最近一年使用:0次



