现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍。X原子的M能层上有4个未成对电子。请回答下列问题:
(1)写出C、D、E三种原子第一电离能由大到小的顺序为_______________ 。
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为_____________ ,根据价层电子对互斥理论预测BA2D的分子构型为____________ 。
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个BC-。与A同族且相差两个周期的元素R的离子位于立方体的恰当位置上。根据其结构特点可知该晶体的化学式为(用最简正整数表示)________
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
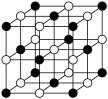
根据表格中的数据:判断KCl、MgO、TiN 三种离子晶体熔点从高到低的顺序是______________ 。MgO晶体中一个Mg2+周围和它最邻近且等距离的O2-有__________________ 个。
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是__________________ 。
(1)写出C、D、E三种原子第一电离能由大到小的顺序为
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个BC-。与A同族且相差两个周期的元素R的离子位于立方体的恰当位置上。根据其结构特点可知该晶体的化学式为(用最简正整数表示)
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:

| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是
2010·黑龙江·模拟预测 查看更多[5]
贵州省安顺市普定县第一中学2018-2019学年高二上学期12月考试化学试题贵州省遵义育新高级中学2018-2019学年高二上学期11月月考化学试题云南省泸水五中2018-2019学年高二上学期期中考试化学试题(已下线)2011届吉林省延吉市汪清六中高三第六次月考(理综)化学部分(已下线)2010年黑龙江省哈九中高三第四次高考模拟考试化学试题
更新时间:2016-12-09 00:30:35
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E、F、G、H为原子序数依次增大的前36号元素,A的一种同位素原子无中子;B元素基态原子的核外电子数是其能级数的2倍,且含有未成对的电子;D的基态原子2p轨道中含有两种不同自旋方向的电子,且电子数之比为3∶1;E为周期表中电负性最强的元素;F、B同主族,H与D元素同主族;G为第四周期元素,其+1价阳离子的核外电子排布式为[Ar]3d10,回答下列问题(用元素符号或化学式表示):
(1)G在元素周期表中位于_______ 区。
(2)B、C、F的原子半径由大到小的顺序为_______ (填元素符号)。
(3)C、D、E的第一电离能由大到小排序是_______ (填元素符号)。
(4)A与其他元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为_______ ,其中心原子的杂化方式为_______ ;A分别与B、C、D形成的共价化合物中既含有极性共价键,又含有非极性共价键的化合物是_______ (填化学式,任意写一种)。
(5)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的酸根离子是_______ (填化学式,下同);酸根离子呈三角锥形结构的是_______ 。
(6)B的一种氢化物相对分子质量是26,其分子中σ键和π键的数目之比为_______ 。
(1)G在元素周期表中位于
(2)B、C、F的原子半径由大到小的顺序为
(3)C、D、E的第一电离能由大到小排序是
(4)A与其他元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为
(5)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的酸根离子是
(6)B的一种氢化物相对分子质量是26,其分子中σ键和π键的数目之比为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W、T是原子序数依次增大的五种短周期元素,且X、Y、Z、W的原子序数之和为32。其中X是元素周期表中原子半径最小的元素,Y、Z左右相邻,Z、W位于同一主族。T的单质常用于自来水的杀菌消毒。请回答下列问题:
(1)W元素在周期表中的位置为_____ 。
(2)由X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与金属铜反应,该反应的离子方程式为_____ 。
(3)Y元素的气态氢化物与其最高价氧化物的水化物可以相互反应,写出其离子方程式:_____ 。
(4)Y和T两元素的非金属性强弱为Y_____ T(填“>”“<”或者“=”),可以验证该结论的方法是_____ 。
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
(1)W元素在周期表中的位置为
(2)由X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与金属铜反应,该反应的离子方程式为
(3)Y元素的气态氢化物与其最高价氧化物的水化物可以相互反应,写出其离子方程式:
(4)Y和T两元素的非金属性强弱为Y
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W是元素周期表前四周期中的四种常见元素,相关信息见下:
(1)Z位于元素周期表第__________ 周期第__________ 族,Y和Z的最高价氧化物对应的水化物的酸性较强的是_____________ (写水化物的化学式)。
(2)XY2是一种常用的溶剂,XY2的分子中存在_____________ 个σ键.在H-Y、H-Z两种共价键中,键的极性较强的是_____________ ,键长较长的是__________ ;
(3)W的基态原子核外电子排布式是__________ W2Y在空气中煅烧生成W2O化学方程式是__________ 。
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(2)XY2是一种常用的溶剂,XY2的分子中存在
(3)W的基态原子核外电子排布式是
您最近半年使用:0次
【推荐1】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。完成下列填空:
(1)下列描述的 原子核外电子运动状态中,能量最高的是_______。
原子核外电子运动状态中,能量最高的是_______。
(2)基态铁原子的价电子排布式为_______ ,基态 与
与 中未成对的电子数之比为
中未成对的电子数之比为_______ 。
(3)与铁同周期元素中, 轨道半充满的元素有
轨道半充满的元素有_______ (填写元素符号)。
(4)氢化锂( )是由两种单核离子构成的离子化合物。组成
)是由两种单核离子构成的离子化合物。组成 的两种元素的电负性:
的两种元素的电负性:
_______  (填“>”或“<”)。判断
(填“>”或“<”)。判断 中两种离子半径的大小,并从原子结构的角度解释原因
中两种离子半径的大小,并从原子结构的角度解释原因_______ 。
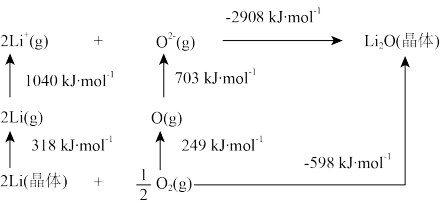
(5)离子化合物 的形成过程如图所示。
的形成过程如图所示。 原子的第一电离能(
原子的第一电离能( )为
)为_______  ,
, 中化学键的键能为
中化学键的键能为_______  。
。
(1)下列描述的
 原子核外电子运动状态中,能量最高的是_______。
原子核外电子运动状态中,能量最高的是_______。A.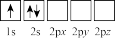 | B.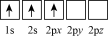 | C.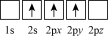 | D. |
 与
与 中未成对的电子数之比为
中未成对的电子数之比为(3)与铁同周期元素中,
 轨道半充满的元素有
轨道半充满的元素有(4)氢化锂(
 )是由两种单核离子构成的离子化合物。组成
)是由两种单核离子构成的离子化合物。组成 的两种元素的电负性:
的两种元素的电负性:
 (填“>”或“<”)。判断
(填“>”或“<”)。判断 中两种离子半径的大小,并从原子结构的角度解释原因
中两种离子半径的大小,并从原子结构的角度解释原因(5)离子化合物
 的形成过程如图所示。
的形成过程如图所示。 原子的第一电离能(
原子的第一电离能( )为
)为 ,
, 中化学键的键能为
中化学键的键能为 。
。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】原子模型塔(如图1所示),由9个大圆球组成,每个圆球代表一个铁原子,构成一个铁原子晶胞模型,象征着人类对和平使用核能源的美好愿望。

(1)基态Fe原子核外电子排布式为___________ ,核外电子占据的最高能层的符号是___________ 。
(2)铁的化合物在生产生活及科学研究方面应用非常广泛。
① 是一种新型光电催化剂。第四电离能大小关系是I4(Co)
是一种新型光电催化剂。第四电离能大小关系是I4(Co) ___________ I4(Fe) (填“>”或“<”),原因是___________ 。
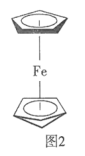
②由环戊二烯离子( )与Fe(Ⅱ)形成的二茂铁[
)与Fe(Ⅱ)形成的二茂铁[ ]结构如图2所示。已知
]结构如图2所示。已知 与苯结构相似,所有原子处于同一平面上,则
与苯结构相似,所有原子处于同一平面上,则 中碳原子的杂化方式为
中碳原子的杂化方式为___________ ,二茂铁中存在___________ (填标号)作用力。
A.金属键 B. 键 C.
键 C. 键 D.氢键
键 D.氢键
③普鲁士蓝的结构特征是Fe(Ⅱ)、Fe(Ⅲ)分别占据立方体互不相邻的顶点,而 位于立方体棱心上,每间隔一个立方体在立方体体心含有一个
位于立方体棱心上,每间隔一个立方体在立方体体心含有一个 ,根据其结构特点,推出其化学式为
,根据其结构特点,推出其化学式为___________ 。
(3)铁的晶胞如图3所示,其堆积方式为___________ (填标号),铁原子的配位数为___________ ,若铁原子的半径为apm,则铁晶胞密度
___________ g/cm3 (用NA表示阿伏加德罗常数的值)。
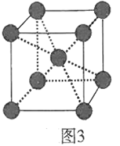
A.简单立方堆积 B.体心立方堆积 C.六方最密堆积 D.面心立方堆积

(1)基态Fe原子核外电子排布式为
(2)铁的化合物在生产生活及科学研究方面应用非常广泛。
①
 是一种新型光电催化剂。第四电离能大小关系是I4(Co)
是一种新型光电催化剂。第四电离能大小关系是I4(Co) ②由环戊二烯离子(
 )与Fe(Ⅱ)形成的二茂铁[
)与Fe(Ⅱ)形成的二茂铁[ ]结构如图2所示。已知
]结构如图2所示。已知 与苯结构相似,所有原子处于同一平面上,则
与苯结构相似,所有原子处于同一平面上,则 中碳原子的杂化方式为
中碳原子的杂化方式为
A.金属键 B.
 键 C.
键 C. 键 D.氢键
键 D.氢键③普鲁士蓝的结构特征是Fe(Ⅱ)、Fe(Ⅲ)分别占据立方体互不相邻的顶点,而
 位于立方体棱心上,每间隔一个立方体在立方体体心含有一个
位于立方体棱心上,每间隔一个立方体在立方体体心含有一个 ,根据其结构特点,推出其化学式为
,根据其结构特点,推出其化学式为(3)铁的晶胞如图3所示,其堆积方式为


A.简单立方堆积 B.体心立方堆积 C.六方最密堆积 D.面心立方堆积
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】含钒化合物广泛用于冶金、化工行业。由富钒废渣(含V2O3、V2O4和Na2O•Al2O3•4SiO2、FeO)制备V2O5的一种流程如下:

查阅资料:①部分含钒物质在水溶液中的主要存在形式如下:
②本工艺中,生成氢氧化物沉淀的pH如下:
回答下列问题:
(1)写出基态V原子的价电子排布式_________________________ 。
(2)“焙烧”中,将“研磨”所得粉末与O2逆流混合的目的为___________________ ;所生成的气体A可在___________ 工序中再利用。
(3)“酸浸”中V元素发生的离子反应方程式__________________________ 。
(4)滤渣2含有的物质为__________________ 。
(5)“转化Ⅱ”需要调整pH范围为__________ ,“转化Ⅲ”中含钒物质反应的离子方程式为_________________________________________________ 。
(6)“沉钒”中加入过量NH4Cl有利于晶体析出,其原因为_________________ 。

查阅资料:①部分含钒物质在水溶液中的主要存在形式如下:
pH | <1 | 1~4 | 4~6 | 6~8.5 | 8.5~13 | >13 |
主要形式 | VO | V2O5 | 多矾酸根 | VO | 多矾酸根 | VO |
备注 | 多矾酸盐在水中溶解度较小 | |||||
物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
开始沉淀pH | 7.0 | 1.9 | 3.2 |
沉淀完全pH | 9.0 | 3.2 | 4.7 |
(1)写出基态V原子的价电子排布式
(2)“焙烧”中,将“研磨”所得粉末与O2逆流混合的目的为
(3)“酸浸”中V元素发生的离子反应方程式
(4)滤渣2含有的物质为
(5)“转化Ⅱ”需要调整pH范围为
(6)“沉钒”中加入过量NH4Cl有利于晶体析出,其原因为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
真题
解题方法
【推荐1】主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍。X、Y和Z分属不同的周期,他们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
(1)W元素原子的L层电子排布式为_________ ,W3分子的空间构型为_________ ;
(2)X单质与水发生主要反应的化学方程式为____________________________ ;
(3)化合物M的化学式为________ ,其晶体结构与NaCl相同,而熔点高于NaCl。M熔点较高的原因是________ 。将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有_________ ,O—C—O的键角约为_________ ;
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X︰Y︰Z=_________ ;
(5)含有元素Z的盐的焰色反应为_________ 色。许多金属盐都可以发生焰色反应,其原因是________________________________________________________ 。
(1)W元素原子的L层电子排布式为
(2)X单质与水发生主要反应的化学方程式为
(3)化合物M的化学式为
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X︰Y︰Z=
(5)含有元素Z的盐的焰色反应为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】a、b、c、d、e、f是H、C、N、Na、Si、Cu六种元素中的其中一种,已知:图1表示的是这六种元素单质的熔点高低顺序,其中c、d均是热和电的良导体,f形成的某种单质硬度最大。

回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为______ (用元素符号表示)。
(2)元素b的单质的一个分子中含有____ 个σ键和______ 个π键。
(3)元素c的单质的晶体堆积方式类型是_______ ;若c单质分别与氟气和氯气形成化合物甲和乙,则甲的晶格能______ 乙的晶格能(填“>”、“<”或“=”)。
(4)元素d的单质基态原子的价电子排布式为______ (用NA表示阿伏伽德罗常数的值)。
(5)元素e和f可形成化合物丙(丙的晶胞结构如图2所示),则丙的化学式为_____ ;丙的晶体类型为_______ ,在丙中,每个e原子周围最近的e原子数目为______ ,若晶胞的边长为a pm,则丙的密度为________ 。

回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为
(2)元素b的单质的一个分子中含有
(3)元素c的单质的晶体堆积方式类型是
(4)元素d的单质基态原子的价电子排布式为
(5)元素e和f可形成化合物丙(丙的晶胞结构如图2所示),则丙的化学式为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(化学-物质结构与性质)
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
A通常显_____ 价,A的电负性________ B的电负性(填“>”、“<”或“=”)。
(2)紫外光的光子所具有的能量约为399 kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因__________________________________________________________________________ 。
组成蛋白质的最简单的氨基酸中的碳原子杂化类型是________________ 。
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),
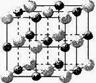
其中3种离子晶体的晶格能数据如下表:
则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:_________________ 。
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有_______ 个。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是_____________ 。
(5)某配合物的分子结构如右图所示,其分子内不含有____ (填序号)。
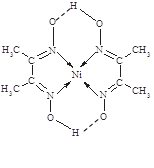
A.离子键 B.极性键
C.金属键 D.配位键
E.氢键 F.非极性键
(6)温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2。
若有1mol CH4生成,则有______ molσ键和______ molπ键断裂。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
A通常显
(2)紫外光的光子所具有的能量约为399 kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因
| 共价键 | C-C | C-N | C-S |
| 键能/ kJ·mol-1 | 347 | 305 | 259 |
组成蛋白质的最简单的氨基酸中的碳原子杂化类型是
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),

其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是
(5)某配合物的分子结构如右图所示,其分子内不含有

A.离子键 B.极性键
C.金属键 D.配位键
E.氢键 F.非极性键
(6)温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2。
若有1mol CH4生成,则有
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】镁及其合金是用途很广的金属材料。大量的镁是从海水中提取的,海水提镁的主要步骤如图所示:

回答下列问题:
(1)Na元素位于元素周期表的_____ (填“s”、“p”、“d”或“ds”)区。
(2)元素Cl、Mg、Na的原子半径由大到小的顺序为_____ (用元素符号表示)。
(3) 属于
属于_____ (填“分子”、“离子”或“共价”)晶体,含有的化学键类型为_____ 。
(4)氯化钠晶体结构模型如图所示:

①氯化钠晶体中,每个离子可吸引周围_____ 个带异性电荷的离子。
②氯化钠晶体中,每个 周围最近且等距离的
周围最近且等距离的 有
有_____ 个。
③设晶胞边长为anm, 为阿伏加德罗常数的值,则NaCl晶体的密度为
为阿伏加德罗常数的值,则NaCl晶体的密度为_____  。
。
(5)氟与氯位于同一主族,查阅资料可知: 的熔点为1534K,NaF的熔点为1266K,NaF的熔点低于
的熔点为1534K,NaF的熔点为1266K,NaF的熔点低于 的熔点的原因为
的熔点的原因为_____ 。

回答下列问题:
(1)Na元素位于元素周期表的
(2)元素Cl、Mg、Na的原子半径由大到小的顺序为
(3)
 属于
属于(4)氯化钠晶体结构模型如图所示:

①氯化钠晶体中,每个离子可吸引周围
②氯化钠晶体中,每个
 周围最近且等距离的
周围最近且等距离的 有
有③设晶胞边长为anm,
 为阿伏加德罗常数的值,则NaCl晶体的密度为
为阿伏加德罗常数的值,则NaCl晶体的密度为 。
。(5)氟与氯位于同一主族,查阅资料可知:
 的熔点为1534K,NaF的熔点为1266K,NaF的熔点低于
的熔点为1534K,NaF的熔点为1266K,NaF的熔点低于 的熔点的原因为
的熔点的原因为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】元素周期表是学习化学的重要工具。下图是元素周期表的一部分,其中①~⑨代表的是对应位置的元素。回答以下问题。
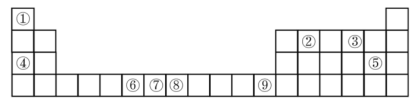
(1)①~⑨代表的9种元素中,②③的电负性_______ >_______ (填元素符号,后同),写出⑨代表的Zn元素基态原子的电子排布式_______ 。
(2)①与②形成简单化合物甲,①与③形成简单化合物乙,甲的沸点_______ 乙的沸点(填“高于”或“低于”),主要原因是_______ 。
(3)⑥⑦⑧三种元素处于_______ 区(填s,p,d,ds),它们分别为铬、锰、铁,其基态原子中未成对电子数由多到少的顺序是_______ 。
(4)关于④和⑤形成的化合物的晶体中,下列说法不正确 的是_______ 。
a.该晶体是共价晶体
b.该晶体固态和液态时均不导电
c.该晶体熔化时需要能量来破坏离子键
d.该晶体中每个④周围与它距离最近且相等的同种微粒有12个

(1)①~⑨代表的9种元素中,②③的电负性
(2)①与②形成简单化合物甲,①与③形成简单化合物乙,甲的沸点
(3)⑥⑦⑧三种元素处于
(4)关于④和⑤形成的化合物的晶体中,下列说法
a.该晶体是共价晶体
b.该晶体固态和液态时均不导电
c.该晶体熔化时需要能量来破坏离子键
d.该晶体中每个④周围与它距离最近且相等的同种微粒有12个
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】某学者分别使用 和
和 作催化剂对燃煤烟气脱硝脱硫进行了研究。
作催化剂对燃煤烟气脱硝脱硫进行了研究。
(1)催化剂制备。在60~100℃条件下,向足量NaOH溶液中通入 一段时间,再加入适量新制
一段时间,再加入适量新制 溶液,充分反应后制得混合物X;向混合物X中加入
溶液,充分反应后制得混合物X;向混合物X中加入 溶液,充分反应后经磁铁吸附、洗涤、真空干燥,制得
溶液,充分反应后经磁铁吸附、洗涤、真空干燥,制得 催化剂。
催化剂。
①通入 的目的是
的目的是_______ 。
②混合物X与 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(2)催化剂研究。如图-1所示,当其他条件一定时,分别在无催化剂、 作催化剂、
作催化剂、 作催化剂的条件下,测定
作催化剂的条件下,测定 浓度对模拟烟气(含一定比例的NO、
浓度对模拟烟气(含一定比例的NO、 、
、 、
、 )中NO和
)中NO和 脱除率的影响,NO脱除率与
脱除率的影响,NO脱除率与 浓度的关系如图-2所示。
浓度的关系如图-2所示。 氧化。·OH产生机理如下。
氧化。·OH产生机理如下。
反应Ⅰ: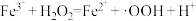 (慢反应)
(慢反应)
反应Ⅱ: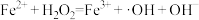 (快反应)
(快反应)
①与 作催化剂相比,相同条件下
作催化剂相比,相同条件下 作催化剂时NO脱除率更高,其原因是
作催化剂时NO脱除率更高,其原因是_______ 。
②NO部分被氧化成 。
。 被NaOH溶液吸收生成两种含氧酸钠盐,该反应的离子方程式为
被NaOH溶液吸收生成两种含氧酸钠盐,该反应的离子方程式为_______ 。
③实验表示·OH氧化 的速率比氧化NO速率慢。但在无催化剂、
的速率比氧化NO速率慢。但在无催化剂、 作催化剂、
作催化剂、 作催化剂的条件下,测得
作催化剂的条件下,测得 脱除率几乎均为100%的原因是
脱除率几乎均为100%的原因是_______ 。
(3)催化剂的回收。将回收的废催化剂进行处理,制成的改性 是一种优良的磁性材料,该
是一种优良的磁性材料,该 晶胞的
晶胞的 的结构如图-3所示,研究发现结构中的
的结构如图-3所示,研究发现结构中的 只可能出现在图中某一“▲”所示位置上,请确定
只可能出现在图中某一“▲”所示位置上,请确定 所在晶胞的位置
所在晶胞的位置_______ ,请说明确定理由:_______ 。
 和
和 作催化剂对燃煤烟气脱硝脱硫进行了研究。
作催化剂对燃煤烟气脱硝脱硫进行了研究。(1)催化剂制备。在60~100℃条件下,向足量NaOH溶液中通入
 一段时间,再加入适量新制
一段时间,再加入适量新制 溶液,充分反应后制得混合物X;向混合物X中加入
溶液,充分反应后制得混合物X;向混合物X中加入 溶液,充分反应后经磁铁吸附、洗涤、真空干燥,制得
溶液,充分反应后经磁铁吸附、洗涤、真空干燥,制得 催化剂。
催化剂。①通入
 的目的是
的目的是②混合物X与
 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(2)催化剂研究。如图-1所示,当其他条件一定时,分别在无催化剂、
 作催化剂、
作催化剂、 作催化剂的条件下,测定
作催化剂的条件下,测定 浓度对模拟烟气(含一定比例的NO、
浓度对模拟烟气(含一定比例的NO、 、
、 、
、 )中NO和
)中NO和 脱除率的影响,NO脱除率与
脱除率的影响,NO脱除率与 浓度的关系如图-2所示。
浓度的关系如图-2所示。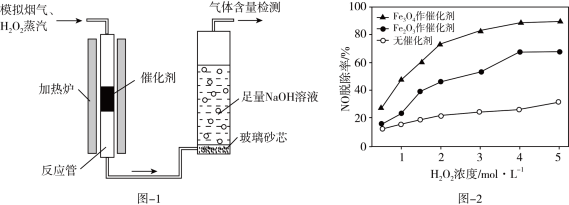
 氧化。·OH产生机理如下。
氧化。·OH产生机理如下。反应Ⅰ:
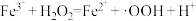 (慢反应)
(慢反应)反应Ⅱ:
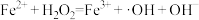 (快反应)
(快反应)①与
 作催化剂相比,相同条件下
作催化剂相比,相同条件下 作催化剂时NO脱除率更高,其原因是
作催化剂时NO脱除率更高,其原因是②NO部分被氧化成
 。
。 被NaOH溶液吸收生成两种含氧酸钠盐,该反应的离子方程式为
被NaOH溶液吸收生成两种含氧酸钠盐,该反应的离子方程式为③实验表示·OH氧化
 的速率比氧化NO速率慢。但在无催化剂、
的速率比氧化NO速率慢。但在无催化剂、 作催化剂、
作催化剂、 作催化剂的条件下,测得
作催化剂的条件下,测得 脱除率几乎均为100%的原因是
脱除率几乎均为100%的原因是(3)催化剂的回收。将回收的废催化剂进行处理,制成的改性
 是一种优良的磁性材料,该
是一种优良的磁性材料,该 晶胞的
晶胞的 的结构如图-3所示,研究发现结构中的
的结构如图-3所示,研究发现结构中的 只可能出现在图中某一“▲”所示位置上,请确定
只可能出现在图中某一“▲”所示位置上,请确定 所在晶胞的位置
所在晶胞的位置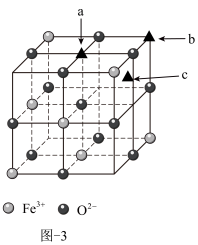
您最近半年使用:0次






