已知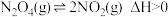 在瞬间即可达成化学平衡。NO2和N2O4混合气体体积由V压缩至
在瞬间即可达成化学平衡。NO2和N2O4混合气体体积由V压缩至 时,相关数据变化如下表。根据表中数据得出若干结论,下列结论
时,相关数据变化如下表。根据表中数据得出若干结论,下列结论不正确 的是
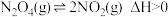 在瞬间即可达成化学平衡。NO2和N2O4混合气体体积由V压缩至
在瞬间即可达成化学平衡。NO2和N2O4混合气体体积由V压缩至 时,相关数据变化如下表。根据表中数据得出若干结论,下列结论
时,相关数据变化如下表。根据表中数据得出若干结论,下列结论| 温度/L | 气体的总压强/Pa | NO2的物质的量浓度/ mol·L-1 | |
 | 298 | 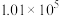 | 1.28×10-2 |
 | 311 | 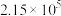 | 2.80×10-2 |
A.体积由V压缩至 时,NO2的物质的量减少 时,NO2的物质的量减少 |
| B.正反应和逆反应的活化能均较低 |
| C.体积缩小后混合气体的颜色加深 |
| D.其它条件不变,温度升高,该反应正向移动 |
更新时间:2023/05/04 16:52:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】 、
、 、
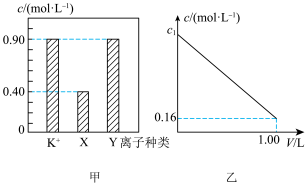
、 三种固体溶于水得到的溶液M中部分离子的物质的量浓度如图甲所示。取200
三种固体溶于水得到的溶液M中部分离子的物质的量浓度如图甲所示。取200 混合溶液加水稀释,测得
混合溶液加水稀释,测得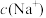 随溶液体积的变化如图乙所示。下列说法正确的是
随溶液体积的变化如图乙所示。下列说法正确的是
 、
、 、
、 三种固体溶于水得到的溶液M中部分离子的物质的量浓度如图甲所示。取200
三种固体溶于水得到的溶液M中部分离子的物质的量浓度如图甲所示。取200 混合溶液加水稀释,测得
混合溶液加水稀释,测得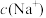 随溶液体积的变化如图乙所示。下列说法正确的是
随溶液体积的变化如图乙所示。下列说法正确的是
A. |
B.向混合液中加入0.4 的 的 可使 可使 完全沉淀 完全沉淀 |
C.溶液M中 物质的量浓度为 物质的量浓度为 |
D. 与 与 物质的量之比为 物质的量之比为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】现有盐酸和硫酸混合溶液 100 mL,其中 c(Cl-)=1.6 mol·L-1,现将其分成两等份,往其中一份中滴加足量 BaCl2溶液,产生2.33g白色沉淀,往另一份中投入足量铁片,放出标准状况下VL气体。下列判断正确的是
A.原混合酸中 n(SO )=0.01 mol )=0.01 mol | B.原混合酸中 n(H+)=0.18 mol |
| C.V=1.12 | D.原溶液中盐酸、硫酸物质的量之和为 0.20 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一种催化 制备
制备 的部分反应历程和能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
的部分反应历程和能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
 制备
制备 的部分反应历程和能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
的部分反应历程和能量变化如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是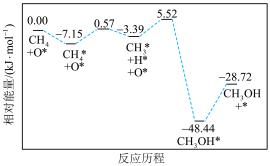
| A.有4个基元反应 |
B.升温有利于 的吸附 的吸附 |
C.反应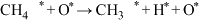 不是决速步 不是决速步 |
D.增大 的投入量,可提高其平衡转化率 的投入量,可提高其平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
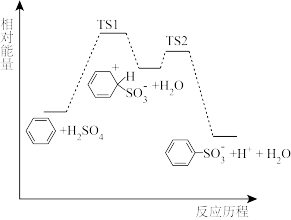
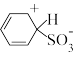
【推荐2】铁的配合物离子(用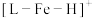 表示)催化某反应的一种反应机理和相对能量的变化情况如下图所示:
表示)催化某反应的一种反应机理和相对能量的变化情况如下图所示:
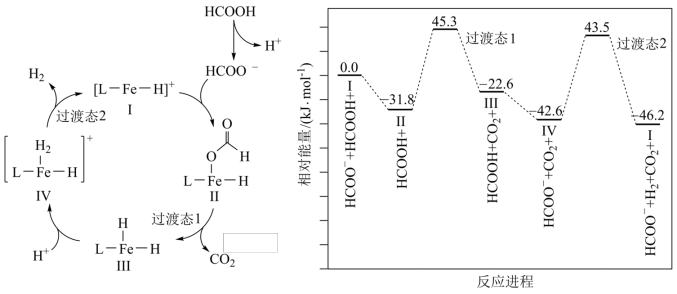
下列说法错误的是
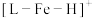 表示)催化某反应的一种反应机理和相对能量的变化情况如下图所示:
表示)催化某反应的一种反应机理和相对能量的变化情况如下图所示:
下列说法错误的是
A.该过程的热化学方程式为  |
B. 浓度过大或者过小,均导致反应速率降低 浓度过大或者过小,均导致反应速率降低 |
| C.加催化剂,可以提高该反应活化分子百分数,从而加快反应速率 |
| D.该过程的总反应速率由Ⅳ→Ⅰ步骤决定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是( )
A.H2(g)+I2(g) 2HI(g)反应达平衡后,压缩体积气体颜色变深 2HI(g)反应达平衡后,压缩体积气体颜色变深 |
| B.Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
C.N2(g)+3H2(g) 2NH3(g)△H<0,工业上采用高压条件更有利于合成氨 2NH3(g)△H<0,工业上采用高压条件更有利于合成氨 |
| D.浸泡在冰水中的NO2球的红棕色明显变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一定温度下,将1mol 和3mol
和3mol 充入体积为11的恒容密闭容器中发生反应并达到平衡:
充入体积为11的恒容密闭容器中发生反应并达到平衡:
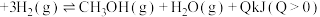 ,测得平衡混合气体中
,测得平衡混合气体中 的物质的量分数为25%。下列说法不正确的是
的物质的量分数为25%。下列说法不正确的是
 和3mol
和3mol 充入体积为11的恒容密闭容器中发生反应并达到平衡:
充入体积为11的恒容密闭容器中发生反应并达到平衡:
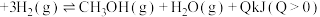 ,测得平衡混合气体中
,测得平衡混合气体中 的物质的量分数为25%。下列说法不正确的是
的物质的量分数为25%。下列说法不正确的是| A.平衡混合气体中C原子的物质的量是1mol |
| B.达平衡后若升高温度,正反应速率增大的程度比逆反应速率增大的程度小 |
C.该反应的化学平衡常数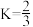 |
D.其他条件相同时,若起始充入2mol 和6mol 和6mol ,达到平衡时 ,达到平衡时 的物质的量分数大于25% 的物质的量分数大于25% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 往饱和Na2CO3溶液中通入CO2 | 溶液变浑浊 | 溶解度:NaHCO3<Na2CO3 |
| B | 取两份新制氯水,分别滴加AgNO3溶液和淀粉KI溶液 | 前者有白色沉淀,后者溶液变蓝色 | 氯气与水的反应存在限度 |
| C | 压缩装有NO2和N2O4混合气体(已达平衡)的容器 | 气体颜色先变深后稍变浅 | 平衡向生成N2O4的方向移动 |
| D | 将SO2气体通入Ca(ClO)2溶液中 | 产生白色沉淀 | 酸性: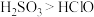 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
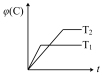
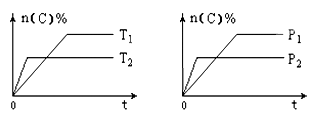
【推荐2】已知可逆反应aA(g)+bB(g) cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
 cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
| A.T1>T2 | B.△H<0 | C.P1>P2 | D.a+b>c+d |
您最近一年使用:0次

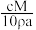
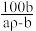



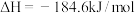 ,其中
,其中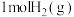 和
和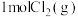 反应生成2HCl(g)表示“每摩尔反应”
反应生成2HCl(g)表示“每摩尔反应”