八水合磷酸亚铁[ ,
, ]难溶于水和醋酸,溶于无机酸,可作为铁质强化剂。某实验室利用如图装置制备八水合磷酸亚铁,步骤如下:
]难溶于水和醋酸,溶于无机酸,可作为铁质强化剂。某实验室利用如图装置制备八水合磷酸亚铁,步骤如下:
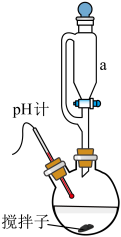
ⅰ.在烧瓶中先加入维生素C稀溶液作底液;
ⅱ.通过仪器a向烧瓶中滴入足量 与
与 的混合溶液;
的混合溶液;
ⅲ.再滴入
 的
的 溶液,保持
溶液,保持 为6左右,水浴加热且不断搅拌至反应充分后静置;
为6左右,水浴加热且不断搅拌至反应充分后静置;
ⅳ.将烧瓶中混合物进行抽滤、洗涤、低温干燥,得到 产品。
产品。
回答下列问题:
(1) 的价电子排布式为
的价电子排布式为___________ , 的空间结构为
的空间结构为___________
(2)仪器a的名称是___________ ,配制 溶液时需将蒸馏水事先煮沸、冷却,其目的是
溶液时需将蒸馏水事先煮沸、冷却,其目的是___________
(3)用维生素C稀溶液作底液而不用铁粉的主要原因是___________
(4)合成时需保持 为6左右的原因是
为6左右的原因是___________
(5)产率的计算:称取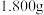 产品,用足量的稀硫酸溶解后,立即用
产品,用足量的稀硫酸溶解后,立即用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。滴定过程中的离子方程式为
。滴定过程中的离子方程式为___________
 ,
, ]难溶于水和醋酸,溶于无机酸,可作为铁质强化剂。某实验室利用如图装置制备八水合磷酸亚铁,步骤如下:
]难溶于水和醋酸,溶于无机酸,可作为铁质强化剂。某实验室利用如图装置制备八水合磷酸亚铁,步骤如下:
ⅰ.在烧瓶中先加入维生素C稀溶液作底液;
ⅱ.通过仪器a向烧瓶中滴入足量
 与
与 的混合溶液;
的混合溶液;ⅲ.再滴入

 的
的 溶液,保持
溶液,保持 为6左右,水浴加热且不断搅拌至反应充分后静置;
为6左右,水浴加热且不断搅拌至反应充分后静置;ⅳ.将烧瓶中混合物进行抽滤、洗涤、低温干燥,得到
 产品。
产品。回答下列问题:
(1)
 的价电子排布式为
的价电子排布式为 的空间结构为
的空间结构为(2)仪器a的名称是
 溶液时需将蒸馏水事先煮沸、冷却,其目的是
溶液时需将蒸馏水事先煮沸、冷却,其目的是(3)用维生素C稀溶液作底液而不用铁粉的主要原因是
(4)合成时需保持
 为6左右的原因是
为6左右的原因是(5)产率的计算:称取
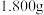 产品,用足量的稀硫酸溶解后,立即用
产品,用足量的稀硫酸溶解后,立即用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。滴定过程中的离子方程式为
。滴定过程中的离子方程式为
更新时间:2023-04-22 14:37:01
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】如下图所示,此装置可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。填写下列空白:
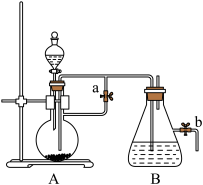
(1)B中盛有一定量的___________ 溶液,A中应预先加入的药品是___________ 。A中反应的离子方程式___________ 。
(2)实验开始时先将止水夹a___________ (填“打开”或“关闭”)。
(3)简述生成Fe(OH)2的操作过程___________ 。
(4)实验完毕,打开b处止水夹,放入一部分空气,此时B瓶中发生的反应为___________
(5)除去Fe(OH)3固体中混有的Al(OH)3:试剂___________ ,其所发生的离子方程式___________ ;

(1)B中盛有一定量的
(2)实验开始时先将止水夹a
(3)简述生成Fe(OH)2的操作过程
(4)实验完毕,打开b处止水夹,放入一部分空气,此时B瓶中发生的反应为
(5)除去Fe(OH)3固体中混有的Al(OH)3:试剂
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】Ⅰ.铁是一种常见的金属,它的单质及化合物在生活生产中处处可见。
(1)苹果中含有丰富的铁元素,新榨的苹果汁是浅绿色的,在空气中久置后会变成黄色,原因是___________ ,若再向其中加入少量的维生素C,又将恢复浅绿色,上述过程中,氧气是___________ 剂(选填“氧化”或“还原”,下同),维生素C是___________ 剂。
Ⅱ.铁及其重要化合物的“价类二维图”如下图所示。

(2)该“价类二维图”中缺失的类别A应为___________ 。
(3)要实现Fe转化为Fe3O4,除了将Fe与氧气点燃外,另外的方法是(写出化学方程式)___________ 。
(4)下列关于金属冶炼的说法中正确的是____;
(5)有关合金的说法错误的是____。
(6)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为____。
(7)在烧制砖瓦时,用黏土做成的坯经过烘烧后,铁的化合物转化成而制得红色砖瓦____。
(8)要实现Fe转化为Fe2+,可选用足量的____。
(9)下列各组离子在溶液中能大量共存的是____。
(10)有失去标签的NaCl、FeCl2、FeCl3、MgCl2四种溶液,只需要一种试剂就可以把它们鉴别开来,这种试剂是____。
Ⅲ.某化学兴趣小组同学设计以下实验探究氢氧化亚铁的制备:
两组同学分别设计如下实验探究能较长时间观察到白色Fe(OH)2沉淀的制取方法。
A组实验:用NaOH溶液和FeSO4溶液直接反应。(如图)

(11)FeSO4可由铁粉还原Fe2(SO4)3制得,反应的离子方程式是:___________ 。
(12)该方法能观察到白色Fe(OH)2沉淀,但沉淀颜色快速发生变化,其颜色变化为___________ 。
B组实验:选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。

(13)实验时,先___________ (填“打开”或“关闭”)止水夹K,然后打开分液漏斗的玻璃塞和活塞,使稀硫酸与铁粉反应,一段时间后,___________ (填“打开”或“关闭”)止水夹K,制得白色Fe(OH)2沉淀,且沉淀能持续一段时间不变色。
(1)苹果中含有丰富的铁元素,新榨的苹果汁是浅绿色的,在空气中久置后会变成黄色,原因是
Ⅱ.铁及其重要化合物的“价类二维图”如下图所示。

(2)该“价类二维图”中缺失的类别A应为
(3)要实现Fe转化为Fe3O4,除了将Fe与氧气点燃外,另外的方法是(写出化学方程式)
(4)下列关于金属冶炼的说法中正确的是____;
| A.通过电解饱和食盐水制备金属钠 |
| B.热还原法常用的还原剂有CO、H2、C等 |
| C.金属Mg、Al均能通过电解熔融氯化物的方法获得 |
| D.人类历史上金属被发现的顺序与金属的活泼性无关 |
(5)有关合金的说法错误的是____。
| A.熔点通常低于组成金属 | B.任意两种金属均可以形成合金 |
| C.钢比生铁的含碳量低 | D.可能含有非金属 |
(6)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为____。
| A.干垃圾 | B.湿垃圾 | C.有毒有害垃圾 | D.可回收垃圾 |
(7)在烧制砖瓦时,用黏土做成的坯经过烘烧后,铁的化合物转化成而制得红色砖瓦____。
| A.Fe2O3 | B.Fe3O4 | C.FeO | D.Fe(OH)3 |
(8)要实现Fe转化为Fe2+,可选用足量的____。
| A.浓硫酸 | B.氯气 | C.稀硝酸 | D.稀硫酸 |
(9)下列各组离子在溶液中能大量共存的是____。
A.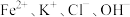 | B.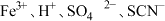 |
C. | D. |
(10)有失去标签的NaCl、FeCl2、FeCl3、MgCl2四种溶液,只需要一种试剂就可以把它们鉴别开来,这种试剂是____。
| A.氨水 | B.盐酸 | C.Na2SO4溶液 | D.KSCN溶液 |
Ⅲ.某化学兴趣小组同学设计以下实验探究氢氧化亚铁的制备:
两组同学分别设计如下实验探究能较长时间观察到白色Fe(OH)2沉淀的制取方法。
A组实验:用NaOH溶液和FeSO4溶液直接反应。(如图)

(11)FeSO4可由铁粉还原Fe2(SO4)3制得,反应的离子方程式是:
(12)该方法能观察到白色Fe(OH)2沉淀,但沉淀颜色快速发生变化,其颜色变化为
B组实验:选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。

(13)实验时,先
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】短周期主族元素X、Y、Z、R的原子序数依次增大。X原子的最外层电子数比Y的次外层电子数多3;Y和R同主族,且原子序数R是Y的2倍,Z是地壳中含量最多的金属元素;W形成的合金是目前使用最广泛的金属合金。回答下列问题:
(1)X在元素周期表中的位置是___________ ,Z元素的原子结构示意图是___________ 。
(2)R的简单氢化物电子式为___________ ,简单氢化物的稳定性X___________ Y(填“>”或“<”)。
(3)下列可用于实验室制备W的低价氧化物对应的水化物(苯是一种有机物,难溶于水,密度比水小)的装置有___________ 。
(4)无机盐W2(RY4)3在T.F菌存在的酸性溶液中可实现天然气的催化除杂,其原理如图所示:

写出过程i中发生反应的离子方程式___________ 。
(1)X在元素周期表中的位置是
(2)R的简单氢化物电子式为
(3)下列可用于实验室制备W的低价氧化物对应的水化物(苯是一种有机物,难溶于水,密度比水小)的装置有

(4)无机盐W2(RY4)3在T.F菌存在的酸性溶液中可实现天然气的催化除杂,其原理如图所示:

写出过程i中发生反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】硫酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物。一片药片所含铁元素60mg,一盒硫酸亚铁片含药100片。
(1)每盒硫酸亚铁中含铁元素的物质的量为_______ mol(结果保留小数点后一位);
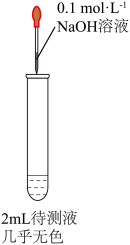
(2)甲同学为检验药片中 ,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如图所示),预测观察到的现象是:
,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如图所示),预测观察到的现象是:_______ ;
(3)乙同学认为药品有部分被氧化,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如下图所示)
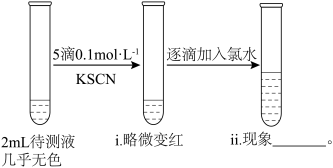
ⅱ中的现象是:_______ ;是由于 被氯水氧化,反应的离子方程式为
被氯水氧化,反应的离子方程式为_______ ;
(4)丙同学认为上述实验不能充分证明药品被部分氧化,应补充的实验是:_______ 。
(1)每盒硫酸亚铁中含铁元素的物质的量为
(2)甲同学为检验药片中
 ,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如图所示),预测观察到的现象是:
,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如图所示),预测观察到的现象是:
(3)乙同学认为药品有部分被氧化,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如下图所示)

ⅱ中的现象是:
 被氯水氧化,反应的离子方程式为
被氯水氧化,反应的离子方程式为(4)丙同学认为上述实验不能充分证明药品被部分氧化,应补充的实验是:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】以菱镁矿(主要成分是碳酸镁,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体(MgSO4·7H2O)的流程如图:
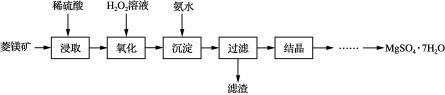
(1)“浸取”时通常将菱镁矿石进行粉碎,其目的是___ 。
(2)写出碳酸镁与稀硫酸反应的化学方程式___ 。
(3)“氧化”和“沉淀”是将“浸取”过程中产生的Fe2+转化为Fe(OH)3沉淀,则“过滤”所得滤液中含有的阳离子主要有___ 和___ 。

(1)“浸取”时通常将菱镁矿石进行粉碎,其目的是
(2)写出碳酸镁与稀硫酸反应的化学方程式
(3)“氧化”和“沉淀”是将“浸取”过程中产生的Fe2+转化为Fe(OH)3沉淀,则“过滤”所得滤液中含有的阳离子主要有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显血红色,它们相互转化关系如图所示。

请回答:
(1)写出A与B反应的化学方程式:______________________ 。
(2)写出第④步反应的离子方程式为______________________ 。
(3)写出向F溶液中通入B时发生反应的离子方程式________________ 。
(4)写出Cu与D溶液反应的离子方程式___________________________ 。
(5)用离子方程式表示D溶液中滴加KSCN溶液显红色的原因__________________ 。
(6)向F溶液中滴入NaOH溶液过程中发生的氧化还原反应化学方程式为_______________ 。

请回答:
(1)写出A与B反应的化学方程式:
(2)写出第④步反应的离子方程式为
(3)写出向F溶液中通入B时发生反应的离子方程式
(4)写出Cu与D溶液反应的离子方程式
(5)用离子方程式表示D溶液中滴加KSCN溶液显红色的原因
(6)向F溶液中滴入NaOH溶液过程中发生的氧化还原反应化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】氮元素与氢元素能形成多种化合物,在工业、农业和国防等方面用途非常广泛,例如:氨气、肼(N2H4)、叠氮酸(HN3)……等,请回答下列问题:
(1)N位于周期表中____ 区,基态N原子的价电子排布式为____ 。
(2)N2H4分子的电子式为____ ,其中N采取____ 杂化。
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N 。请写出一种与N
。请写出一种与N 互为等电子体的分子的化学式
互为等电子体的分子的化学式____ ;叠氮化物易与过渡金属元素形成配合物,如:[Fe(N3)(NH3)5]SO4,在该配合物中Fe的配位数为____ ,SO 的立体构型为
的立体构型为____ 。
(4)已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+,1mol该离子含有σ键的数目为____ 。
(5)氮与铝形成的某种晶体的晶胞如图所示。
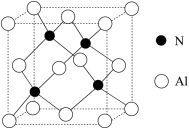
①该晶体的化学式为____ 。
②已知该晶体的密度为dg·cm−3,N和Al的半径分别为apm和bpm,阿伏加德罗常数值为NA。用含a、b、d和NA的式子表示该晶体中原子的空间利用率____ (用含a、b、d和NA的式子表示)。
(1)N位于周期表中
(2)N2H4分子的电子式为
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N
 。请写出一种与N
。请写出一种与N 互为等电子体的分子的化学式
互为等电子体的分子的化学式 的立体构型为
的立体构型为(4)已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+,1mol该离子含有σ键的数目为
(5)氮与铝形成的某种晶体的晶胞如图所示。

①该晶体的化学式为
②已知该晶体的密度为dg·cm−3,N和Al的半径分别为apm和bpm,阿伏加德罗常数值为NA。用含a、b、d和NA的式子表示该晶体中原子的空间利用率
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】碳酸锂(Li2CO3)微溶于水 、稀酸, 其溶解度随温度的升高而降低,不溶于C2H5OH,医学上可用其治疗精神忧郁症。以钴酸锂废料(主要含有LiCoO2,难溶于水,还含有少量Al2O3)为原料制备Co(OH)2及Li2CO3的工艺流程如图所示。
(1)“酸浸还原”时得到的溶液中阴离子主要为 ,
, 的空间构型为
的空间构型为___________ ,LiCoO2发生反应的离子方程式为___________ 。
(2)“滤渣1”中含有少量 Co(OH)2,原因为___________ 。
(3)常温下[Ksp[Co(OH)2]=1.0×10−15,当c(Co2+ )= 10−5 mol·L−1时视作“沉钴”完全,此时溶液的pH=___________ ;Co(OH)2久置于空气中转化为棕色的Co(OH)3,化学方程式为 ___________ 。
(4)“沉锂”所得的溶液中主要含有硫酸钠,则试剂X为___________ (填化学式)溶液。
(5)“系列操作”为蒸发浓缩、___________ 、洗涤、 干燥,洗涤时所用到的玻璃仪器为烧杯、漏斗、___________ 。

(1)“酸浸还原”时得到的溶液中阴离子主要为
 ,
, 的空间构型为
的空间构型为(2)“滤渣1”中含有少量 Co(OH)2,原因为
(3)常温下[Ksp[Co(OH)2]=1.0×10−15,当c(Co2+ )= 10−5 mol·L−1时视作“沉钴”完全,此时溶液的pH=
(4)“沉锂”所得的溶液中主要含有硫酸钠,则试剂X为
(5)“系列操作”为蒸发浓缩、
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】青蒿素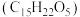 是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
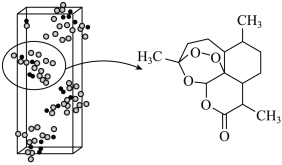
(1)提取青蒿素:在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚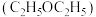 提取,效果更好。
提取,效果更好。
①乙醚沸点低于乙醇,原因是___________ 。
②用乙醚提取效果更好,原因是___________ 。
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。比较青蒿素分子中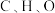 的原子核附近电子云密度大小:
的原子核附近电子云密度大小:___________ 。
②图中晶胞的棱长分别为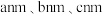 ,晶体的密度为
,晶体的密度为___________  。(用
。(用 表示阿伏加德罗常数;
表示阿伏加德罗常数; ;青蒿素的相对分子质量为282)
;青蒿素的相对分子质量为282)
③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是___________ 。
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效:一定条件下,用 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。
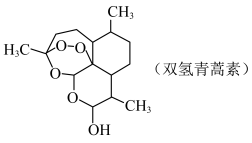
①双氢青蒿素分子中碳原子的杂化方式为___________ 。
② 的空间结构为
的空间结构为___________ ,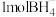 中有
中有___________  配位键。
配位键。
③比较水溶性:双氢青蒿素___________ (填“ ”)青蒿素。
”)青蒿素。
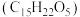 是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
(1)提取青蒿素:在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚
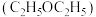 提取,效果更好。
提取,效果更好。①乙醚沸点低于乙醇,原因是
②用乙醚提取效果更好,原因是
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。比较青蒿素分子中
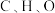 的原子核附近电子云密度大小:
的原子核附近电子云密度大小:②图中晶胞的棱长分别为
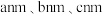 ,晶体的密度为
,晶体的密度为 。(用
。(用 表示阿伏加德罗常数;
表示阿伏加德罗常数; ;青蒿素的相对分子质量为282)
;青蒿素的相对分子质量为282)③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效:一定条件下,用
 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。
①双氢青蒿素分子中碳原子的杂化方式为
②
 的空间结构为
的空间结构为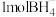 中有
中有 配位键。
配位键。③比较水溶性:双氢青蒿素
 ”)青蒿素。
”)青蒿素。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】葡萄糖酸亚铁 易溶于水、几乎不溶于乙醇,是常用的补铁剂,一种制备流程如下:
易溶于水、几乎不溶于乙醇,是常用的补铁剂,一种制备流程如下:

已知: 溶液呈酸性,
溶液呈酸性, 溶液呈碱性。
溶液呈碱性。
回答下列问题:
(1)葡萄糖酸的结构简式为______ 。
(2)反应Ⅰ制备 ,用如图所示实验装置完成。为避免产生
,用如图所示实验装置完成。为避免产生 ,
, 溶液与
溶液与 溶液混合时的加料方式是
溶液混合时的加料方式是______ 。

(3)过滤洗涤中,证明 已洗涤干净的方法是
已洗涤干净的方法是______ .
(4)葡萄糖氧化为葡萄糖酸的一种生产工艺采用HBr催化 氧化法。取一定量葡萄糖,加入蒸馏水至完全溶解,加入少量HBr和稍过量30%
氧化法。取一定量葡萄糖,加入蒸馏水至完全溶解,加入少量HBr和稍过量30% ,充分反应,加热煮沸,将产生的气体用
,充分反应,加热煮沸,将产生的气体用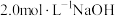 溶液吸收,加入无水乙醇,静置,过滤,干燥,得纯净葡萄糖酸晶体。
溶液吸收,加入无水乙醇,静置,过滤,干燥,得纯净葡萄糖酸晶体。
①完成HBr催化 氧化法的反应方程式。
氧化法的反应方程式。
第一步:______
第二步: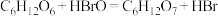
②加热煮沸的作用是______ 。
③加入无水乙醇的作用是______ 。
(5)用酸性 溶液测定葡萄糖酸亚铁晶体中
溶液测定葡萄糖酸亚铁晶体中 含量,进而计算出晶体的纯度,发现纯度总是大于100%。若实验操作和计算均正确,其可能原因是
含量,进而计算出晶体的纯度,发现纯度总是大于100%。若实验操作和计算均正确,其可能原因是______ 。
 易溶于水、几乎不溶于乙醇,是常用的补铁剂,一种制备流程如下:
易溶于水、几乎不溶于乙醇,是常用的补铁剂,一种制备流程如下:
已知:
 溶液呈酸性,
溶液呈酸性, 溶液呈碱性。
溶液呈碱性。回答下列问题:
(1)葡萄糖酸的结构简式为
(2)反应Ⅰ制备
 ,用如图所示实验装置完成。为避免产生
,用如图所示实验装置完成。为避免产生 ,
, 溶液与
溶液与 溶液混合时的加料方式是
溶液混合时的加料方式是
(3)过滤洗涤中,证明
 已洗涤干净的方法是
已洗涤干净的方法是(4)葡萄糖氧化为葡萄糖酸的一种生产工艺采用HBr催化
 氧化法。取一定量葡萄糖,加入蒸馏水至完全溶解,加入少量HBr和稍过量30%
氧化法。取一定量葡萄糖,加入蒸馏水至完全溶解,加入少量HBr和稍过量30% ,充分反应,加热煮沸,将产生的气体用
,充分反应,加热煮沸,将产生的气体用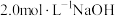 溶液吸收,加入无水乙醇,静置,过滤,干燥,得纯净葡萄糖酸晶体。
溶液吸收,加入无水乙醇,静置,过滤,干燥,得纯净葡萄糖酸晶体。①完成HBr催化
 氧化法的反应方程式。
氧化法的反应方程式。第一步:
第二步:
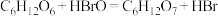
②加热煮沸的作用是
③加入无水乙醇的作用是
(5)用酸性
 溶液测定葡萄糖酸亚铁晶体中
溶液测定葡萄糖酸亚铁晶体中 含量,进而计算出晶体的纯度,发现纯度总是大于100%。若实验操作和计算均正确,其可能原因是
含量,进而计算出晶体的纯度,发现纯度总是大于100%。若实验操作和计算均正确,其可能原因是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】钛和钛合金被认为是21世纪的重要金属材料,广泛用于火箭、飞机制造业等。如图是工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备金属钛的工艺流程。
资料: Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。

(1)钛酸亚铁(FeTiO3)中钛元素的化合价是___________ 。
(2)反应釜中发生的反应是:2FeTiO3 + 7Cl2 + 6C 2X + 2TiCl4 + 6CO,X的化学式是
2X + 2TiCl4 + 6CO,X的化学式是___________ 。
(3)反应釜中得到TiCl4和FeCl3的混合物在沸腾炉中分离,这是利用了TiCl4与FeCl3的___________ 不同。
(4)写出合成器中反应的化学方程式___________ ,该反应___________ (填“是”或“不是”)氧化还原反应。
(5)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属___________ 。由金属钛的性质可知,除去这种杂质可以用___________ 。
(6)依据“绿色低碳”理念,你认为该流程中存在的不足之处是___________ 。
资料: Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。

(1)钛酸亚铁(FeTiO3)中钛元素的化合价是
(2)反应釜中发生的反应是:2FeTiO3 + 7Cl2 + 6C
 2X + 2TiCl4 + 6CO,X的化学式是
2X + 2TiCl4 + 6CO,X的化学式是(3)反应釜中得到TiCl4和FeCl3的混合物在沸腾炉中分离,这是利用了TiCl4与FeCl3的
(4)写出合成器中反应的化学方程式
(5)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属
(6)依据“绿色低碳”理念,你认为该流程中存在的不足之处是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某校课外活动小组为了探究铜与稀硝酸反应产生的气体是NO,设计了如图实验,实验过程中同时用石灰水吸收产生的氮氧化物获得应用广泛的Ca(NO3)2,实验装置如图所示:

(1)实验之前通入N2的目的是___________ 。
(2)在(1)进作后将装置A中铜丝插入稀硝酸,溶液显蓝色,有无色气体生成,其中发生反应的离子方程式是___________ ;该反应体现了硝酸的___________ 性。
(3)装置B中用注射器压入空气之后现象是___________ ;反应的化学方程式是___________ 。
(4)实际工业生产中,制备Ca(NO2)2需控制NO和NO2物质的量之比接近1:1,若n(NO):n(NO2)<1则会导致___________ 。
(5)D装置的作用是___________ 。

(1)实验之前通入N2的目的是
(2)在(1)进作后将装置A中铜丝插入稀硝酸,溶液显蓝色,有无色气体生成,其中发生反应的离子方程式是
(3)装置B中用注射器压入空气之后现象是
(4)实际工业生产中,制备Ca(NO2)2需控制NO和NO2物质的量之比接近1:1,若n(NO):n(NO2)<1则会导致
(5)D装置的作用是
您最近一年使用:0次



