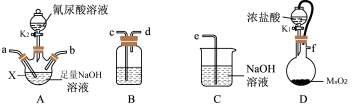
二氯异氰尿酸钠的化学式为C3N3O3Cl2Na(简写为DCCNa,摩尔质量为220g/mol)。常温下DCCNa易溶于水难溶于乙醇。实验室可用氰尿酸(C3H3N3O3)与足量Cl2制备DCCNa:2Cl2+C3H3N3O3+3NaOH=C3N3O3Cl2Na+3H2O+2NaCl,实验装置如图所示(夹持装置和加热装置省略):
回答下列问题:
(1)仪器X的名称为___________ ;装置D发生的离子反应方程式为___________ 。
(2)B中试剂为___________ (填字母标号);
A.饱和NaCl溶液 B.CCl4 C.浓硫酸 D.NaOH溶液
完成上述产品的制备,装置连接的顺序为___________ 。
f→___________→___________→___________→___________→___________(填小写字母)。
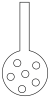
(3)实验员认为可将插入NaOH溶液的导管下端加装多孔的球泡(如图),其目的是______ 。
(4)反应结束后,关闭K1、K2,向X中加入乙醇,静置、减压过滤得粗品;
①乙醇的作用是___________ ;
②减压过滤的优点是___________ ;
③进一步提纯DCCNa的方法是___________ 。
(5)已知实验过程中消耗cmol/L氰尿酸V1mL,最终得到DCCNa的质量为xg,则本次实验的产率为___________ %(用含c、V1、x的代数式表示)。

回答下列问题:
(1)仪器X的名称为
(2)B中试剂为
A.饱和NaCl溶液 B.CCl4 C.浓硫酸 D.NaOH溶液
完成上述产品的制备,装置连接的顺序为
f→___________→___________→___________→___________→___________(填小写字母)。
(3)实验员认为可将插入NaOH溶液的导管下端加装多孔的球泡(如图),其目的是

(4)反应结束后,关闭K1、K2,向X中加入乙醇,静置、减压过滤得粗品;
①乙醇的作用是
②减压过滤的优点是
③进一步提纯DCCNa的方法是
(5)已知实验过程中消耗cmol/L氰尿酸V1mL,最终得到DCCNa的质量为xg,则本次实验的产率为
2023·四川乐山·三模 查看更多[2]
更新时间:2023-05-20 23:43:03
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】氯气广泛应用于杀菌、消毒及化工领域.某化学实验小组设计如图装置制取氯气并探究其性质
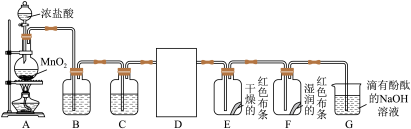
(1)装置A中发生反应的化学方程式为_______
(2)D处收集纯净氯气,观察其物理性质
①推测装置B的作用是_______ ,装置C中的试剂是_______ (填名称)
②D处装置可选用_______ (填序号)
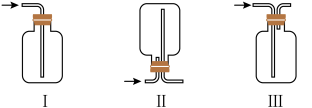
(3)能够证明氯气与水发生反应的现象是_______
(4)装置G中溶液的红色逐渐褪去而得到无色溶液,小组同学认为溶液红色褪去的原因可能有两种,一种是氯气与水反应产生的 具有漂白性,使红色褪去;另一种是
具有漂白性,使红色褪去;另一种是_______ 。请你设计一个简单的实验验证褪色的原因(简述实验步骤)_______
(5)工业上氯气和石灰乳反应可以制取漂白粉,该反应放热会使体系温度升高,导致氯气和石灰乳发生副反应,产生杂质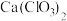 ,该副反应中还原剂与氧化剂的物质的量之比为
,该副反应中还原剂与氧化剂的物质的量之比为_______

(1)装置A中发生反应的化学方程式为
(2)D处收集纯净氯气,观察其物理性质
①推测装置B的作用是
②D处装置可选用

(3)能够证明氯气与水发生反应的现象是
(4)装置G中溶液的红色逐渐褪去而得到无色溶液,小组同学认为溶液红色褪去的原因可能有两种,一种是氯气与水反应产生的
 具有漂白性,使红色褪去;另一种是
具有漂白性,使红色褪去;另一种是(5)工业上氯气和石灰乳反应可以制取漂白粉,该反应放热会使体系温度升高,导致氯气和石灰乳发生副反应,产生杂质
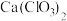 ,该副反应中还原剂与氧化剂的物质的量之比为
,该副反应中还原剂与氧化剂的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】KMnO4是常见的氧化剂,以下是有关KMnO4的制备和应用:
Ⅰ:制备KMnO4
某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应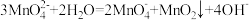 。回答下列问题:
。回答下列问题:
(1)装置A中a的作用是_________ ;装置A中制备Cl2的化学方程式为_________ 。
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是_________ 。
Ⅱ:探究酸性KMnO4与H2C2O4反应速率的影响因素
设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol·L-1H2C2O4溶液、0.010 mol·L-1KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
(3)上述实验①、②是探究_______ 对化学反应速率的影响;若上述实验②、③是探究浓度对化学反应速率的影响,则a为_______ ;
(4)请写出酸性KMnO4与H2C2O4反应的离子方程式_______ 。
(5)若②组紫色褪去时间为10s,计算KMnO4的反应速率______ (保留两位有效数字)。
Ⅲ:氧化还原滴定
(6)KMnO4常作氧化还原滴定的氧化剂,滴定时应将KMnO4溶液加入_______ (填“酸式”或“碱式”)滴定管中;
[测定H2C2O4·xH2O 中结晶水个数x值]
①称取1.260 g纯草酸晶体,将其制成 100.00 mL 水溶液为待测液;
②取25.00mL 待测液放入锥形瓶中,再加入适量稀H2SO4;
③用浓度为0.05 000 mol·L-1的KMnO4标准溶液进行滴定。
标准液消耗数据如图:
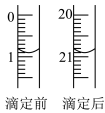
(7)滴定终点的现象_____________ 。
(8)通过上述数据,求得x=______ 。以标准KMnO4溶液滴定样品溶液的浓度,未用标KMnO4溶液润洗滴定管,引起实验结果______ (偏大、偏小或没有影响) 。
Ⅰ:制备KMnO4
某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应
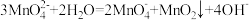 。回答下列问题:
。回答下列问题:(1)装置A中a的作用是
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是
Ⅱ:探究酸性KMnO4与H2C2O4反应速率的影响因素
设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol·L-1H2C2O4溶液、0.010 mol·L-1KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
| 物理量 | V(0.20mol∙L-1H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010mol∙L-1KMnO4溶液)/mL | T/℃ | 时间 |
| ① | 2.0 | 0 | 4.0 | 50 | |
| ② | 2.0 | 0 | 4.0 | 25 | |
| ③ | 1.0 | a | 4.0 | 25 |
(4)请写出酸性KMnO4与H2C2O4反应的离子方程式
(5)若②组紫色褪去时间为10s,计算KMnO4的反应速率
Ⅲ:氧化还原滴定
(6)KMnO4常作氧化还原滴定的氧化剂,滴定时应将KMnO4溶液加入
[测定H2C2O4·xH2O 中结晶水个数x值]
①称取1.260 g纯草酸晶体,将其制成 100.00 mL 水溶液为待测液;
②取25.00mL 待测液放入锥形瓶中,再加入适量稀H2SO4;
③用浓度为0.05 000 mol·L-1的KMnO4标准溶液进行滴定。
标准液消耗数据如图:

(7)滴定终点的现象
(8)通过上述数据,求得x=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】乙苯是主要的有机化工产品。某课题组拟制备乙苯,其反应原理为: +CH3CH2Br
+CH3CH2Br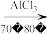
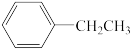 +HBr。
+HBr。
I.制备无水AlCl3(AlCl3易升华,冷却易结块,易潮解)
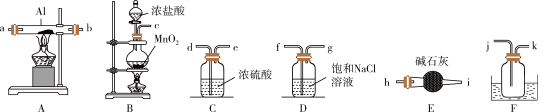
(1)B中烧瓶内反应的离子方程式为_______ 。
(2)导管接口顺序为c→_______ →ab→jk→________ ,E的作用是_______ 。
(3)装置F存在安全隐患,改进措施可以是_______ 。
II.制备乙苯
步骤1:连接装置并检查气密性(如图所示,夹持装置省略)。
步骤2:用酒精灯微热三颈烧瓶。
步骤3:向三项烧瓶中加入25.00mL苯(过量)和12.0g无水AlCl3,在搅拌下滴加15.00mL溴乙烷,70~80℃下加热45min。
步骤4:提纯产品。
(4)本实验宜采用的加热方式为___________ ,为了证明三颈烧瓶中已发生了上述反应,烧杯中的“X溶液”可以是________ 。
A.AgNO3溶液 B.石蕊试液 C.品红溶液 D.NaOH溶液
(5)提纯产品的步骤有:①用大量水洗;②用稀盐酸洗除;③少量蒸馏水水洗;④加入大量无水氯化钙;⑤_______ ;⑥_______ ,并收集136.2℃时的产品。(填操作名称)
(6)实验中收集到10.00mL乙苯,则乙苯的产率为_______ 。(保留一位小数)
 +CH3CH2Br
+CH3CH2Br
 +HBr。
+HBr。I.制备无水AlCl3(AlCl3易升华,冷却易结块,易潮解)

(1)B中烧瓶内反应的离子方程式为
(2)导管接口顺序为c→
(3)装置F存在安全隐患,改进措施可以是
II.制备乙苯
| 名称 | 相对分子质量 | 沸点/℃ | 密度/(g•mL-1) | 实验装置 |
| 苯 | 78 | 80.1 | 0.88 |  |
| 溴乙烷 | 109 | 38.4 | 1.46 | |
| 乙苯 | 106 | 136.2 | 0.87 |
步骤2:用酒精灯微热三颈烧瓶。
步骤3:向三项烧瓶中加入25.00mL苯(过量)和12.0g无水AlCl3,在搅拌下滴加15.00mL溴乙烷,70~80℃下加热45min。
步骤4:提纯产品。
(4)本实验宜采用的加热方式为
A.AgNO3溶液 B.石蕊试液 C.品红溶液 D.NaOH溶液
(5)提纯产品的步骤有:①用大量水洗;②用稀盐酸洗除;③少量蒸馏水水洗;④加入大量无水氯化钙;⑤
(6)实验中收集到10.00mL乙苯,则乙苯的产率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发黏、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
(1)制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生在SCl2。____________ ,装置F中试剂的作用是____________ 。
②装置连接顺序:A→________ →________ →________ →E→D。
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是____________ 。
④为了提高S2Cl2的纯度,实验的关键是控制好温度和____________ 。
(2)少量S2Cl2泄漏时应喷水减慢其挥发(或扩散),并产生酸性悬浊液,但不要对泄漏物或泄漏点直接喷水,其原因是____________ 。
(3)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中SO2的体积分数。____________ (填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为____________ (用含V、m的式子表示)。
| 物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
| 剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
| 化学性质 | ①300℃以上完全分解 ②S2Cl2+Cl2 ④受热或遇水分解放热,放出腐蚀性烟气 | ||||
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生在SCl2。
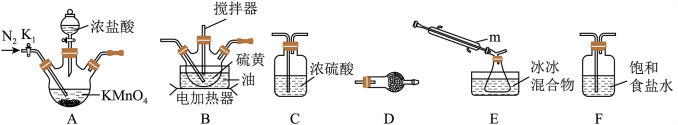
②装置连接顺序:A→
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是
④为了提高S2Cl2的纯度,实验的关键是控制好温度和
(2)少量S2Cl2泄漏时应喷水减慢其挥发(或扩散),并产生酸性悬浊液,但不要对泄漏物或泄漏点直接喷水,其原因是
(3)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中SO2的体积分数。
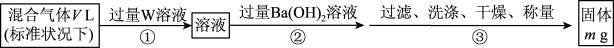
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】“摩尔盐”[ (NH4)2Fe(SO4)2·6H2O ] 是分析化学中的重要试剂。查阅文献得知:“摩尔盐”隔绝空气加热至500℃时可完全分解,但产物复杂。某学习小组欲探究其分解产物。
Ⅰ.【提出猜想】摩尔盐受热分解,小组同学认为分解产物可能有以下几种情况:
a.Fe2O3、SO3、NH3、H2O b.FeO、NH3、SO3、H2O
c.FeO、SO2、NH3、H2O d.Fe2O3、NH3、SO2、SO3、H2O
经认真分析,通过推理即可确定,猜想__________ 不成立(填序号)。
Ⅱ.【实验探究】为检验分解产物,甲同学设计了如下实验装置。
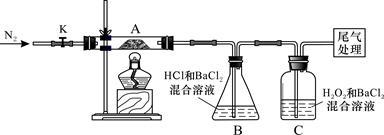
请回答下列问题:
(1)B装置的容器名称是__________ 。
(2)取一定量“摩尔盐”置于加热管A中,加热至分解完后打开K,再通入N2,目的是______ 。
(3)观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀。C中发生反应的离子方程式为_________________________ 。
(4)待A中剩余固体冷却至室温后,取少量置于试管中,加入稀硫酸溶解,再滴几滴KSCN溶液,可以观察到的现象是_______________ 。
(5)乙同学设计实验验证A中残留物不含FeO,操作方法及实验现象是:取少量A中残留物放入试管中,_________________ 。
Ⅲ.【实验反思】
乙同学认为:装置B中产生白色沉淀不能证明分解产物中一定含SO3,原因是_______ 。
Ⅰ.【提出猜想】摩尔盐受热分解,小组同学认为分解产物可能有以下几种情况:
a.Fe2O3、SO3、NH3、H2O b.FeO、NH3、SO3、H2O
c.FeO、SO2、NH3、H2O d.Fe2O3、NH3、SO2、SO3、H2O
经认真分析,通过推理即可确定,猜想
Ⅱ.【实验探究】为检验分解产物,甲同学设计了如下实验装置。

请回答下列问题:
(1)B装置的容器名称是
(2)取一定量“摩尔盐”置于加热管A中,加热至分解完后打开K,再通入N2,目的是
(3)观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀。C中发生反应的离子方程式为
(4)待A中剩余固体冷却至室温后,取少量置于试管中,加入稀硫酸溶解,再滴几滴KSCN溶液,可以观察到的现象是
(5)乙同学设计实验验证A中残留物不含FeO,操作方法及实验现象是:取少量A中残留物放入试管中,
Ⅲ.【实验反思】
乙同学认为:装置B中产生白色沉淀不能证明分解产物中一定含SO3,原因是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】工业上常利用含硫废水生产 ,实验室可用如下装置(略去部分加持仪器)模拟生成过程。
,实验室可用如下装置(略去部分加持仪器)模拟生成过程。
 (
( );
);
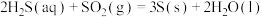 (
( );
);
 (
( )。
)。
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若___________ ,则整个装置气密性良好。装置D的作用是___________ 。装置E中为___________ 溶液。
(2)为提高产品纯度,应使烧瓶C中 和
和 恰好完全反应,则烧瓶C中
恰好完全反应,则烧瓶C中 和
和 物质的量之比为
物质的量之比为___________ 。
(3)装置B的作用之一是观察 的生成速率,其中的液体最好选择
的生成速率,其中的液体最好选择___________ 。
a.蒸馏水 b.饱和 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和
溶液 d.饱和 溶液
溶液
实验中,为使 缓慢进入烧瓶C,采用的操作是
缓慢进入烧瓶C,采用的操作是___________ 。
(4)已知反应( )相对较慢,则烧瓶C中反应达到终点的现象是
)相对较慢,则烧瓶C中反应达到终点的现象是___________ 。
(5)反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有___________ 。
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(6) 还原性较强,在溶液中易被
还原性较强,在溶液中易被 氧化成
氧化成 ,常用作脱氯剂,该反应的离子方程式为:
,常用作脱氯剂,该反应的离子方程式为:___________ 。
 ,实验室可用如下装置(略去部分加持仪器)模拟生成过程。
,实验室可用如下装置(略去部分加持仪器)模拟生成过程。
 (
( );
);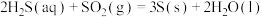 (
( );
); (
( )。
)。(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若
(2)为提高产品纯度,应使烧瓶C中
 和
和 恰好完全反应,则烧瓶C中
恰好完全反应,则烧瓶C中 和
和 物质的量之比为
物质的量之比为(3)装置B的作用之一是观察
 的生成速率,其中的液体最好选择
的生成速率,其中的液体最好选择a.蒸馏水 b.饱和
 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和
溶液 d.饱和 溶液
溶液实验中,为使
 缓慢进入烧瓶C,采用的操作是
缓慢进入烧瓶C,采用的操作是(4)已知反应(
 )相对较慢,则烧瓶C中反应达到终点的现象是
)相对较慢,则烧瓶C中反应达到终点的现象是(5)反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(6)
 还原性较强,在溶液中易被
还原性较强,在溶液中易被 氧化成
氧化成 ,常用作脱氯剂,该反应的离子方程式为:
,常用作脱氯剂,该反应的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】钼催化剂常用于合成氨工业,以废钼催化剂(主要含有MoS2和Al2O3)为原料制备钼酸钠晶体和硫酸钠晶体的一种工艺流程如下图所示。回答下列问题:_____ (写一条即可),“焙烧”反应中氧化剂与还原剂物质的量之比为_____ 。
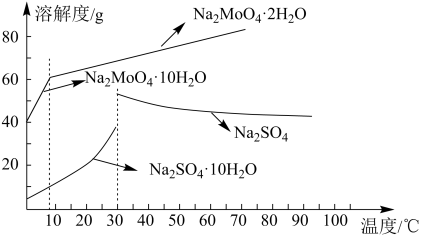
(2)“水溶”时,钼浸取率与浸取时间、浸取温度的关系如下图所示,综合考虑成本等因素,则最佳浸取时间和浸取温度为____ 。_____ ,调节pH不能过低的原因是______ 。
(4)“操作I”的名称为_______ ;“溶液1”中含有大量Na2SO4和少量Na2MoO4,根据下图分析“结晶”过程的操作为______ (填标号)。
B.蒸发水分至有大量晶体析出时,趁热过滤
C.蒸发浓缩,冷却至10℃左右
(5)碱性条件下,将废钼催化剂加入NaClO溶液中,也可制备钼酸钠,同时生成硫酸盐,该反应的离子方程式为______ 。

(2)“水溶”时,钼浸取率与浸取时间、浸取温度的关系如下图所示,综合考虑成本等因素,则最佳浸取时间和浸取温度为

(4)“操作I”的名称为
B.蒸发水分至有大量晶体析出时,趁热过滤
C.蒸发浓缩,冷却至10℃左右
(5)碱性条件下,将废钼催化剂加入NaClO溶液中,也可制备钼酸钠,同时生成硫酸盐,该反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】硫代硫酸钠晶体(Na2S2O3·5H2O,M=248 g·mol-1)是重要的化工原料,易溶于水,不溶于乙醇,具有较强的还原性和配位能力,在中性或碱性环境中稳定。某兴趣小组用如图装置制备 。
。
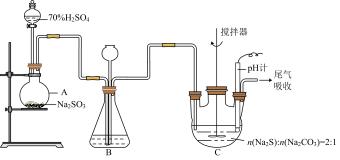
I.制备Na2S2O3•5H2O
合成反应: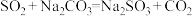 ;
; ;
; 。
。
实验步骤:装置A制备的 通入装置C中的混合溶液,加热、搅拌,至溶液
通入装置C中的混合溶液,加热、搅拌,至溶液 约为7时,停止通入
约为7时,停止通入 气体,得产品混合溶液,经过分离提纯得到
气体,得产品混合溶液,经过分离提纯得到 产品。
产品。
(1)仪器A的名称是_______ ,仪器B中长颈漏斗的作用是_______ ,另外可以通过装置B观察SO2的生成速率,其中的液体可以选择_______
a.浓H2SO4 b.饱和Na2SO3溶液 c.饱和NaCl溶液 d.饱和NaHSO3溶液
(2)装置C中的反应混合溶液pH过低将导致产率降低,原因是(离子方程式表示)_______
(3)产品混合溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到Na2S2O3·5H2O产品。下列说法正确的是_______。
II.测定产品纯度:准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L-1碘的标准溶液滴定。 反应原理为:2S2O +I2=S4O
+I2=S4O +2I-
+2I-
(4)滴定至终点时,滴定终点的现象是_______ 。
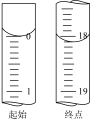
(5)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为_______ mL。若滴定终点时仰视凹液面,则测定产品的纯度结果_______ 。(填“偏高”、“偏低”、或“无影响”)
III.Na2S2O3的应用
(6)Na2S2O3溶液常用作定影剂,溶去胶片上未感光的AgBr,生成配位数为2的配离子,请写出该反应的离子方程式_______ 。
 。
。
I.制备Na2S2O3•5H2O
合成反应:
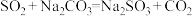 ;
; ;
; 。
。实验步骤:装置A制备的
 通入装置C中的混合溶液,加热、搅拌,至溶液
通入装置C中的混合溶液,加热、搅拌,至溶液 约为7时,停止通入
约为7时,停止通入 气体,得产品混合溶液,经过分离提纯得到
气体,得产品混合溶液,经过分离提纯得到 产品。
产品。(1)仪器A的名称是
a.浓H2SO4 b.饱和Na2SO3溶液 c.饱和NaCl溶液 d.饱和NaHSO3溶液
(2)装置C中的反应混合溶液pH过低将导致产率降低,原因是(离子方程式表示)
(3)产品混合溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到Na2S2O3·5H2O产品。下列说法正确的是_______。
| A.蒸发浓缩至有大量晶体析出时,停止加热,用预热蒸干 |
| B.快速蒸发溶液中水分,可得较大晶体颗粒 |
| C.冷却结晶后的固液混合物中加入乙醇可提高产率 |
| D.可选用冷的Na2SO3溶液作洗涤剂 |
II.测定产品纯度:准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L-1碘的标准溶液滴定。 反应原理为:2S2O
 +I2=S4O
+I2=S4O +2I-
+2I-(4)滴定至终点时,滴定终点的现象是
(5)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为

III.Na2S2O3的应用
(6)Na2S2O3溶液常用作定影剂,溶去胶片上未感光的AgBr,生成配位数为2的配离子,请写出该反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】新冠肺炎疫情期间,多种含氯消毒剂如84消毒液、Cl2、NaClO2等对病毒均具有很好的消杀作用,其中亚氯酸钠(NaClO2)在工业上常以ClO2气体为原料制备,实验室制备亚氯酸钠的装置如图所示(夹持装置已略)。

已知:①控制电压电解饱和食盐水可得到ClO2;
②Cl2易溶于CCl4;
③亚氯酸钠在不同温度下的溶解度如下表所示:
回答下列问题:
(1)装置甲中产生ClO2的电极反应式为_____________________ 。
(2)装置乙中CCl4的作用为________________________________ 。
(3)装置丙中生成NaClO2的化学方程式为____________________________ 。
(4)从装置丙反应后的溶液中获得NaClO2晶体的步骤如下:

其中步骤①加热到_________________ (填现象)时停止加热,步骤②是__________________ 。
(5)准确称取2.26gNaClO2粗品,加入盛有20.00mL刚煮沸并冷却过的水、足量10%的稀硫酸和30.00mL质量分数为40%的KI溶液(足量)的碘量瓶中,立即密封并摇晃碘量瓶至试样完全反应,再加入淀粉作指示剂用浓度为3.00mol/L的Na2S2O3溶液滴定(已知整个过程中发生的反应依次为 +4I-+4H+=2I2+Cl-+2H2O,
+4I-+4H+=2I2+Cl-+2H2O, ),
),
①若三次平行实验测得消耗的Na2S2O3溶液的平均体积为30.00mL,则粗品的纯度为_________________ %(保留三位有效数字),
②若使用的水未煮沸,则测定结果会___________________ (填“偏高”“偏低”或“无影响”)。

已知:①控制电压电解饱和食盐水可得到ClO2;
②Cl2易溶于CCl4;
③亚氯酸钠在不同温度下的溶解度如下表所示:
| 温度℃ | 20 | 40 | 60 |
| 溶解度/g | 6.2 | 23.4 | 48.3 |
回答下列问题:
(1)装置甲中产生ClO2的电极反应式为
(2)装置乙中CCl4的作用为
(3)装置丙中生成NaClO2的化学方程式为
(4)从装置丙反应后的溶液中获得NaClO2晶体的步骤如下:

其中步骤①加热到
(5)准确称取2.26gNaClO2粗品,加入盛有20.00mL刚煮沸并冷却过的水、足量10%的稀硫酸和30.00mL质量分数为40%的KI溶液(足量)的碘量瓶中,立即密封并摇晃碘量瓶至试样完全反应,再加入淀粉作指示剂用浓度为3.00mol/L的Na2S2O3溶液滴定(已知整个过程中发生的反应依次为
 +4I-+4H+=2I2+Cl-+2H2O,
+4I-+4H+=2I2+Cl-+2H2O, ),
),①若三次平行实验测得消耗的Na2S2O3溶液的平均体积为30.00mL,则粗品的纯度为
②若使用的水未煮沸,则测定结果会
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】I.一氯甲烷(CH3C1)是一种重要的化工原料,常温下它是无色有毒气体,微溶于水,易溶于乙醇、CCl4等.某同学在实验室用下图所示装置模拟催化法制备和收集一氯甲烷.

(1)无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为__________________________
(2)装置B的主要作用是____________________
(3)收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的V1mL、c1mol•L﹣1NaOH溶液充分吸收,以甲基橙作指示剂,用c2 mol•L﹣1盐酸标准液对吸收液进行返滴定(发生的反应为:NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+2CO2↑+2H2O),最终消耗V2mL盐酸.则所收集CH3Cl的物质的量为_______ mol.
(已知:2CH3Cl+3O2 2CO2+2H2O+2HCl)
2CO2+2H2O+2HCl)
II. 锂/磷酸氧铜电池是一种以磷酸氧铜作为正极材料的锂离子电池,其正极的活性物质是Cu4O(PO4)2,制备流程如下:

主要反应原理:2Na3PO4+4CuSO4+2NH3·H2O==Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)实验室进行“过滤”操作使用的玻璃仪器除烧杯外主要有____________________________________ 。
(2)流程中“洗涤Ⅰ”后,检验沉淀已洗涤干净的方法是________________________________________ 。

(1)无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为
(2)装置B的主要作用是
(3)收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的V1mL、c1mol•L﹣1NaOH溶液充分吸收,以甲基橙作指示剂,用c2 mol•L﹣1盐酸标准液对吸收液进行返滴定(发生的反应为:NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+2CO2↑+2H2O),最终消耗V2mL盐酸.则所收集CH3Cl的物质的量为
(已知:2CH3Cl+3O2
 2CO2+2H2O+2HCl)
2CO2+2H2O+2HCl)II. 锂/磷酸氧铜电池是一种以磷酸氧铜作为正极材料的锂离子电池,其正极的活性物质是Cu4O(PO4)2,制备流程如下:

主要反应原理:2Na3PO4+4CuSO4+2NH3·H2O==Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)实验室进行“过滤”操作使用的玻璃仪器除烧杯外主要有
(2)流程中“洗涤Ⅰ”后,检验沉淀已洗涤干净的方法是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
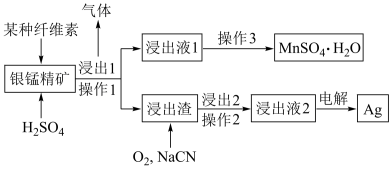
【推荐2】某有色金属研究室对从银锰精矿中提取单质银的方法进行改良创新,从而更高效地实现锰和银的分离。其简易流程如下图。已知:银锰精矿主要成分为MnO2和银单质。
(1)操作1与操作2所对应的分离方法是__________________ 。
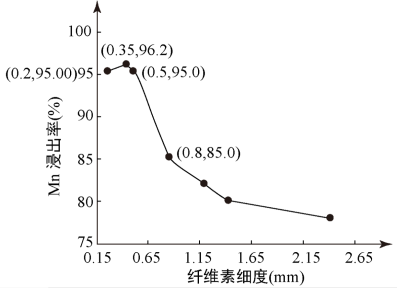
(2)通过对“浸出1”步骤中纤维细度的控制,绘制出一定时间内纤维素-Mn浸出率图象如上图所示,实际生产中应控制细度________ mm较为合适,理由是_________ 。
(3)在“浸出1”步骤中,纤维素会先水解为单糖,请写出该单糖(用分子式表达)与银锰精矿反应的离子方程式:_______________________ 。
(4)浸出液2的主要成分为[Ag(CN)2]-,使用情性电极电解浸出液2,请写出阴极的电极方程式:________ 。本流程中可循环使用的物质为_________________ 。
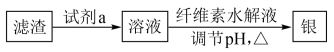
(5)通过上述流程,浸出液1中通常还含有少量银离子,充分提取银,可对MnSO4·H2O晶体进行洗涤,请简述洗涤的方法_____________________________ 。将洗涤液与母液合并,加入盐酸,过滤后再经过以下步骤可回收大部分浸出液1中的银。试剂a是______________ 。
(1)操作1与操作2所对应的分离方法是
(2)通过对“浸出1”步骤中纤维细度的控制,绘制出一定时间内纤维素-Mn浸出率图象如上图所示,实际生产中应控制细度
(3)在“浸出1”步骤中,纤维素会先水解为单糖,请写出该单糖(用分子式表达)与银锰精矿反应的离子方程式:
(4)浸出液2的主要成分为[Ag(CN)2]-,使用情性电极电解浸出液2,请写出阴极的电极方程式:
(5)通过上述流程,浸出液1中通常还含有少量银离子,充分提取银,可对MnSO4·H2O晶体进行洗涤,请简述洗涤的方法
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】对硝基苯甲酸(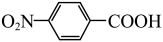 )是一种广泛用于医药、染料、感光材料等的重要精细化工中间体。工业上以对硝基甲苯(
)是一种广泛用于医药、染料、感光材料等的重要精细化工中间体。工业上以对硝基甲苯(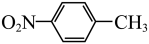 )、Cr(SO)3等物质为主要原料,通过间接电合成法制备对硝基苯甲酸,生产工艺流程如下:
)、Cr(SO)3等物质为主要原料,通过间接电合成法制备对硝基苯甲酸,生产工艺流程如下:
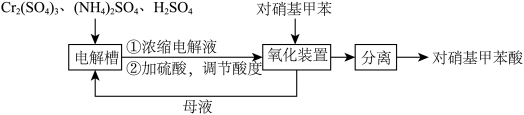
已知:①对硝基甲苯:黄色晶体,熔点为51.7℃,沸点为238.5℃,不溶于水,易溶于乙醇、乙醚、氯仿和苯。②对硝基苯甲酸:黄色晶体,熔点为242℃,沸点为359℃,微溶于水,溶于乙醇,能升华。
回答下列问题:
(1)电解制备Cr2O72-:用H型隔膜电解槽电解制备Cr2O72-,装置如下图1所示。外接电源的负极为__ (填“A”或“B”),反应II的离子方程式为_______ 。
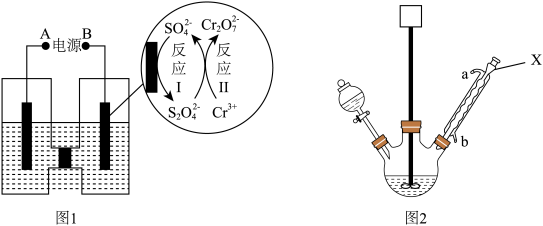
(2)氧化制备对硝基苯甲酸:用上图2所示装置制备对硝基苯甲酸,具体过程如下:
步骤1:向250 mL三颈烧瓶中依次加入一定量含Cr2O72-的电解液、对硝基甲苯,搅拌、水浴升温到设定温度,恒温下进行反应,直至反应液由棕红色变为墨绿色时为止。
步骤2:待反应混合物冷却至室温后,与适量冰水充分混合,抽滤。滤液返回电解槽中重新电解。
步骤3:把步骤2中抽滤所得固体溶于5%的热NaOH溶液中(约60℃),待温度降到50℃时,抽滤,向滤液中加入过量2 mol/L H2SO4,析出黄色沉淀,再抽滤,并用冷水洗涤,然后在低于80℃的条件下烘干,可得粗产品。
①仪器X的名称是_____ ,冷却水应从___ 口进入(填“a”或“b”)。
②步骤2中,抽滤所得固体的主要成分是_____ 。
③步骤3中,用NaOH溶液处理后,需待温度降到50℃时进行抽滤的原因是______ 。
④制得的粗产品需要进一步纯化,根据对硝基苯甲酸的有关性质可知,对其进行纯化还可以采用_____ 法完成。
⑤该合成技术的优点是实现了____ (填化学式)的循环利用,绿色环保。
(3)测定对硝基苯甲酸的纯度:称取1.670 g粗产品,配成100 mL溶液,取25.00 mL溶液,用0.1000 mol·L-1 KOH溶液滴定,重复滴定四次,每次消耗KOH溶液的体积如下表所示。已知:对硝基苯甲酸的摩尔质量为167.0 g·mol-1,则对硝基苯甲酸的纯度为_____ 。
 )是一种广泛用于医药、染料、感光材料等的重要精细化工中间体。工业上以对硝基甲苯(
)是一种广泛用于医药、染料、感光材料等的重要精细化工中间体。工业上以对硝基甲苯( )、Cr(SO)3等物质为主要原料,通过间接电合成法制备对硝基苯甲酸,生产工艺流程如下:
)、Cr(SO)3等物质为主要原料,通过间接电合成法制备对硝基苯甲酸,生产工艺流程如下:
已知:①对硝基甲苯:黄色晶体,熔点为51.7℃,沸点为238.5℃,不溶于水,易溶于乙醇、乙醚、氯仿和苯。②对硝基苯甲酸:黄色晶体,熔点为242℃,沸点为359℃,微溶于水,溶于乙醇,能升华。
回答下列问题:
(1)电解制备Cr2O72-:用H型隔膜电解槽电解制备Cr2O72-,装置如下图1所示。外接电源的负极为

(2)氧化制备对硝基苯甲酸:用上图2所示装置制备对硝基苯甲酸,具体过程如下:
步骤1:向250 mL三颈烧瓶中依次加入一定量含Cr2O72-的电解液、对硝基甲苯,搅拌、水浴升温到设定温度,恒温下进行反应,直至反应液由棕红色变为墨绿色时为止。
步骤2:待反应混合物冷却至室温后,与适量冰水充分混合,抽滤。滤液返回电解槽中重新电解。
步骤3:把步骤2中抽滤所得固体溶于5%的热NaOH溶液中(约60℃),待温度降到50℃时,抽滤,向滤液中加入过量2 mol/L H2SO4,析出黄色沉淀,再抽滤,并用冷水洗涤,然后在低于80℃的条件下烘干,可得粗产品。
①仪器X的名称是
②步骤2中,抽滤所得固体的主要成分是
③步骤3中,用NaOH溶液处理后,需待温度降到50℃时进行抽滤的原因是
④制得的粗产品需要进一步纯化,根据对硝基苯甲酸的有关性质可知,对其进行纯化还可以采用
⑤该合成技术的优点是实现了
(3)测定对硝基苯甲酸的纯度:称取1.670 g粗产品,配成100 mL溶液,取25.00 mL溶液,用0.1000 mol·L-1 KOH溶液滴定,重复滴定四次,每次消耗KOH溶液的体积如下表所示。已知:对硝基苯甲酸的摩尔质量为167.0 g·mol-1,则对硝基苯甲酸的纯度为
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积( mL) | 23.00 | 23.10 | 21.40 | 22.90 |
您最近一年使用:0次

 2SCl2
2SCl2 

