 既是大气主要污染物之一,又在生产生活中具有广泛应用,如可生产
既是大气主要污染物之一,又在生产生活中具有广泛应用,如可生产 并进而制得硫酸等,其反应原理为:
并进而制得硫酸等,其反应原理为: 。对于反应
。对于反应 ,下列说法正确的是
,下列说法正确的是| A.该反应在任何条件下都能自发进行 |
B.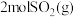 和 和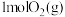 所含键能总和比 所含键能总和比 所含键能小 所含键能小 |
C.反应达平衡后再通入 的体积分数一定增加 的体积分数一定增加 |
D.反应在高压、催化剂条件下进行可提高 的平衡转化率 的平衡转化率 |
22-23高三下·江苏南通·阶段练习 查看更多[2]
更新时间:2023-05-05 00:06:10
|
相似题推荐
【推荐1】对于反应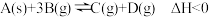 ,下列说法正确的是
,下列说法正确的是
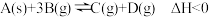 ,下列说法正确的是
,下列说法正确的是| A.加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B.该反应△S>0,△H<0,在任何条件下能自发进行 |
| C.恒温恒容条件下,混合气体密度不变达到化学平衡状态 |
| D.达到平衡状态后,若增加A的量,平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在合成氨时,要使氨的产率增大,又要使化学反应速率增大,可以采取的措施有
①增大体积使压强减小②减小体积使压强增大③升高温度④降低温度
⑤恒温恒容,再充入等量的 和
和 ⑥恒温恒压,再充入等量的
⑥恒温恒压,再充入等量的 和
和
⑦液化分离 ⑧使用正催化剂
⑧使用正催化剂
①增大体积使压强减小②减小体积使压强增大③升高温度④降低温度
⑤恒温恒容,再充入等量的
 和
和 ⑥恒温恒压,再充入等量的
⑥恒温恒压,再充入等量的 和
和
⑦液化分离
 ⑧使用正催化剂
⑧使用正催化剂| A.②④⑤⑦ | B.②③④⑤⑦⑧ | C.②⑤ | D.②③⑤⑧ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.已知H2(g)+S(g)=H2S(g) ∆H1<0,H2(g)+S(s)=H2S(g) ∆H2<0,则∆H1<∆H2 |
| B.中和热的测定实验中,氢氧化钠分批加入,反应更充分,测定的中和热数值误差更小 |
| C.已知:CH4的燃烧热为890.3kJ/mol,则101kPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H=-890.3kJ/mol |
D.500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,则其热化学方程式为N2(g)+3H2(g) 2NH3(g) ΔH=-38.6kJ/mol 2NH3(g) ΔH=-38.6kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.69 g NO2和N2O4的混合气体中所含原子数小于4.5NA |
| B.100 g38%的过氧乙酸的水溶液中氧原子数目为1.5NA |
| C.等物质的量的Na3N和NaN3中含有阴离子数为NA |
| D.1mol SO2与0.5mol O2在密闭容器中充分反应后的分子数大于NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列生产或实验事实引出的相应结论不 正确的是
| 选项 | 事实 | 结论 |
| A | 向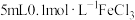 溶液中加入 溶液中加入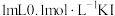 溶液,充分振荡,完全反应后,滴加 溶液,充分振荡,完全反应后,滴加 溶液,出现血红色 溶液,出现血红色 |  是可逆反应 是可逆反应 |
| B | 工业制硫酸时,在 的吸收阶段,吸收塔里要装填瓷环 的吸收阶段,吸收塔里要装填瓷环 | 增大气液接触面积,使 的吸收速率增大 的吸收速率增大 |
| C | 其他条件相同, 溶液和 溶液和 溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
| D | A、B两支试管中分别加入等体积 的 的 溶液,在B试管中加入2~3滴 溶液,在B试管中加入2~3滴 溶液,B试管中产生气泡块 溶液,B试管中产生气泡块 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一定温度下,可逆反应: 在某密闭容器中达到平衡,下列说法不正确的是
在某密闭容器中达到平衡,下列说法不正确的是
 在某密闭容器中达到平衡,下列说法不正确的是
在某密闭容器中达到平衡,下列说法不正确的是A. |
B.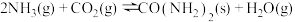 ,反应达到平衡,升高温度,有利于平衡逆移 ,反应达到平衡,升高温度,有利于平衡逆移 |
C.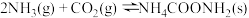 ,若在恒温下压缩容器体积,氨基甲酸铵固体的质量增大 ,若在恒温下压缩容器体积,氨基甲酸铵固体的质量增大 |
D.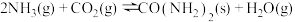 ,在密闭容器中达到平衡,混合气体的平均相对分子质量不变,则反应一定达到平衡 ,在密闭容器中达到平衡,混合气体的平均相对分子质量不变,则反应一定达到平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定温度下,将足量的 固体置于盛有1mol
固体置于盛有1mol 的恒容密闭容器中,发生反应
的恒容密闭容器中,发生反应 (不考虑
(不考虑 转化为
转化为 ,下列不能判断该反应达到平衡状态的是
,下列不能判断该反应达到平衡状态的是
 固体置于盛有1mol
固体置于盛有1mol 的恒容密闭容器中,发生反应
的恒容密闭容器中,发生反应 (不考虑
(不考虑 转化为
转化为 ,下列不能判断该反应达到平衡状态的是
,下列不能判断该反应达到平衡状态的是| A.气体的颜色不再改变 | B.有amol 生成,同时有4amol 生成,同时有4amol 生成 生成 |
| C.气体的平均相对分子质量不再变化 | D.固体混合物中铜元素的质量分数不再变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于自发过程的叙述正确的是
| A.只有不需要任何条件就能够自动进行的过程才是自发过程 |
| B.需要加热才能进行的过程肯定不是自发过程 |
| C.能自发进行的反应一定是放热反应 |
| D.焓变小于零而熵变大于零的反应肯定是自发的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】哈伯法合成氨技术是德国诺贝尔化学奖获得者哈伯发明的。其合成原理为:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H<0,
H<0, S<0。下列有关工业合成氨的说法正确的是
S<0。下列有关工业合成氨的说法正确的是
 2NH3(g)
2NH3(g)  H<0,
H<0, S<0。下列有关工业合成氨的说法正确的是
S<0。下列有关工业合成氨的说法正确的是A.因为 H<0,所以该反应一定能自发进行 H<0,所以该反应一定能自发进行 |
B.因为 S<0,所以该反应一定不能自发进行 S<0,所以该反应一定不能自发进行 |
| C.在低温下进行是为了提高反应物的转化率 |
| D.使用催化剂加快反应速率是因为催化剂降低了反应的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法正确的是
| A.常温下2S2O(g)=3S(s)+SO2(g)能自发进行,则该反应△H<0 |
| B.一定温度下,饱和Ca(OH)2溶液中加入少量的生石灰,所得液的pH会增大 |
| C. CaSO4悬浊液中滴加少量Na2CO3溶液可生成CaCO3,则Ksp(CaCO3) > Ksp(CaSO4) |
| D.用惰性电极电解1L1mol•L的CuSO4溶液,当阴极析出3.2g铜时,加0.05molCu(OH)2固体可将溶液恢复至原浓度 |
您最近一年使用:0次

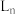 表示配体
表示配体 ,下列叙述正确的是
,下列叙述正确的是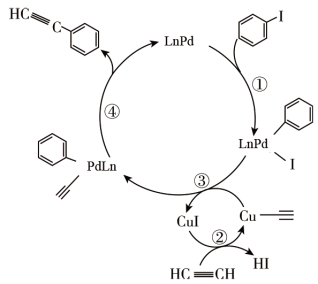
 元素被还原
元素被还原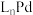 和
和 是该反应过程的催化剂,可以提高
是该反应过程的催化剂,可以提高 的平衡转化率
的平衡转化率 反应,可以合成
反应,可以合成
 2C(g)+D(g)已达平衡状态的是
2C(g)+D(g)已达平衡状态的是 

