相同的温度和压强下,有关下列两个反应的说法不正确的是
注:其中Δn表示反应方程式中气体系数差;
| 反应 | ΔH/kJ•mol-1 | Δn | ΔS/J•K•mol-1 |
| MgCO3(s)=MgO(s)+CO2(g) | 117.6 | 1 | a |
| CaCO3(s)=CaO(s)+CO2(g) | 177.9 | 1 | b |
| A.因为Δn相同,所以a与b大小相近 |
| B.a-b=S[MgO(s)]+S[CaCO3(s)]-S[MgCO3(s)]-S[CaO(s)] |
| C.热分解温度:MgCO3(s)>CaCO3(s) |
| D.两个反应的ΔH和ΔS都大于零 |
更新时间:2023-05-05 00:12:07
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】能源是人类生存和发展的重要支柱,研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义,已知下列热化学方程式
则下列说法正确的是
| ① | H2(g)+ O2(g)= H2O(g) △H =﹣242kJ /mol; O2(g)= H2O(g) △H =﹣242kJ /mol; | |||||||
| ② | 2H2(g)+ O2(g)= 2H2O(l) △H=﹣572kJ/mol; | |||||||
| ③ | C(s)+ O2(g)= CO(g) △H=﹣110.5kJ/moL; O2(g)= CO(g) △H=﹣110.5kJ/moL; | |||||||
| ④ | C(s)+ O2(g)= CO2(g) △H=﹣393.5kJ/moL; | |||||||
| ⑤ | CO2(g)+ 2H2O(g)= CH4(g)+ 2O2(g)△H=" +" 802kJ/moL | |||||||
| 化学键 | O=O | C-C | H-H | O-O | C-O | O-H | C-H | |
| 键能kJ/mol | 497 | 348 | 436 | 142 | 351 | 463 | 414 | |
则下列说法正确的是
A.H2燃烧热的热化学方程式为H2(g)+ O2(g)= H2O(g) △H =﹣242kJ /mol O2(g)= H2O(g) △H =﹣242kJ /mol |
B.热化学方程式:C(s)+ H2O(g) H2(g)+ CO(g) △H =" +" 175.5 kJ/moL H2(g)+ CO(g) △H =" +" 175.5 kJ/moL |
| C.CH4的燃烧热△H ="—" 802 kJ/moL |
| D.估算出C=O键能为800kJ/moL |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列图示与对应的叙述不相符合 的是
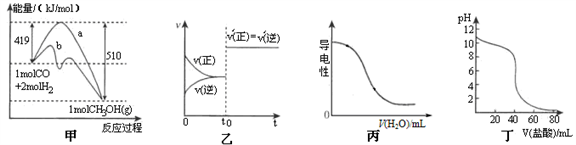
A.图甲表示工业上用CO生产甲醇的反应CO(g)+2H2(g) CH3OH(g)。该反应的△H=-91.kJ·mol-1 CH3OH(g)。该反应的△H=-91.kJ·mol-1 |
| B.图乙表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件可能是加入催化剂 |
| C.图丙表示向0.1 mol·L–1的氨水溶液中逐渐加水时溶液的导电性变化 |
| D.图丁表示盐酸滴加到0.1mol·L-1某碱溶液得到的滴定曲线,用已知浓度盐酸滴定未知浓度该碱时最好选取酚酞作指示剂 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g)+ 5O2(g)→ 3CO2 (g)+ 4H2O(l) △H =-a kJ·mol-1
途径II:C3H8(g) → C3H6(g)+ H2(g) △H = +b kJ·mol-1
2C3H6(g)+ 9O2 (g)→ 6CO2 (g)+ 6H2O(l) △H = -c kJ·mol-1
2H2(g)+ O2 (g)=2H2O(l) △H = -d kJ·mol-1(a、b、c、d均为正值)
则有关a、b、c、d的关系正确的是
途径I:C3H8(g)+ 5O2(g)→ 3CO2 (g)+ 4H2O(l) △H =-a kJ·mol-1
途径II:C3H8(g) → C3H6(g)+ H2(g) △H = +b kJ·mol-1
2C3H6(g)+ 9O2 (g)→ 6CO2 (g)+ 6H2O(l) △H = -c kJ·mol-1
2H2(g)+ O2 (g)=2H2O(l) △H = -d kJ·mol-1(a、b、c、d均为正值)
则有关a、b、c、d的关系正确的是
| A.2b=c+d-2a | B.b=c+d-2a |
| C.2b=c-d-2a | D.b=c+d+2a |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列依据热化学方程式得出的结论正确的是
| A.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| B.已知C(s)+O2(g)=CO2(g) ΔH1 C(s)+1/2O2(g)=CO(g) ΔH2;则ΔH2>ΔH1 |
| C.已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
| D.放热过程(ΔH<0)或熵增加(ΔS> 0)的过程一定是自发的 |
您最近半年使用:0次
单选题
|
较难
(0.4)
真题
解题方法
【推荐2】相同温度和压强下,关于反应的 ,下列判断正确的是
,下列判断正确的是

 ,下列判断正确的是
,下列判断正确的是
A. | B. |
C.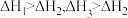 | D.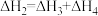 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列各组热化学方程式中,化学反应的△H前者小于后者的有
①C(s)+O2(g)═CO2(g) △H1 C(s)+ O2(g)═CO(g) △H2
O2(g)═CO(g) △H2
②S(s)+O2(g)═SO2(g) △H3 S(g)+O2(g)═SO2(g) △H4
③2H2(g)+O2(g)═2H2O(l) △H5 2H2(g)+O2(g)═2H2O(g) △H6
④CaCO3(s)═CaO(s)+CO2(g) △H7 CaO(s)+H2O(l)═Ca(OH)2(s) △H8
⑤ H2SO4(浓)+NaOH(aq)=
H2SO4(浓)+NaOH(aq)= Na2SO4(aq)+H2O(l) ΔH9CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH10
Na2SO4(aq)+H2O(l) ΔH9CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH10
⑥N2O4(g) 2NO2(g) △H11 2NO2(g)
2NO2(g) △H11 2NO2(g)  N2O4(g) △H12
N2O4(g) △H12
①C(s)+O2(g)═CO2(g) △H1 C(s)+
 O2(g)═CO(g) △H2
O2(g)═CO(g) △H2②S(s)+O2(g)═SO2(g) △H3 S(g)+O2(g)═SO2(g) △H4
③2H2(g)+O2(g)═2H2O(l) △H5 2H2(g)+O2(g)═2H2O(g) △H6
④CaCO3(s)═CaO(s)+CO2(g) △H7 CaO(s)+H2O(l)═Ca(OH)2(s) △H8
⑤
 H2SO4(浓)+NaOH(aq)=
H2SO4(浓)+NaOH(aq)= Na2SO4(aq)+H2O(l) ΔH9CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH10
Na2SO4(aq)+H2O(l) ΔH9CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH10⑥N2O4(g)
 2NO2(g) △H11 2NO2(g)
2NO2(g) △H11 2NO2(g)  N2O4(g) △H12
N2O4(g) △H12| A.2项 | B.3项 | C.4项 | D.5项 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】已知 、
、 、
、 可作为燃料电池的燃料,其相关热化学方程式如下。
可作为燃料电池的燃料,其相关热化学方程式如下。
①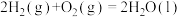
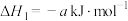
②
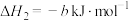
③

④

下列说法正确的是
 、
、 、
、 可作为燃料电池的燃料,其相关热化学方程式如下。
可作为燃料电池的燃料,其相关热化学方程式如下。①
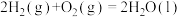
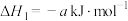
②

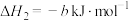
③


④


下列说法正确的是
A.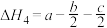 |
B.反应③的 |
C.反应①中若生成 ,则 ,则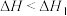 |
D.反应②中的 能表示甲烷的燃烧热 能表示甲烷的燃烧热 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】一定条件下,银催化剂表面上存在反应: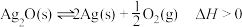 ,起始状态Ⅰ中有
,起始状态Ⅰ中有 、
、 和
和 ,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是

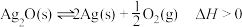 ,起始状态Ⅰ中有
,起始状态Ⅰ中有 、
、 和
和 ,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
A.从Ⅰ到Ⅱ的过程 |
B.反应的平衡压强: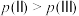 |
C.平衡常数: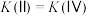 |
D.若体积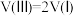 ,则 ,则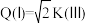 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】将一定量的氨基甲酸铵置于恒容的密闭真空容器中(固体体积忽略不计),使其达到化学平衡:H2NCOONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
下列有关叙述正确的是
 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列有关叙述正确的是
| A.在低温下该反应能自发进行 |
| B.15℃时,该反应的化学平衡常数约为2.0 |
| C.当混合气体平均相对分子质量不变时,该反应达到化学反应限度 |
| D.恒温条件下,向原平衡体系中再充入2molNH3和1molCO2,达平衡后CO2浓度不变 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列说法正确的是
| A.在相同条件下PH=5的CH3COOH溶液和PH=5的NH4Cl溶液中,水的电离程度前者比后者大 |
B.反应NH3(g)+HCl(g)  NH4Cl(s)能自发进行,则该反应ΔH>0 NH4Cl(s)能自发进行,则该反应ΔH>0 |
| C.锌与稀硫酸反应时加入少量硫酸铜,反应加快的主要原因是Cu2+水解增大了c(H+) |
D.一定条件下,反应2SO2(g)+O2(g)  2SO3(g) ΔH<0达到平衡后,升高体系温度,反应重新达到平衡前,有2v正(O2)<v逆(SO3) 2SO3(g) ΔH<0达到平衡后,升高体系温度,反应重新达到平衡前,有2v正(O2)<v逆(SO3) |
您最近半年使用:0次






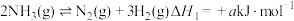
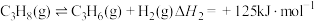
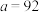
 分解率不变
分解率不变


