一定条件下,银催化剂表面上存在反应: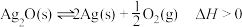 ,起始状态Ⅰ中有
,起始状态Ⅰ中有 、
、 和
和 ,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是

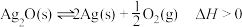 ,起始状态Ⅰ中有
,起始状态Ⅰ中有 、
、 和
和 ,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
A.从Ⅰ到Ⅱ的过程 |
B.反应的平衡压强: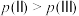 |
C.平衡常数: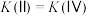 |
D.若体积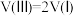 ,则 ,则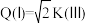 |
更新时间:2024-04-03 09:26:36
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】一定条件下,分别向体积为1L的密闭容器中充入表中所示的①、②、③三组反应气,发生反应:2X(g)+Y(g) Z(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法不正确的是
Z(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法不正确的是
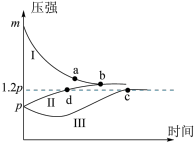
 Z(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法不正确的是
Z(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法不正确的是| 实验 | 充入气体量 | 反应过程条件 |
| ① | 2molX+1molY | 恒温 |
| ② | 1molZ | 恒温 |
| ③ | 1molZ | 绝热 |

| A.曲线I对应实验① | B.正反应为放热反应 |
| C.气体的总物质的量:nc=nd | D.b点平衡常数比c点平衡常数小 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
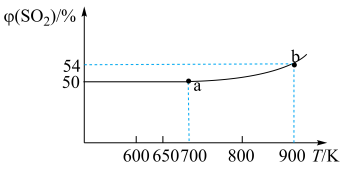
【推荐2】将 晶体置于真空刚性容器中,升温可发生反应:
晶体置于真空刚性容器中,升温可发生反应: 和
和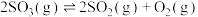 ,该体系达到平衡状态时
,该体系达到平衡状态时 的体积分数
的体积分数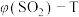 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 晶体置于真空刚性容器中,升温可发生反应:
晶体置于真空刚性容器中,升温可发生反应: 和
和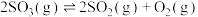 ,该体系达到平衡状态时
,该体系达到平衡状态时 的体积分数
的体积分数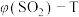 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A.700 K前,只发生反应 |
B.650 K时,若容器内气体压强为 ,则 ,则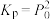 |
C.b点温度下, 分解率为8% 分解率为8% |
| D.在a点容器中加入催化剂,则b点将向上平移 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】利用CO2催化加氢可制乙烯,反应为2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g) △H,在两个容积均为1L恒容密闭容器中,分别加入2molCO2、4molH2,分别选用两种催化剂,反应进行相同时间,测得CO2转化率随反应温度的变化如下图所示。下列说法正确的是
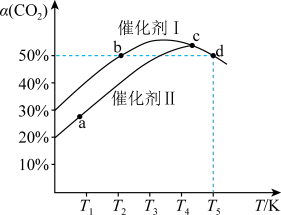

| A.使用催化剂I时反应的活化能低于催化剂II |
| B.△H>0 |
| C.b、d两状态下,化学反应速率相等 |
| D.d状态下,保持其他条件不变,向容器中再加入1molCO2与0.5molC2H4,v(正)<v(逆) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
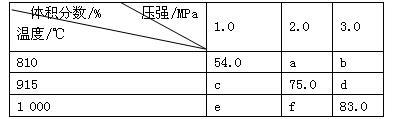
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
| A.a<54.0 |
| B.b> f |
| C.915 ℃,2.0 MPa时E的转化率为60% |
| D.K(1000 ℃)>K(810 ℃) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应:A(g)+B(g) xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是

 xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
xC(g)+D(s) ΔH<0在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是
| A.x=1 |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是增大反应物的浓度或降温 |
| D.t1~t2、t2~t3平衡常数相等,且K=4 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在体积为2L的密闭容器中进行下列反应:C(g)+CO2(g) 2CO(g);△H=+Q kJ·mol-1。下图为CO2、CO的物质的量随时间t的变化关系图。下列说法不正确的是
2CO(g);△H=+Q kJ·mol-1。下图为CO2、CO的物质的量随时间t的变化关系图。下列说法不正确的是

 2CO(g);△H=+Q kJ·mol-1。下图为CO2、CO的物质的量随时间t的变化关系图。下列说法不正确的是
2CO(g);△H=+Q kJ·mol-1。下图为CO2、CO的物质的量随时间t的变化关系图。下列说法不正确的是
| A.在0-1min内CO的物质的量增加了2mol |
| B.当固焦炭的质量不发生变化时,说明反应已达平衡状态 |
| C.5min时再充入一定量的CO,n(CO)、n(CO2)的变化可分别由c、b曲线表示 |
| D.3min时温度由T1升高到T2,重新平衡时K(T2)小于K(T1) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将一定量的氨基甲酸铵置于恒容的密闭真空容器中(固体体积忽略不计),使其达到化学平衡:H2NCOONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
下列有关叙述正确的是
 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列有关叙述正确的是
| A.在低温下该反应能自发进行 |
| B.15℃时,该反应的化学平衡常数约为2.0 |
| C.当混合气体平均相对分子质量不变时,该反应达到化学反应限度 |
| D.恒温条件下,向原平衡体系中再充入2molNH3和1molCO2,达平衡后CO2浓度不变 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】下列变化过程的焓变(△H)和熵变(△S)均大于零的是
| A.H2O(g)→H2O(l) | B.N2(g)+O2(g)=2NO(g) |
| C.2H2O2(l)=2H2O(l)+O2(g) | D.Ag+(aq)+Cl-(aq)=AgCl(s) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】相同的温度和压强下,有关下列两个反应的说法不正确的是
注:其中Δn表示反应方程式中气体系数差;
| 反应 | ΔH/kJ•mol-1 | Δn | ΔS/J•K•mol-1 |
| MgCO3(s)=MgO(s)+CO2(g) | 117.6 | 1 | a |
| CaCO3(s)=CaO(s)+CO2(g) | 177.9 | 1 | b |
| A.因为Δn相同,所以a与b大小相近 |
| B.a-b=S[MgO(s)]+S[CaCO3(s)]-S[MgCO3(s)]-S[CaO(s)] |
| C.热分解温度:MgCO3(s)>CaCO3(s) |
| D.两个反应的ΔH和ΔS都大于零 |
您最近半年使用:0次


 恒容密闭容器中发生反应:
恒容密闭容器中发生反应: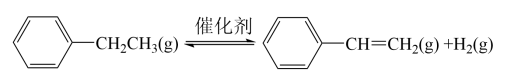

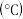

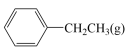

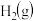
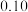
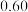
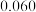


 体积分数比容器2中的小
体积分数比容器2中的小
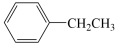
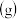 、
、
 、
、 、
、 可作为燃料电池的燃料,其相关热化学方程式如下。
可作为燃料电池的燃料,其相关热化学方程式如下。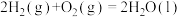
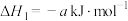

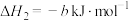




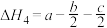
 ,则
,则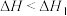
 能表示甲烷的燃烧热
能表示甲烷的燃烧热

