利用CO2催化加氢可制乙烯,反应为2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g) △H,在两个容积均为1L恒容密闭容器中,分别加入2molCO2、4molH2,分别选用两种催化剂,反应进行相同时间,测得CO2转化率随反应温度的变化如下图所示。下列说法正确的是
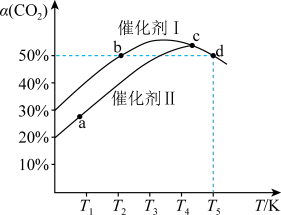

| A.使用催化剂I时反应的活化能低于催化剂II |
| B.△H>0 |
| C.b、d两状态下,化学反应速率相等 |
| D.d状态下,保持其他条件不变,向容器中再加入1molCO2与0.5molC2H4,v(正)<v(逆) |
21-22高三下·江苏徐州·阶段练习 查看更多[12]
(已下线)题型04 化学反应速率与平衡图像分析-2024年高考化学答题技巧与模板构建河北省保定市六校联考2023-2024学年高二上学期11月期中考试化学试题江西省宜春市宜丰中学2023-2024学年高二上学期9月月考化学试题(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)河南省南阳市2022-2023学年高三上学期11月期中考试化学试题(已下线)题型23 平衡常数、平衡转化率图象学科特色4 化学反应速率、平衡图像河南省南阳市2022-2023学年高三上学期期中质量评估化学试题(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)湖北省襄阳市第五中学2022届高三下学期适应性考试(二模)化学试题(已下线)卷06 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)江苏省徐州市新沂市第一中学2021-2022学年高三下学期3月月考化学试题
更新时间:2022-03-30 18:56:25
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】在恒温密闭容器中发生反应:CaCO3(s)⇌CaO(s)+CO2(g)ΔH>0反应达到平衡后, 时缩小容器体积,x随时间(t)变化的关系如图所示。x不可能是
时缩小容器体积,x随时间(t)变化的关系如图所示。x不可能是

 时缩小容器体积,x随时间(t)变化的关系如图所示。x不可能是
时缩小容器体积,x随时间(t)变化的关系如图所示。x不可能是
| A.V逆(逆反应速率) |
| B.ρ(容器内气体密度) |
| C.m(容器内CaO质量) |
D.c( 浓度) 浓度) |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2(T2>T1)时,Y的体积分数(或Y的物质的量分数)与时间的关系如图2所示。则下列结论正确的是
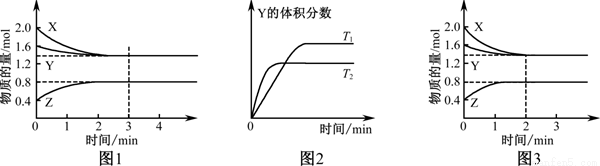

A.容器中发生的反应可表示为:4X(g)+Y(g) 2Z(g) 2Z(g) |
| B.反应进行的前3min内,用X表示的反应速率v(X)=0.3mol/(L·min) |
| C.升高温度,反应的化学平衡常数K增大 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列有关对应图像的说法正确的是

A.据①知,某温度下,平衡状态由A变到B时,平衡常数 |
B.据平衡常数的负对数(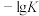 )—温度(T)图像②知,30℃时,B点对应状态的 )—温度(T)图像②知,30℃时,B点对应状态的 |
C.由 的稳定性与溶液pH的关系可知图③中 的稳定性与溶液pH的关系可知图③中 |
D.图④所示体系中气体平均摩尔质量: , , |
您最近半年使用:0次
【推荐2】向相同容积的甲、乙两容器中分别充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g)=2SO3(g) △H<0。若甲容器保持恒温恒容,乙容器保持恒温恒压,分别达到平衡。乙容器中平衡时生成SO3为1.6 mol,同时放出热量Q kJ。下列说法正确的是
| A.平衡时,反应放出的热量:甲>乙 |
| B.平衡时,O2的质量:甲<乙 |
| C.乙容器若把条件“恒温恒压”改为“恒压绝热”,则平衡后n(SO2)大于2.4 mol |
| D.平衡时,向乙容器中再通入一定量的SO3气体,重新达到平衡时,SO2的百分含量升高 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】温度为 时,在三个容积均为1L的恒容密闭容器中仅发生反应:
时,在三个容积均为1L的恒容密闭容器中仅发生反应: (正反应吸热)。实验测得:
(正反应吸热)。实验测得: ,
, ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是
 时,在三个容积均为1L的恒容密闭容器中仅发生反应:
时,在三个容积均为1L的恒容密闭容器中仅发生反应: (正反应吸热)。实验测得:
(正反应吸热)。实验测得: ,
, ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是| 容器编号 | 物质的起始浓度(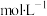 ) ) | 物质的平衡浓度(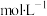 ) ) | ||
 |  |  |  | |
| I | 0.6 | 0 | 0 | 0.2 |
| II | 0.3 | 0.5 | 0.2 | |
| III | 0 | 0.6 | 0.3 | |
| A.达平衡时,容器I反应前、后的总压强之比为4∶5 |
B.达平衡时,容器II中 比容器I中的大 比容器I中的大 |
C.达平衡时,容器III中 的体积分数小于50% 的体积分数小于50% |
D.当温度改变为 时,若 时,若 ,则 ,则 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
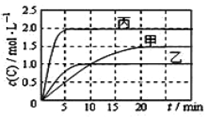
下列说法正确的是
 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 1L | 1L | 2L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1molA 2molB | 1molA 2molB | 4molA 8molB |
| A.由图可知Tl<T2,且正反应为吸热反应 |
| B.前5min内甲、乙、丙三个容器中反应的平均速率:v (A)乙<v(A)甲<v(A)丙 |
| C.平衡时A的转化率a : a乙<a甲<a丙 |
| D.T2时该反应的平衡常数K=1.33 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】一定温度下,在甲、乙、丙三个体积均为10L的恒容密闭容器中分别发生反应 ,实验过程中测得的相关数据如下表所示。下列说法错误的是
,实验过程中测得的相关数据如下表所示。下列说法错误的是
 ,实验过程中测得的相关数据如下表所示。下列说法错误的是
,实验过程中测得的相关数据如下表所示。下列说法错误的是| 容器 | 温度/℃ | 物质的起始加入量 | 平衡时Z的物质的量 |
| 甲 | 1000 | 1molX、1molY、0molZ | 0.6mol |
| 乙 | 1000 | 2molX、2molY、0molZ | |
| 丙 | 1200 | 0molX、0molY、1molZ | 0.5mol |
| A.该反应的正反应放热 |
| B.平衡时逆反应速率:v(丙)>v(甲) |
| C.平衡时Z的物质的量:n(乙)>2n(甲) |
D.1200℃时,该反应的平衡常数 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是
| A.某放热反应能自发进行,因此该反应是熵增反应 |
| B.用惰性电极电解含有H218O的普通水时,阳极可能产生两种相对分子质量不同的氧分子 |
C.反应A(g)  B(g) △H,若正反应的活化能为EakJ/mol,逆反应的活化能为EbkJ/mol,则△H=- (Ea-Eb) kJ/mol B(g) △H,若正反应的活化能为EakJ/mol,逆反应的活化能为EbkJ/mol,则△H=- (Ea-Eb) kJ/mol |
| D.3x%的A物质的溶液与x%的A物质的溶液等体积混合后溶液质量分数小于2x%,则A可能为乙醇 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表,下列说法错误的是
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表,下列说法错误的是
 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表,下列说法错误的是
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表,下列说法错误的是| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3 mol·L-1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A.当混合气体平均相对分子质量为26时说明该反应已达平衡 |
| B.达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量增大 |
| C.根据表中数据,计算15.0 ℃时的分解平衡常数约为2.0×10-9 |
| D.因该反应熵变(ΔS)大于0,焓变(ΔH)大于0,所以在高温下自发进行 |
您最近半年使用:0次

 和
和 反应生成
反应生成 的过程中主要涉及的反应如下:
的过程中主要涉及的反应如下:

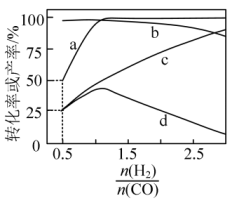
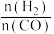 的变化情况如下图所示。
的变化情况如下图所示。 的选择性
的选择性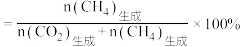 ]。
]。
 表示
表示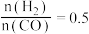 ,反应达平衡时,
,反应达平衡时,
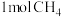 和一定量的
和一定量的 ,发生反应
,发生反应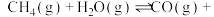
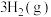 。
。 随温度的变化曲线如图所示。下列说法正确的是
随温度的变化曲线如图所示。下列说法正确的是



 ,当容器内压强不变时,反应达到平衡状态
,当容器内压强不变时,反应达到平衡状态 随温度变化情况。若在图示温度范围内焓变
随温度变化情况。若在图示温度范围内焓变 和熵变
和熵变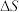 不变,且
不变,且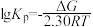 ,其中R为常数,T为温度。下列说法错误的是
,其中R为常数,T为温度。下列说法错误的是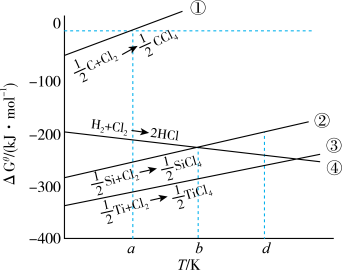
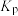 为1
为1 还原
还原 制备
制备


