下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟生成E,A是强碱,D的焰色为紫色 (部分反应物和生成物及水已略去)。
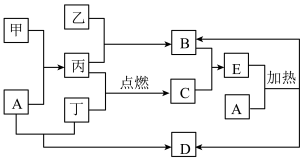
请回答下列问题
(1)写出工业制备B的化学方程式____________________ ;
(2)写出常温下,A与丁反应的离子方程式____________________ ;
(3)下图装置为用排空气法收集气体的实验装置

Ⅰ.当从M端通入气体时,可收集的气体有____________________ ;
Ⅱ.当从N端通入气体时,可收集的气体有____________________ ; (填数字编号)
①气体乙 ②气体丙 ③气体丁 ④气体B ⑤气体C
(4)E中所含阳离子的检验方法为(包括实验步骤、现象及结论)____________________ ;
(5)A中所含阳离子的检验方法为(包括实验步骤、现象及结论)____________________ 。

请回答下列问题
(1)写出工业制备B的化学方程式
(2)写出常温下,A与丁反应的离子方程式
(3)下图装置为用排空气法收集气体的实验装置

Ⅰ.当从M端通入气体时,可收集的气体有
Ⅱ.当从N端通入气体时,可收集的气体有
①气体乙 ②气体丙 ③气体丁 ④气体B ⑤气体C
(4)E中所含阳离子的检验方法为(包括实验步骤、现象及结论)
(5)A中所含阳离子的检验方法为(包括实验步骤、现象及结论)
14-15高一上·辽宁沈阳·期末 查看更多[1]
(已下线)2013-2014学年辽宁省沈阳市高一上教学质量监测化学试卷
更新时间:2016-12-09 05:14:32
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
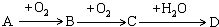
(1)若A是一种金属,C是淡黄色固体,写出C的一种用途_______ ;
(2)若A为淡黄色固体单质,写出D的浓溶液与铜反应的化学方程式______ ;
(3)若A是化合物,C是红棕色气体,则A的化学式为_____________ ;C转化为D的过程中,氧化剂与还原剂的质量比为__________________ 。
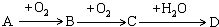
(1)若A是一种金属,C是淡黄色固体,写出C的一种用途
(2)若A为淡黄色固体单质,写出D的浓溶液与铜反应的化学方程式
(3)若A是化合物,C是红棕色气体,则A的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D均为中学化学常见的纯净物且都含有一种相同元素,A是单质,B是A的氧化物。它们有如图反应关系:
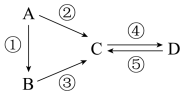
(1)若B是淡黄色固体,②③的反应中均有一种相同的反应物且摩尔质量为18g/mol,D俗称小苏打。则C的化学式为___________ ,写出物质B与 反应的化学方程式
反应的化学方程式___________ ,由D和澄清石灰水可得到C,写出该反应的离子方程式___________ 。
(2)若B是制作光导纤维的材料,②③的反应物中均有烧碱,D为酸。用氧化物表示C的组成___________ ,反应①②③④⑤中,属于氧化还原反应的有___________ (填序号),写出D转化为C的离子方程式___________ 。
(3)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为___________ ;若C、D组成元素相同,则C转化为D的离子方程式为___________ ,在D中滴入氢氧化钠溶液,一段时间内观察到的现象是___________ 。

(1)若B是淡黄色固体,②③的反应中均有一种相同的反应物且摩尔质量为18g/mol,D俗称小苏打。则C的化学式为
 反应的化学方程式
反应的化学方程式(2)若B是制作光导纤维的材料,②③的反应物中均有烧碱,D为酸。用氧化物表示C的组成
(3)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为
您最近一年使用:0次
【推荐1】下图中A~J分别代表相关反应的一种物质.已知A分解得到等物质的量的B、C、D,图中有部分生成物未标出.

请填写以下空白:
(1)A的化学式____________ ;
(2)写出反应①②的化学方程式:
①_____________ ,②___________ ;
(3)写出反应③的离子方程式:_______________________ ;
(4)在反应④中,当生成标准状况下2.24 L G时,转移电子数为________ mol。

请填写以下空白:
(1)A的化学式
(2)写出反应①②的化学方程式:
①
(3)写出反应③的离子方程式:
(4)在反应④中,当生成标准状况下2.24 L G时,转移电子数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫氰化钾(KSCN)是一种用途广泛的化学药品,常用于合成树脂、杀虫杀菌剂等。某实验小组用下图所示的装置制备硫化钾。
(1)制备NH4SCN溶液:三颈烧瓶D内盛放有CS2、水和催化剂,实验开始时,打开K1,(K2处于关闭状态)加热装置A、D,使A中产生的氨气缓缓通入到三颈烧瓶中,反应至CS2消失,反应的方程式为: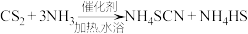 。
。
①写出A装置生成氨气的化学方程式___________
②仪器B的名称是:___________ 。
③装置C的作用是:___________ 。
④三颈烧瓶左侧导管口必须插入到下层的CS2液体中,主要原因是___________ (写出一条原因即可)。
(2)制备KSCN溶液:
熄灭A处的酒精灯,关闭K1,移开水浴,将装置D继续加热至105℃,NH4SCN完全分解后(反应方程式为 ),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。反应的化学方程式为
),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。反应的化学方程式为___________ 。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、___________ 、过滤、洗涤、干燥,得到硫氰化钾晶体。
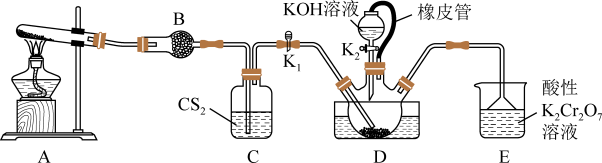
(1)制备NH4SCN溶液:三颈烧瓶D内盛放有CS2、水和催化剂,实验开始时,打开K1,(K2处于关闭状态)加热装置A、D,使A中产生的氨气缓缓通入到三颈烧瓶中,反应至CS2消失,反应的方程式为:
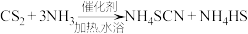 。
。①写出A装置生成氨气的化学方程式
②仪器B的名称是:
③装置C的作用是:
④三颈烧瓶左侧导管口必须插入到下层的CS2液体中,主要原因是
(2)制备KSCN溶液:
熄灭A处的酒精灯,关闭K1,移开水浴,将装置D继续加热至105℃,NH4SCN完全分解后(反应方程式为
 ),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。反应的化学方程式为
),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。反应的化学方程式为(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某无色溶液X,由Na+、Ag+、Ba2+、Al3+、Fe3+、AlO2﹣、CO32﹣、SO42﹣中的若干种离子组成,取该溶液进行如下实验:

(1)气体A的成分是________ (填化学式,下同),气体B的成分是________ 。
(2)写出步骤①发生反应的所有离子方程式________________________ 。
(3)写出步骤②形成白色沉淀甲的离子方程式________________________ 。
(4)通过上述实验,可确定X溶液中一定存在的离子是________ ,尚未确定是否存在的离子是________ ,只要设计一个简单的后续实验就可以确定该离子是否存在,该方法是________________________________________________________ 。

(1)气体A的成分是
(2)写出步骤①发生反应的所有离子方程式
(3)写出步骤②形成白色沉淀甲的离子方程式
(4)通过上述实验,可确定X溶液中一定存在的离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】高中化学课本必修一中出现的部分物质间的转化关系如下图所示(部分物质已省略。已知A→B是实验室制取氯气的主要方法之一,H的焰色试验呈黄色),请完成下列填空。
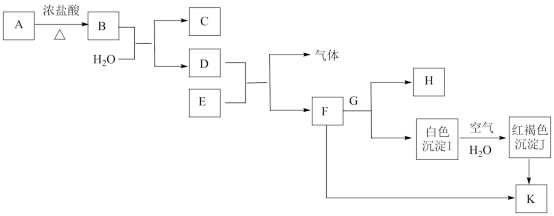
(1)E和H的化学式为:E___________ ;H___________ 。
(2)检验K溶液中阳离子的试剂是___________ 。若K中含有F的杂质,应加入___________ (填化学式)除杂。
(3)I转化为J的化学方程式为___________ 。
(4)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是___________(填字母序号)。
(5)当前,新冠病毒变异毒株奥密克戎来势汹汹,化学消毒剂在疫情防控中起着重要作用。
①目前,很多自来水厂用氯气来杀菌、消毒。A→B的离子反应方程式为___________ 。
②C可以杀菌、消毒,但不稳定,难以保存,原因是___________ (用化学方程式表示)。
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,该漂白液的有效成分是___________ 。
④ 为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(
为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠( )固体与B反应可得到
)固体与B反应可得到 和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
和NaCl,该反应中,氧化剂与还原剂的物质的量之比为___________ 。

(1)E和H的化学式为:E
(2)检验K溶液中阳离子的试剂是
(3)I转化为J的化学方程式为
(4)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是___________(填字母序号)。
A.胶体L的分散质粒子直径为 | B.胶体L比K的饱和溶液颜色深 |
| C.胶体L是均一的分散系 | D.胶体L具有丁达尔效应 |
①目前,很多自来水厂用氯气来杀菌、消毒。A→B的离子反应方程式为
②C可以杀菌、消毒,但不稳定,难以保存,原因是
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,该漂白液的有效成分是
④
 为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(
为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠( )固体与B反应可得到
)固体与B反应可得到 和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】共分如图所示的物质反应关系中,部分产物被略去。已知2 mol白色固体粉末X受热分解,恢复到室温生成白色固体A、无色液体B、无色气体C各1 mol。A、X、E、G、H的焰色反应均为黄色,且H为淡黄色固体。
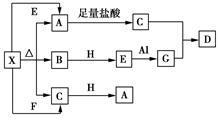
回答下列问题:
(1)写出下列物质的化学式:X________ ; H________ 。
(2)写出E+Al→G反应的化学方程式_________ ;
(3)写出G溶液中通入过量C制取D的反应离子方程式:____________________ ;
(4)写出X溶液中滴加过量澄清石灰水反应的离子方程式:__________________ ;
(5)0.1 mol H与足量的C反应,转移的电子数为________ 个。

回答下列问题:
(1)写出下列物质的化学式:X
(2)写出E+Al→G反应的化学方程式
(3)写出G溶液中通入过量C制取D的反应离子方程式:
(4)写出X溶液中滴加过量澄清石灰水反应的离子方程式:
(5)0.1 mol H与足量的C反应,转移的电子数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律,绘制出如下转化关系图(部分反应物或产物略去),并用于研究物质A、B、C、D的性质及其变化。
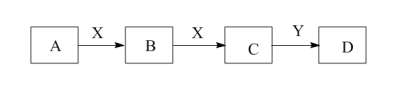
(1)若A是黄绿色气体,X是生活中应用最大量的金属,D是白色固体。
① 组成A的元素在周期表中的位置是______ 。
② 下列说法正确的是______ (填字母)。
a.B的水溶液中加入KSCN溶液,变为红色
b.C只具有还原性
c.若Y是碱,D放置在空气中会迅速变为灰绿色,最终变为红褐色
(2)若A、B、C、D的焰色反应均为黄色,X的固体俗称干冰。
① B转化为C的离子方程式是______ 。
② A用于呼吸面具或潜水艇中氧气的来源,则A和X反应生成1 mol B时,转移电子数为______ 。
③ C与Y反应生成X的离子方程式_________________ 。

(1)若A是黄绿色气体,X是生活中应用最大量的金属,D是白色固体。
① 组成A的元素在周期表中的位置是
② 下列说法正确的是
a.B的水溶液中加入KSCN溶液,变为红色
b.C只具有还原性
c.若Y是碱,D放置在空气中会迅速变为灰绿色,最终变为红褐色
(2)若A、B、C、D的焰色反应均为黄色,X的固体俗称干冰。
① B转化为C的离子方程式是
② A用于呼吸面具或潜水艇中氧气的来源,则A和X反应生成1 mol B时,转移电子数为
③ C与Y反应生成X的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
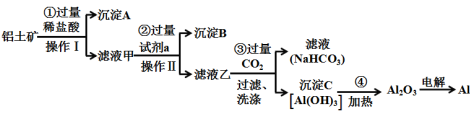
(1)用电解饱和食盐水制备试剂a的化学方程式为___________ ;
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为___________ ;
(3)步骤③中通入过量CO2气体而不加入过量盐酸的理由是___________ ;
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为___________ 。
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________ ;
a.MgO b.V2O5 c.Fe3O4 d.MnO2
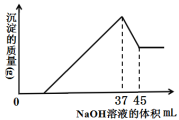
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为___________ 。

(1)用电解饱和食盐水制备试剂a的化学方程式为
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为
(3)步骤③中通入过量CO2气体而不加入过量盐酸的理由是
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是
a.MgO b.V2O5 c.Fe3O4 d.MnO2
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】为了解决环境污染问题,中国政府大力扶持新能源汽车行业的发展。新能源汽车的核心部件是锂离子电池,常用磷酸亚铁锂(LiFePO4)做电极材料。对LiFePO4废旧电极(含杂质Al、石墨粉)回收并获得高纯Li2CO3的工艺流程如图:
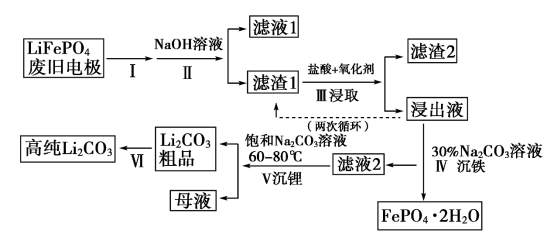
碳酸锂在水中溶解度:
(1)过程Ⅰ的操作是_______ 。
(2)过程Ⅱ加入足量NaOH溶液的作用是_______ (用化学方程式表示)。
(3)过程Ⅲ采用不同氧化剂分别进行实验,均采用Li含量为3.7%的原料,控制pH为3.5,浸取1.5h后,实验结果如表所示:
①实验2中,NaClO3与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为_______ 。
②综合考虑Li+的浸出率及环保因素,选择的氧化剂最好为_______ 。
(4)浸出液中存在大量H2PO 和HPO
和HPO ,结合平衡移动原理,解释过程Ⅳ:加入30%的Na2CO3溶液得到磷酸铁晶体的原因
,结合平衡移动原理,解释过程Ⅳ:加入30%的Na2CO3溶液得到磷酸铁晶体的原因_______ 。

碳酸锂在水中溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/℃ | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(1)过程Ⅰ的操作是
(2)过程Ⅱ加入足量NaOH溶液的作用是
(3)过程Ⅲ采用不同氧化剂分别进行实验,均采用Li含量为3.7%的原料,控制pH为3.5,浸取1.5h后,实验结果如表所示:
| 序号 | 酸 | 氧化剂 | 浸出液Li+浓度(g/L) | 滤渣中Li含量/% |
| 实验1 | HCl | H2O2 | 9.02 | 0.10 |
| 实验2 | HCl | NaClO3 | 9.05 | 0.08 |
| 实验3 | HCl | O2 | 7.05 | 0.93 |
①实验2中,NaClO3与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为
②综合考虑Li+的浸出率及环保因素,选择的氧化剂最好为
(4)浸出液中存在大量H2PO
 和HPO
和HPO ,结合平衡移动原理,解释过程Ⅳ:加入30%的Na2CO3溶液得到磷酸铁晶体的原因
,结合平衡移动原理,解释过程Ⅳ:加入30%的Na2CO3溶液得到磷酸铁晶体的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】明矾[Ka1(SO4)2·12H2O]在工业上用作净水剂,医药上用作收敛剂。实验小组采用废弃的铝制易拉罐按如下流程制备明矾大晶体。
(1)废铝制易拉罐溶于KOH溶液发生的主要反应为_______ (用离子方程式表示)。
(2)下列说法不正确的是_______。
(3)“系列操作Ⅱ”的装置如图所示,烧杯上方所盖的纸片的作用是_______ 。
步骤①: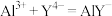
步骤②: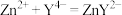
步骤③: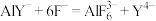
①NH4F溶液实验室_______ (填“能”或“不能”)盛装在玻璃细口瓶中。
②下列有关说法不正确的是_______ 。
A.天然水体样品中的Ca2+(CaY2-不与F-反应)不影响Al3+含量的测定
B.步骤①所加试剂EDTA,实验前不需要标定其浓度
C.如果步骤②所加Zn2+标准溶液偏少,会导致Al3+浓度的测定值小于真实值
③根据检测过程,请给出配合离子ZnY2-、AlY-、 的稳定性由弱到强的顺序:
的稳定性由弱到强的顺序:_______ 。
④要准确计算水样中Al3+浓度,须利用水样1的体积以及步骤_______ 的实验数据(选填:①、②、③、④)
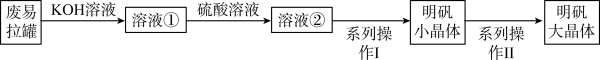
(1)废铝制易拉罐溶于KOH溶液发生的主要反应为
(2)下列说法不正确的是_______。
| A.可采取将废易拉罐剪碎、酒精灯加热等方式加快溶解速率 |
| B.加入KOH溶液至不再产生气泡后,趁热过滤,除去不溶物 |
| C.“系列操作Ⅰ”有:蒸发浓缩、冷却结晶、过滤、洗涤、灼烧 |
| D.制备明矾大晶体时,小晶体应悬挂在靠近烧杯底部的位置 |
(3)“系列操作Ⅱ”的装置如图所示,烧杯上方所盖的纸片的作用是


步骤①:
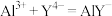
步骤②:
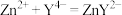
步骤③:
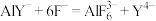
①NH4F溶液实验室
②下列有关说法不正确的是
A.天然水体样品中的Ca2+(CaY2-不与F-反应)不影响Al3+含量的测定
B.步骤①所加试剂EDTA,实验前不需要标定其浓度
C.如果步骤②所加Zn2+标准溶液偏少,会导致Al3+浓度的测定值小于真实值
③根据检测过程,请给出配合离子ZnY2-、AlY-、
 的稳定性由弱到强的顺序:
的稳定性由弱到强的顺序:④要准确计算水样中Al3+浓度,须利用水样1的体积以及步骤
您最近一年使用:0次




