为了解决环境污染问题,中国政府大力扶持新能源汽车行业的发展。新能源汽车的核心部件是锂离子电池,常用磷酸亚铁锂(LiFePO4)做电极材料。对LiFePO4废旧电极(含杂质Al、石墨粉)回收并获得高纯Li2CO3的工艺流程如图:
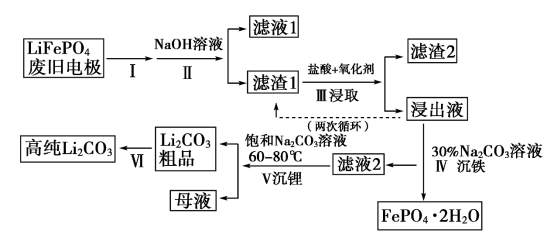
碳酸锂在水中溶解度:
(1)过程Ⅰ的操作是_______ 。
(2)过程Ⅱ加入足量NaOH溶液的作用是_______ (用化学方程式表示)。
(3)过程Ⅲ采用不同氧化剂分别进行实验,均采用Li含量为3.7%的原料,控制pH为3.5,浸取1.5h后,实验结果如表所示:
①实验2中,NaClO3与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为_______ 。
②综合考虑Li+的浸出率及环保因素,选择的氧化剂最好为_______ 。
(4)浸出液中存在大量H2PO 和HPO
和HPO ,结合平衡移动原理,解释过程Ⅳ:加入30%的Na2CO3溶液得到磷酸铁晶体的原因
,结合平衡移动原理,解释过程Ⅳ:加入30%的Na2CO3溶液得到磷酸铁晶体的原因_______ 。

碳酸锂在水中溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/℃ | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(1)过程Ⅰ的操作是
(2)过程Ⅱ加入足量NaOH溶液的作用是
(3)过程Ⅲ采用不同氧化剂分别进行实验,均采用Li含量为3.7%的原料,控制pH为3.5,浸取1.5h后,实验结果如表所示:
| 序号 | 酸 | 氧化剂 | 浸出液Li+浓度(g/L) | 滤渣中Li含量/% |
| 实验1 | HCl | H2O2 | 9.02 | 0.10 |
| 实验2 | HCl | NaClO3 | 9.05 | 0.08 |
| 实验3 | HCl | O2 | 7.05 | 0.93 |
①实验2中,NaClO3与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为
②综合考虑Li+的浸出率及环保因素,选择的氧化剂最好为
(4)浸出液中存在大量H2PO
 和HPO
和HPO ,结合平衡移动原理,解释过程Ⅳ:加入30%的Na2CO3溶液得到磷酸铁晶体的原因
,结合平衡移动原理,解释过程Ⅳ:加入30%的Na2CO3溶液得到磷酸铁晶体的原因
2021高三·全国·专题练习 查看更多[1]
(已下线)难点2 无机工艺流程中的操作分析-2021年高考化学【热点·重点·难点】专练(新高考)
更新时间:2021-05-20 10:02:37
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】碲是ⅥA 族元素,其单质和化合物在化工生产等方面具有广泛地应用。
(1)TeO2 是两性氧化物,微溶于水,可溶于强酸或强碱。TeO2 和足量 NaOH 溶液发生反应的离子方程式为_____ 。
(2)从粗铜精炼的阳极泥(主要含有 Cu2Te)中提取粗碲的一种工艺流程如图:
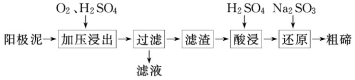
①已知加压酸浸时控制溶液的 pH 为 5.0,生成 TeO2 沉淀。如果 H2SO4 溶液浓度过大,产生 的后果是______________________________________________ 。
②对滤渣“酸浸”后,将 Na2SO3 加入 Te(SO4)2 溶液中进行“还原”得到固态碲,该反应的离子 方程式是______________________________________________ 。
③“还原”得到固态碲后分离出粗碲后,对粗碲进行洗涤,判断洗涤干净的实验操作和现象是_____ 。
(3)已知阳极泥中 Cu2Te 的含量为 a%,则 m 吨阳极泥理论上可制得纯度为 n%的粗碲_____ 吨。
(1)TeO2 是两性氧化物,微溶于水,可溶于强酸或强碱。TeO2 和足量 NaOH 溶液发生反应的离子方程式为
(2)从粗铜精炼的阳极泥(主要含有 Cu2Te)中提取粗碲的一种工艺流程如图:

①已知加压酸浸时控制溶液的 pH 为 5.0,生成 TeO2 沉淀。如果 H2SO4 溶液浓度过大,产生 的后果是
②对滤渣“酸浸”后,将 Na2SO3 加入 Te(SO4)2 溶液中进行“还原”得到固态碲,该反应的离子 方程式是
③“还原”得到固态碲后分离出粗碲后,对粗碲进行洗涤,判断洗涤干净的实验操作和现象是
(3)已知阳极泥中 Cu2Te 的含量为 a%,则 m 吨阳极泥理论上可制得纯度为 n%的粗碲
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】铬是一种具有战略意义的金属,它具有多种价态,单质铬熔点为1857℃。
(1)工业上以铬铁矿[主要成分是Fe(CrO2)2]为原料冶炼铬的流程如图所示:
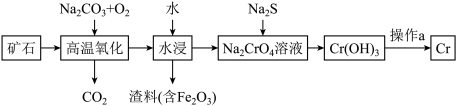
①Fe(CrO2)2中各元素化合价均为整数,则铬为___________ 价。
②操作a由两种均发生了化学反应的过程构成,其内容分别是___________ 、与铝粉混合高温下发生铝热反应。
(2)Cr(OH)3是两性氢氧化物,请写出其分别与NaOH、稀硫酸反应的离子方程式___________ 、___________ 。
(3)水中的铬元素对水质及环境均有严重的损害作用,必须进行无害化处理。转化为重要产品磁性铁铬氧体(CrxFeyOz):先向含CrO 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分Fe2+)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分Fe2+)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
①写出CrO 在酸性条件下被Fe2+还原为Cr3+的离子方程式
在酸性条件下被Fe2+还原为Cr3+的离子方程式___________ 。
②若处理含1molCrO (不考虑其他含铬微粒)的污水时恰好消耗10molFeSO4,则当铁铬氧体中n(Fe2+)∶n(Fe3+)=3∶2时,铁铬氧体的化学式为
(不考虑其他含铬微粒)的污水时恰好消耗10molFeSO4,则当铁铬氧体中n(Fe2+)∶n(Fe3+)=3∶2时,铁铬氧体的化学式为___________ 。
(4)利用K2Cr2O7测定CuI样品中CuI质量分数(杂质不参加反应)的方法如下:称取CuI样品0.600g,向其中加入足量Fe2(SO4)3溶液恰好使其溶解,生成Fe2+、Cu2+和I2。待充分反应后,滴加5.000×10-2mol·L-1K2Cr2O7溶液氧化其中的Fe2+,当恰好完全反应时消耗K2Cr2O7溶液的体积为20.00mL。计算该样品中CuI的质量分数(写出计算过程)_____ 。
(1)工业上以铬铁矿[主要成分是Fe(CrO2)2]为原料冶炼铬的流程如图所示:

①Fe(CrO2)2中各元素化合价均为整数,则铬为
②操作a由两种均发生了化学反应的过程构成,其内容分别是
(2)Cr(OH)3是两性氢氧化物,请写出其分别与NaOH、稀硫酸反应的离子方程式
(3)水中的铬元素对水质及环境均有严重的损害作用,必须进行无害化处理。转化为重要产品磁性铁铬氧体(CrxFeyOz):先向含CrO
 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分Fe2+)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分Fe2+)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。①写出CrO
 在酸性条件下被Fe2+还原为Cr3+的离子方程式
在酸性条件下被Fe2+还原为Cr3+的离子方程式②若处理含1molCrO
 (不考虑其他含铬微粒)的污水时恰好消耗10molFeSO4,则当铁铬氧体中n(Fe2+)∶n(Fe3+)=3∶2时,铁铬氧体的化学式为
(不考虑其他含铬微粒)的污水时恰好消耗10molFeSO4,则当铁铬氧体中n(Fe2+)∶n(Fe3+)=3∶2时,铁铬氧体的化学式为(4)利用K2Cr2O7测定CuI样品中CuI质量分数(杂质不参加反应)的方法如下:称取CuI样品0.600g,向其中加入足量Fe2(SO4)3溶液恰好使其溶解,生成Fe2+、Cu2+和I2。待充分反应后,滴加5.000×10-2mol·L-1K2Cr2O7溶液氧化其中的Fe2+,当恰好完全反应时消耗K2Cr2O7溶液的体积为20.00mL。计算该样品中CuI的质量分数(写出计算过程)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于18。其中只有C、D为金属元素;A和C的最外层均只有1个电子;B和E的最外层电子数相同,且B的L层电子数是K层电子数的3倍;D常用作易拉罐外壳。完成下列问题:
(1)写出相应元素的元素符号:B___________ ,E___________ 。
(2)A的一种核素中质子数为质量数的 ,则以
,则以 X的形式表示该核素为
X的形式表示该核素为___________ 。
(3)E元素的最高化合价为___________ 。
(4)A2B和C2B2反应的化学方程式___________ 。
(5)D与氢氧化钠溶液反应的化学方程式___________ 。
(1)写出相应元素的元素符号:B
(2)A的一种核素中质子数为质量数的
 ,则以
,则以 X的形式表示该核素为
X的形式表示该核素为(3)E元素的最高化合价为
(4)A2B和C2B2反应的化学方程式
(5)D与氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,元素A有可变化合价,它们之间存在如下图的所示的转化关系。由此推断:

(1) 甲的化学式为________,丙的化学式为_________。
(2)写出甲和D反应的化学方程式_______________________。
(3)已知D能与烧碱溶液反应,写出D与烧碱溶液反应的离子方程式_______________。
(4)为检验化合物甲中元素的化合价,需要用到的药品有___________
A.稀硫酸
B.盐酸
C.硫氰化钾溶液
D.高锰酸钾溶液
(5)为测定A和乙高温反应后所得固体中化合物甲的质量分数。取反应后所得固体并设计以下实验:

化合物甲的质量分数为______。

(1) 甲的化学式为________,丙的化学式为_________。
(2)写出甲和D反应的化学方程式_______________________。
(3)已知D能与烧碱溶液反应,写出D与烧碱溶液反应的离子方程式_______________。
(4)为检验化合物甲中元素的化合价,需要用到的药品有___________
A.稀硫酸
B.盐酸
C.硫氰化钾溶液
D.高锰酸钾溶液
(5)为测定A和乙高温反应后所得固体中化合物甲的质量分数。取反应后所得固体并设计以下实验:

化合物甲的质量分数为______。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
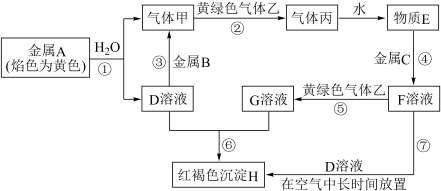
请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B
(2)写出实验室制备黄绿色气体乙的化学方程式:
反应过程⑦可能观察到的实验现象是:
产生红褐色沉淀的化学方程式是
(3)反应③中的离子方程式是
(4)向G溶液中加入H2S的离子方程式是
(5)反应⑦中如果可以长时间看到白色沉淀,可采取哪些方法:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】在2L恒温恒容密闭容器中投入2molSO2和1molO2在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。___________ ;平衡时,SO2的转化率为___________ 。
(2)下列叙述能判断该反应达到平衡状态的是___________ (填序号)。
①容器中压强不再改变
②容器中气体密度不再改变
③SO3的质量不再改变
④O2的物质的量浓度不再改变
⑤SO2的消耗速率和SO3的生成速率相等
(3)以下操作会引起化学反应速率变快的是___________ (填字母)。
A.向容器中通入氦气 B.升高温度 C.扩大容器的容积 D.向容器中通入O2 E.使用催化剂
(4)25min时,正反应速率___________ 逆反应速率(填“>”“<”或“=”)。
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:___________ 。(填“正极”或“负极”)
②电解质溶液中OH-离子向___________ 移动(填“电极a”或“电极b”)。
③电极b的电极反应式为___________ 。

(2)下列叙述能判断该反应达到平衡状态的是
①容器中压强不再改变
②容器中气体密度不再改变
③SO3的质量不再改变
④O2的物质的量浓度不再改变
⑤SO2的消耗速率和SO3的生成速率相等
(3)以下操作会引起化学反应速率变快的是
A.向容器中通入氦气 B.升高温度 C.扩大容器的容积 D.向容器中通入O2 E.使用催化剂
(4)25min时,正反应速率
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
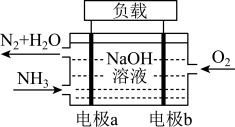
②电解质溶液中OH-离子向
③电极b的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验是化学研究的一种重要手段,请完成以下实验的探究与分析。
(1)中和热测定实验的关键是准确配制一定物质的量浓度的溶液,量热器尽量做到绝热;在量热过程中尽量避免热量的散失,准确测量出反应前后溶液温度的变化。请回答下列问题:
①测定中和热时需要用到的玻璃仪器有大烧杯、小烧杯、量筒、温度计和_______ ,在大、小烧杯之间填满碎泡沫(或碎纸条)的作用是_______ 。
②该实验常用 的盐酸和
的盐酸和 的
的 溶液各
溶液各 进行反应,
进行反应, 的浓度大于
的浓度大于 的浓度,原因是
的浓度,原因是_______ 。
③若上述盐酸、 溶液的密度都近似为
溶液的密度都近似为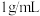 ,中和后生成的溶液的比热容
,中和后生成的溶液的比热容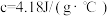 ,混合溶液的起始温度为
,混合溶液的起始温度为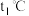 ,最高温度为
,最高温度为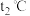 ,则中和热
,则中和热
_______  (填表达式,下同)
(填表达式,下同)
(2)某研究性学习小组利用 溶液和酸性
溶液和酸性 溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:(不考虑溶液混合所引起的体积缩小)
溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:(不考虑溶液混合所引起的体积缩小)
①通过实验A、B,可探究出浓度的改变对反应速率的影响,其中
_______ ;
_______ 。通过实验_______ 可探究出温度变化对化学反应速率的影响。
②C组实验中溶液褪色时间
_______ (填“ ”或“
”或“ ”)8s,C组实验的反应速率
”)8s,C组实验的反应速率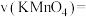
_______ 。(用含有 的式子表示)
的式子表示)
(1)中和热测定实验的关键是准确配制一定物质的量浓度的溶液,量热器尽量做到绝热;在量热过程中尽量避免热量的散失,准确测量出反应前后溶液温度的变化。请回答下列问题:
①测定中和热时需要用到的玻璃仪器有大烧杯、小烧杯、量筒、温度计和
②该实验常用
 的盐酸和
的盐酸和 的
的 溶液各
溶液各 进行反应,
进行反应, 的浓度大于
的浓度大于 的浓度,原因是
的浓度,原因是③若上述盐酸、
 溶液的密度都近似为
溶液的密度都近似为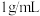 ,中和后生成的溶液的比热容
,中和后生成的溶液的比热容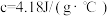 ,混合溶液的起始温度为
,混合溶液的起始温度为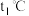 ,最高温度为
,最高温度为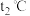 ,则中和热
,则中和热
 (填表达式,下同)
(填表达式,下同)(2)某研究性学习小组利用
 溶液和酸性
溶液和酸性 溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:(不考虑溶液混合所引起的体积缩小)
溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:(不考虑溶液混合所引起的体积缩小)| 实验序号 | 实验温度/K | 参加反应的物质 | 溶液颜色褪至无色时所需时间/s | ||||
 溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | |||||
 |  |  |  |  | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | 6 |
| B |  | 2 | 0.02 | 3 | 0.1 |  | 8 |
| C | 313 | 2 | 0.02 |  | 0.1 | 1 |  |


②C组实验中溶液褪色时间

 ”或“
”或“ ”)8s,C组实验的反应速率
”)8s,C组实验的反应速率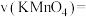
 的式子表示)
的式子表示)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】优化反应条件是研究化学反应的重要方向。
(1)以硫代硫酸钠与硫酸的反应Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。
①表中,a为______ ,b为______ 。
②实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象为_______ 。
③硫代硫酸钠可用于从含氧化银的矿渣中浸出银,反应如下:Ag2O+4S2O32-+H2O⇌2[Ag(S2O3)2]3-+2OH-。在实际生产中,为了提高银的浸出率需要调节pH的范围为8.5~9.5,解释其原因:_________ 。
(2)工业上常用空气催化氧化法除去电石渣浆(含 CaO)上清液中的S2-,并制取石膏(CaSO4•2H2O),其中的物质转化过程如图所示。

①过程Ⅰ、Ⅱ中,起催化剂作用的物质是_________ 。
②过程Ⅱ中,反应的离子方程式为________ 。
③根据物质转化过程,若将10L上清液中的S2-转化为SO42-(S2-浓度为320mg/L),理论上共需要标准状况下的O2的体积为_______ L。
(1)以硫代硫酸钠与硫酸的反应Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。
| 实验序 号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | 温度/℃ | ||
| 浓度/(mol/L) | 体积/mL | 浓度/(mol/L) | 体积/mL | 体积/mL | ||
| Ⅰ | 0.1 | 1.5 | 0.1 | 1.5 | 10 | 20 |
| Ⅱ | 0.1 | 2.5 | 0.1 | 1.5 | 9 | a |
| Ⅲ | 0.1 | b | 0.1 | 1.5 | 9 | 30 |
②实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象为
③硫代硫酸钠可用于从含氧化银的矿渣中浸出银,反应如下:Ag2O+4S2O32-+H2O⇌2[Ag(S2O3)2]3-+2OH-。在实际生产中,为了提高银的浸出率需要调节pH的范围为8.5~9.5,解释其原因:
(2)工业上常用空气催化氧化法除去电石渣浆(含 CaO)上清液中的S2-,并制取石膏(CaSO4•2H2O),其中的物质转化过程如图所示。

①过程Ⅰ、Ⅱ中,起催化剂作用的物质是
②过程Ⅱ中,反应的离子方程式为
③根据物质转化过程,若将10L上清液中的S2-转化为SO42-(S2-浓度为320mg/L),理论上共需要标准状况下的O2的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】炼铁厂用铁矾渣制备FeCO3过程如图:
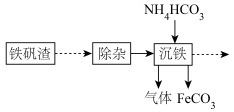
其中沉铁的过程中加入NH4HCO3,实现向目标产物碳酸亚铁的转化,碳酸亚铁可用于制备补血剂。某研究小组模拟“沉铁”过程设计如图实验,在实验室制备FeCO3。
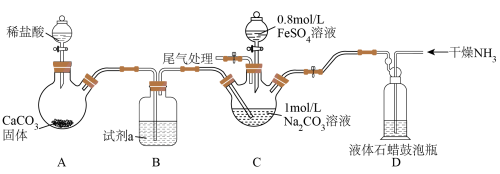
已知:FeCO3是白色固体,难溶于水。
【实验I】
(1)试剂a的作用是________ 。
(2)关闭C、D之间的止水夹,向C装置的Na2CO3溶液中通入足量CO2气体,写出发生反应的离子方程式________ ,再加入0.8mol/LFeSO4溶液后,观察到C装置中产生气泡(CO2)和白色沉淀(主要是FeCO3),请结合化学用语从平衡的角度解释产生气泡和FeCO3的原因________ 。
(3)产生白色沉淀,经过滤、洗涤、干燥,最终得到FeCO3固体,但固体产品检测后发现纯度并不高,则可能含有的杂质是________ (写化学式)。

其中沉铁的过程中加入NH4HCO3,实现向目标产物碳酸亚铁的转化,碳酸亚铁可用于制备补血剂。某研究小组模拟“沉铁”过程设计如图实验,在实验室制备FeCO3。

已知:FeCO3是白色固体,难溶于水。
【实验I】
(1)试剂a的作用是
(2)关闭C、D之间的止水夹,向C装置的Na2CO3溶液中通入足量CO2气体,写出发生反应的离子方程式
(3)产生白色沉淀,经过滤、洗涤、干燥,最终得到FeCO3固体,但固体产品检测后发现纯度并不高,则可能含有的杂质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如图实验: (aq)(橙色)+H2O(l)
(aq)(橙色)+H2O(l) 2CrO
2CrO (aq)(黄色)+2H+(aq)△H1=+13.8kJ•mol-1
(aq)(黄色)+2H+(aq)△H1=+13.8kJ•mol-1
②+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为墨绿色。
(1)对比试管c和b,推测试管c的现象是:__ 。
(2)对比试管a和b,发现a中溶液橙色比b的更深,请用平衡移动理论分析原因:____ 。
(3)对比试管a、b、c的实验现象,若pH增大,则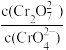
__ (选填“增大”,“减小”,“不变”);
(4)分析如图试管c中滴加KI溶液无明显现象、继续滴加过量稀H2SO4溶液变成墨绿色,由此实验现象,说明+6价铬盐氧化性强弱为Cr2O
____ CrO (填“大于”,“小于”,“不确定”);
(填“大于”,“小于”,“不确定”);
(5)电解法处理:工业上处理含Cr2O 离子的酸性废水,用石墨为电极进行电解,将Cr2O
离子的酸性废水,用石墨为电极进行电解,将Cr2O 离子还原为可溶性Cr3+。则Cr2O
离子还原为可溶性Cr3+。则Cr2O 离子在
离子在___ 极(填“阴”或“阳”)放电,写出Cr2O 放电的电极反应式
放电的电极反应式___ 。

 (aq)(橙色)+H2O(l)
(aq)(橙色)+H2O(l) 2CrO
2CrO (aq)(黄色)+2H+(aq)△H1=+13.8kJ•mol-1
(aq)(黄色)+2H+(aq)△H1=+13.8kJ•mol-1②+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为墨绿色。
(1)对比试管c和b,推测试管c的现象是:
(2)对比试管a和b,发现a中溶液橙色比b的更深,请用平衡移动理论分析原因:
(3)对比试管a、b、c的实验现象,若pH增大,则
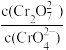
(4)分析如图试管c中滴加KI溶液无明显现象、继续滴加过量稀H2SO4溶液变成墨绿色,由此实验现象,说明+6价铬盐氧化性强弱为Cr2O

 (填“大于”,“小于”,“不确定”);
(填“大于”,“小于”,“不确定”);(5)电解法处理:工业上处理含Cr2O
 离子的酸性废水,用石墨为电极进行电解,将Cr2O
离子的酸性废水,用石墨为电极进行电解,将Cr2O 离子还原为可溶性Cr3+。则Cr2O
离子还原为可溶性Cr3+。则Cr2O 离子在
离子在 放电的电极反应式
放电的电极反应式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】盐酸羟胺(化学式为 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
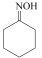 (环己酮肟)
(环己酮肟)
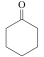 (环己酮)
(环己酮)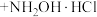
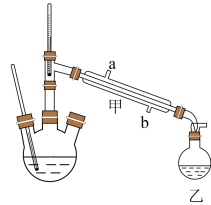
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。
盐酸羟胺在不同温度下的溶解度如下表:
(1)仪器甲中进水口应为___________ 。
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是___________ 。
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
(4)反应后,从三口烧瓶的溶液中获取盐酸羟胺的实验方法为___________。
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵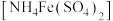 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。
反应原理为:①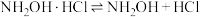
②
③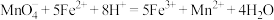
(5)将反应②补充完整,并标出电子转移的方向和数目___________ 。
(6)配制上述盐酸羟胺溶液所需要的定量仪器有___________ 。
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为___________ 。
(7)通过计算判断该产品的纯度级别___________ 。(写出计算过程)
已知:
 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
 (环己酮肟)
(环己酮肟)
 (环己酮)
(环己酮)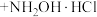
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。

盐酸羟胺在不同温度下的溶解度如下表:
| 温度(℃) | 溶解度(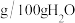 ) ) |
| 20 | 46.7 |
| 40 | 54.9 |
| 60 | 63.2 |
| 80 | 71.1 |
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
| A.共价键 | B.离子键 | C.氢键 | D.范德华力 |
| A.冷却结晶 | B.渗析 | C.蒸馏 | D.萃取、分液 |
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵
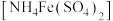 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。反应原理为:①
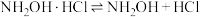
②

③
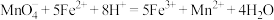
(5)将反应②补充完整,并标出电子转移的方向和数目
(6)配制上述盐酸羟胺溶液所需要的定量仪器有
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为
(7)通过计算判断该产品的纯度级别
| 纯度级别 | 优级纯 | 分析纯 | 化学纯 |
质量分数 | 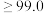 |  |  |

您最近一年使用:0次

 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
 ,反应①应通入
,反应①应通入 气体。
气体。 具有
具有 检验其中含有
检验其中含有 的方法是
的方法是

