浓度均为0.1mol/L的NH4Cl、(NH4)2SO4、NH4HSO4、(NH4)2Fe(SO4)2四种溶液中,设NH 离子浓度分别为amol/L、bmol/L和cmol/L,dmol/L则a、b、c、d关系为
离子浓度分别为amol/L、bmol/L和cmol/L,dmol/L则a、b、c、d关系为
 离子浓度分别为amol/L、bmol/L和cmol/L,dmol/L则a、b、c、d关系为
离子浓度分别为amol/L、bmol/L和cmol/L,dmol/L则a、b、c、d关系为| A.b=d>a=c | B.c<a<b<d | C.a<c<b=d | D.a<c<b<d |
更新时间:2023-05-11 00:08:46
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】水合肼( )是常见的航天器燃料,其制备原理为:
)是常见的航天器燃料,其制备原理为: ,设NA为阿伏加德罗常数,下列有关说法正确的是
,设NA为阿伏加德罗常数,下列有关说法正确的是
 )是常见的航天器燃料,其制备原理为:
)是常见的航天器燃料,其制备原理为: ,设NA为阿伏加德罗常数,下列有关说法正确的是
,设NA为阿伏加德罗常数,下列有关说法正确的是A.常温常压下, 中所含电子数为10NA 中所含电子数为10NA |
B. 中含有极性共价键数目为5NA 中含有极性共价键数目为5NA |
C. 溶液中含有的 溶液中含有的 数目为0.1NA 数目为0.1NA |
D.反应生成 时转移电子数为2NA 时转移电子数为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】NA代表阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下22.4 LO2与足量H2反应生成H2O,转移的电子数为4NA |
| B.常温下2.24 L N2中共用电子对数目为0.3NA |
| C.1L0.1mol·L-1 NH4Cl溶液中,NH4+的数目为0.1NA |
| D.31gP4分子中含有的P-P键数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】实验室使用pH传感器来测定某Na2A和NaHA混合溶液中NaHA的含量。用0.1mol·L−1盐酸滴定该混合溶液,得到如下曲线。以下说法错误的是
【注】滴定过程中,当滴入标准溶液的物质的量与待测组分的物质的量恰好符合化学反应式所表示的计量关系时,称反应达到了化学计量点,简称计量点。

【注】滴定过程中,当滴入标准溶液的物质的量与待测组分的物质的量恰好符合化学反应式所表示的计量关系时,称反应达到了化学计量点,简称计量点。

| A.未滴定时该混合溶液中:c(A2−)+2c(OH−)=2c(H2A)+c(HA−)+2c(H+) |
| B.滴加10mL盐酸时:c(Na+)=c(H2A)+c(HA−)+c(A2−)+c(Cl−) |
| C.滴加30mL盐酸时:c(Na+)=c(Cl−)>c(H2A)>c(H+)>c(OH−) |
| D.将等浓度的H2A水溶液和等浓度的Na2A混合,溶液可能显酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在0.1mol·L-1的NH4HSO4溶液中,下列关于微粒物质的量浓度的关系式不正确的是
A.c平(H+)>c平( )>c平( )>c平( ) ) |
B.c平( )+c平(H+)=2c平( )+c平(H+)=2c平( )+c平(OH-) )+c平(OH-) |
C.c平(H+)=c平( )+c平(NH3·H2O)+c平(OH-) )+c平(NH3·H2O)+c平(OH-) |
D.常温下向该溶液中滴加NaOH溶液至中性后:c平(Na+)>c平( )>c平( )>c平( )>c平(OH-)=c平(H+) )>c平(OH-)=c平(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温时,将 的氨水滴加到
的氨水滴加到 的盐酸中,下列说法正确的是
的盐酸中,下列说法正确的是
 的氨水滴加到
的氨水滴加到 的盐酸中,下列说法正确的是
的盐酸中,下列说法正确的是 A.若混合溶液中 ,则 ,则 |
B.若混合液中 ,则 ,则 |
C.若混合液中 ,则混合液的pH<7 ,则混合液的pH<7 |
D.若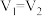 ,且混合液的pH<7,则一定 ,且混合液的pH<7,则一定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】测定 0.1 mol/LNa2SO3溶液先升温再降温过程中的 pH ,数据如下。
实验过程中,取①、④时刻的溶液,加入盐酸酸化的 BaCl2 溶液做对比实验,④产生白色沉淀多。下列说法不正确的是
时刻 | ① | ② | ③ | ④ |
温度/°C | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
| A.此实验中 Na2SO3溶液的 pH 是由 pH 计测定的 |
| B.④与①的 PH 不同,是由于 SO32—浓度减小造成的 |
| C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致 |
| D.①与④的 KW值相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】要求设计实验证明某种盐的水解是吸热的,有四位学生分别作出如下回答,其中正确的是
| A.甲学生:将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的 |
| B.乙学生:在盐酸中加入相同温度的氨水,若实验过程中混合液温度下降,说明盐类水解是吸热的 |
| C.丙学生:在醋酸钠溶液中加入醋酸钠晶体,若溶液温度下降,说明盐类水解是吸热的 |
| D.丁学生:在醋酸钠溶液中滴入酚酞试液,加热后若红色加深,说明盐类水解是吸热的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验操作能达到实验目的的是
| 实验目的 | 实验操作 | |
| A | 制备无水AlCl3 固体 | 蒸干Al与稀盐酸反应后所得的溶液 |
| B | 证明Na2CO3溶液中的水解平衡 | 向Na2CO3溶液中滴加酚酞溶液变红,加入足量BaCl2固体,搅拌,溶液逐渐褪色 |
| C | 验证铁的吸氧腐蚀 | 将铁钉放入试管中,用盐酸浸没,产生气泡 |
| D | 验证Ksp(CuS)<Ksp(ZnS) | 在2mL 0.01mol/L的Na2S溶液中先滴入几滴0.01mol/L 的ZnSO4溶液有白色沉淀,再滴入CuSO4溶液,又出现黑色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 为二元弱酸,
为二元弱酸, ,
, 。室温下,下列说法不正确的是
。室温下,下列说法不正确的是
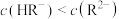

 的NaOH溶液完全中和时,消耗酸与碱溶液的体积比为1∶2
的NaOH溶液完全中和时,消耗酸与碱溶液的体积比为1∶2

