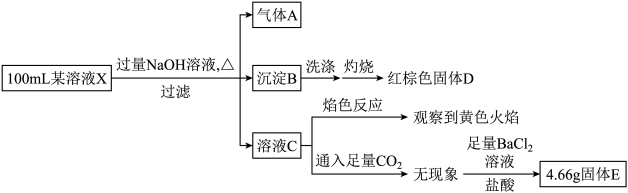
代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.标准状况下, 二氯甲烷中含有 二氯甲烷中含有 键的数目为 键的数目为 |
B.向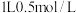 盐酸中通 盐酸中通 至中性(忽略溶液体积变化),此时 至中性(忽略溶液体积变化),此时 的数目为 的数目为 |
C.向 溶液中通入适量的 溶液中通入适量的 ,当有 ,当有 被氧化时,反应转移电子数为 被氧化时,反应转移电子数为 |
D.用惰性电极电解 溶液,当阴极生成 溶液,当阴极生成 气体(标准状况),转移电子数为 气体(标准状况),转移电子数为 |
更新时间:2023-06-02 22:09:16
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】用NA表示阿伏加德罗常数的数值,下列叙述正确的是
| A.标准状况下,22.4LN2和H2混合气中含2NA个原子 |
| B.2L物质的量浓度为0.5mol/L的MgCl2溶液中,Cl—的物质的量浓度为2mol/L |
| C.通常状况下,NA个CO分子占有的体积为22.4L |
| D.常温常压下,1mol氦气含有的原子数为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NA代表阿伏加德罗常数的值,下列说法正确的是
| A.在标准状况下,22.4 LH2O的质量约为18 g |
| B.136 g KHSO4固体中含有H+的数目为NA |
| C.含0.4 mol HCl的浓盐酸与足量MnO2反应,转移电子数目为0.2NA |
| D.1 mol Na2O2固体中含离子总数为3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】NA是阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,22.4 L D2中所含中子数为2NA |
B.0.l mol环氧乙烷( )中含有的共价键数为0.3NA )中含有的共价键数为0.3NA |
C.1 mol CO2与1 L 2 mol·L-1的NaOH溶液反应后,溶液中CO 数为NA 数为NA |
| D.6.8 g熔融的KHSO4中含有0.1NA个阳离子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】资源化利用 是实现“碳中和”战略目标的重要环节之一。对于反应:
是实现“碳中和”战略目标的重要环节之一。对于反应: ,下列有关说法正确的是
,下列有关说法正确的是
 是实现“碳中和”战略目标的重要环节之一。对于反应:
是实现“碳中和”战略目标的重要环节之一。对于反应: ,下列有关说法正确的是
,下列有关说法正确的是A. 和CO互为同素异形体 和CO互为同素异形体 |
B. 的水溶液可以导电,故 的水溶液可以导电,故 属于电解质 属于电解质 |
C.生成1 mol  时转移电子数约为 时转移电子数约为 |
D.大气中 、 、 含量升高均会加剧温室效应 含量升高均会加剧温室效应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】假定NA为阿伏加 德罗常数的值。下列说法正确的是
| A.常温下,46 g乙醇中含C-H键的数目为6NA |
| B.1 mol/L的K2SO4溶液中含K+的数目为2NA |
| C.标准状况下,22.4 L氦气中含质子的数目为4NA |
| D.1 mol HNO3被还原为NO转移电子的数目为3NA . |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设 是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是
 是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是A.2.0 g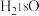 与 与 的混合物中所含原子数为0.3 的混合物中所含原子数为0.3 |
B.8 g甲烷分子中所含共价键的数目为 |
C.将0.1 mol  缓慢通入0.1 mol 缓慢通入0.1 mol  溶液中,被氧化的 溶液中,被氧化的 数最多为0.2 数最多为0.2 |
D.100 mL1 的蔗糖溶液中的分子数目为0.1 的蔗糖溶液中的分子数目为0.1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】NA为阿伏加德罗常数的值,下列有关说法正确的是
| A.常温常压下,31 g P4中含P-P键的数目为NA |
| B.标准状况下,将22.4 LCl2通入足量NaOH溶液中,转移电子数为NA |
| C.一定条件下,6.4 g铜粉与过量的硫粉充分反应,转移电子数为0.2NA |
| D.常温常压下,46 g NO2与92 g N2O4所含的分子数相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】设NA为阿伏加德罗常数的值,下列说法正确的是( )
①50mL12mol/L的盐酸与足量MnO2共热,转移电子数为0.3NA
②2.0gH218O与D216O的混合物中所含中子数为NA
③常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA
④常温常压下,6.72 L NO2与水充分反应转移的电子数目为0.2NA
⑤标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0.1NA
⑥10g46%的乙醇水溶液中所含氢原子数目为0.6NA
⑦60 g石英晶体中含有的Si﹣O键数目为2NA
⑧25℃时,100mlpH=13的Ba(OH)2溶液中OH﹣的数目为0.02NA
①50mL12mol/L的盐酸与足量MnO2共热,转移电子数为0.3NA
②2.0gH218O与D216O的混合物中所含中子数为NA
③常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA
④常温常压下,6.72 L NO2与水充分反应转移的电子数目为0.2NA
⑤标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0.1NA
⑥10g46%的乙醇水溶液中所含氢原子数目为0.6NA
⑦60 g石英晶体中含有的Si﹣O键数目为2NA
⑧25℃时,100mlpH=13的Ba(OH)2溶液中OH﹣的数目为0.02NA
| A.①②③⑥⑦⑧ | B.②③ | C.①②③④⑤ | D.②③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,向 20 mL 0.2 mol/LH2A溶液中滴加0. 2 mol/L NaOH溶液.有关微粒的物质的量变化曲线如图所示(其中I代表H2A.,II代表HA—,III表A2—)。根据图示.判断下列说法正确的是
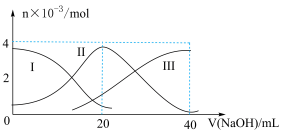

| A.当V(NaOH)=20 mL时.溶液中各离子浓度的大小关系为c(Na+)>c(HA—)>c(H+)>c(A2一)>c(OH—) |
| B.等体积、等物质的量浓度的NaOH溶液与H2 A溶液混合后,其溶液中水的电离程度比纯水中的大 |
| C.NaHA溶液中:c(OH—)+2c(A2—) =c(H+) +c(H2A ) |
| D.将Na2A溶液加水稀释.溶液中所有离子的浓度都减小.但部分离子的物质的量增加 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下向二元弱酸H2A溶液中滴加NaOH溶液,所得溶液的pH与离子浓度的变化关系如图所示。下列说法错误的是


A.曲线E表示溶液pH与 的变化关系 的变化关系 |
B. |
| C.图中a点对应溶液中: c(Na+ )>c(H2A)+2c(A2- ) |
| D.pH从4.6到5.8的过程中,水的电离程度逐渐增大 |
您最近一年使用:0次

 、
、 、
、 、
、 、
、 、
、 ,且所含离子的浓度均相等。某同学为了确认其成分,取部分溶液,设计并完成了如图所示实验。
,且所含离子的浓度均相等。某同学为了确认其成分,取部分溶液,设计并完成了如图所示实验。