HA是一元酸,下列说法不正确 的是
A.25℃时,若测得0.01 mol·L NaA溶液pH>7,则HR是弱酸 NaA溶液pH>7,则HR是弱酸 |
B.25℃时,若测得0.01 mol·L HA溶液pH>2且pH<7,则HR是弱酸 HA溶液pH>2且pH<7,则HR是弱酸 |
| C.体积相同、浓度相同的HA溶液与NaOH溶液恰好完全反应,则HR是弱酸 |
D.0.1 mol·L HA溶液与0.1 mol·L HA溶液与0.1 mol·L NaOH溶液混合呈中性,则 NaOH溶液混合呈中性,则 |
更新时间:2023-06-08 17:47:46
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列电离方程式中书写正确的是
A.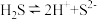 |
B. |
C. |
D.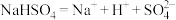 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列关于电解质溶液的叙述正确的是( )
| A.常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
| B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D.常温下,同浓度的Na2CO3与NaHCO3溶液相比,Na2CO3溶液为pH大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】等物质的量浓度的下列物质的水溶液,水电离程度最大的是
| A.CH3COONa | B.NaOH | C.HCl | D.KNO3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列反应的发生与“盐类水解平衡”或“难溶电解质的溶解平衡”无关 的是
A. 可溶于 可溶于 溶液 溶液 |
B.盐酸与 反应生成 反应生成 |
C. 溶液与NaOH溶液反应生成 溶液与NaOH溶液反应生成 |
D. 溶液和 溶液和 溶液反应生成 溶液反应生成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列实验方案、现象和结论都正确的是
选项 | 实验方案 | 现象 | 结论 |
A | 往 | 产生白色沉淀 |
|
B | 用精密pH试纸分别测定相同浓度NaClO和 |
| 酸性强弱: |
C | 将稀硫酸酸化的 | 溶液出现黄色 |
|
D | 向少量蒸馏水中逐渐加入苯酚晶体并振荡至浑浊,静置片刻后,将试管放在热水浴中,片刻后取出,冷却静置 | 加热后可得到澄清溶液,冷却后溶液变浑浊 | 较高温度,苯酚能与水混溶;温度降低,苯酚溶解度降低 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸 的
的 ,
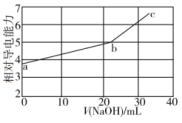
,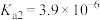 )溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列说法正确的是
)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列说法正确的是
 的
的 ,
,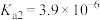 )溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列说法正确的是
)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列说法正确的是
A. 与 与 的导电能力之和比 的导电能力之和比 的大 的大 |
B.a、b、c三点对应的溶液中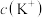 相等 相等 |
C.a点对应的溶液中: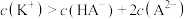 |
D.b点的混合溶液中,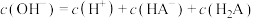 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】某溶液只含有Na+、A13+、Cl-、SO 四种离子,已知Na+、A13+、Cl-的个数比为1:2:3,则溶液中A13+和SO
四种离子,已知Na+、A13+、Cl-的个数比为1:2:3,则溶液中A13+和SO 的个数比为( )
的个数比为( )
 四种离子,已知Na+、A13+、Cl-的个数比为1:2:3,则溶液中A13+和SO
四种离子,已知Na+、A13+、Cl-的个数比为1:2:3,则溶液中A13+和SO 的个数比为( )
的个数比为( )| A.1:2 | B.1:4 | C.1:1 | D.2:3 |
您最近一年使用:0次

 固体样品溶液中加入
固体样品溶液中加入 溶液
溶液 溶液的pH值
溶液的pH值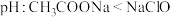
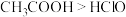
 加入
加入 溶液中
溶液中 强
强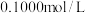 的
的 溶液滴定
溶液滴定 浓度为
浓度为
 时,三种溶液中
时,三种溶液中