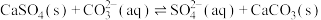为研究工业废水(含有 和Cu2+,且
和Cu2+,且 的浓度远大于Cu2+)的处理方法,某实验小组用NaOH溶液调节该废水的pH(溶液体积变化忽略不计),测得上层清液中铜元素的含量随pH变化如图所示:
的浓度远大于Cu2+)的处理方法,某实验小组用NaOH溶液调节该废水的pH(溶液体积变化忽略不计),测得上层清液中铜元素的含量随pH变化如图所示:
下列有关说法正确的是
 和Cu2+,且
和Cu2+,且 的浓度远大于Cu2+)的处理方法,某实验小组用NaOH溶液调节该废水的pH(溶液体积变化忽略不计),测得上层清液中铜元素的含量随pH变化如图所示:
的浓度远大于Cu2+)的处理方法,某实验小组用NaOH溶液调节该废水的pH(溶液体积变化忽略不计),测得上层清液中铜元素的含量随pH变化如图所示:| 图表 | 查阅资料 |
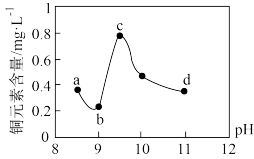 | 存在平衡Ⅰ: 存在平衡Ⅱ:  |
| A.处理工业废水中的Cu2+最佳点应选择c点 |
| B.bc段:随pH升高,Cu2+的量增加,平衡Ⅰ正向移动 |
C.cd段:随pH升高, 增大,再次有Cu(OH)2成 增大,再次有Cu(OH)2成 |
| D.d点以后,随pH升高,铜元素含量下降并保持不变 |
2023·广东汕头·三模 查看更多[2]
更新时间:2023-06-22 08:49:53
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列图示与对应的叙述相符的是( )
A.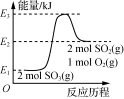 由图可知,2SO3(g)===2SO2(g)+O2(g) ΔH=(E1-E2)kJ·mol-1 由图可知,2SO3(g)===2SO2(g)+O2(g) ΔH=(E1-E2)kJ·mol-1 |
B.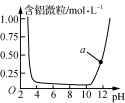 表示Al3+与OH-反应时溶液中含铝微粒浓度变化曲线,a点溶液中存在大量Al3+ 表示Al3+与OH-反应时溶液中含铝微粒浓度变化曲线,a点溶液中存在大量Al3+ |
C.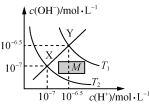 温度在T1和T2时水溶液中c(H+)和c(OH-)的关系,则阴影部分M内任意一点均满足c(H+)>c(OH-) 温度在T1和T2时水溶液中c(H+)和c(OH-)的关系,则阴影部分M内任意一点均满足c(H+)>c(OH-) |
D.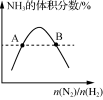 表示反应N2(g)+3H2(g)=2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2) 表示反应N2(g)+3H2(g)=2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】I2在KI溶液中存在下列平衡:I2(aq)+I—(aq) I3—(aq)。某I2、KI混合溶液中,I3—的物质的量浓度c(I3—)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法都正确的是
I3—(aq)。某I2、KI混合溶液中,I3—的物质的量浓度c(I3—)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法都正确的是
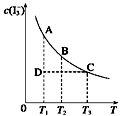
①反应I2(aq) +I—(aq) I3—(aq)的
I3—(aq)的 H>0
H>0
②若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2
③若反应进行到状态D时,一定有v正>v逆
④状态A与状态B相比,状态A的c(I2)大
⑤保持温度不变,在该混合液中加水,c(I3—)/c(I2)将变大
 I3—(aq)。某I2、KI混合溶液中,I3—的物质的量浓度c(I3—)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法都正确的是
I3—(aq)。某I2、KI混合溶液中,I3—的物质的量浓度c(I3—)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法都正确的是
①反应I2(aq) +I—(aq)
 I3—(aq)的
I3—(aq)的 H>0
H>0②若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2
③若反应进行到状态D时,一定有v正>v逆
④状态A与状态B相比,状态A的c(I2)大
⑤保持温度不变,在该混合液中加水,c(I3—)/c(I2)将变大
| A.只有①② | B.只有②③ | C.②③④ | D.②③⑤ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】黏土钒矿中,钒以+3、+4、+5价的化合物形式存在,还包括钾、镁和铝的硅酸盐,以及 、
、 等。采用以下工艺流程可由黏土钒矿制备
等。采用以下工艺流程可由黏土钒矿制备 。
。
已知:“中和沉淀”中, 水解并沉淀为
水解并沉淀为 。“沉淀转溶”中,
。“沉淀转溶”中, 转化为钒酸盐溶解。
转化为钒酸盐溶解。
下列说法错误的是
 、
、 等。采用以下工艺流程可由黏土钒矿制备
等。采用以下工艺流程可由黏土钒矿制备 。
。
| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 1.9 | 7.0 | 8.9 | 3.0 | 8.1 |
| 完全沉淀的pH | 3.2 | 9.0 | 10.9 | 4.7 | 10.1 |
 水解并沉淀为
水解并沉淀为 。“沉淀转溶”中,
。“沉淀转溶”中, 转化为钒酸盐溶解。
转化为钒酸盐溶解。下列说法错误的是
A.“酸浸氧化”中,有 、 、 、 、 三种离子被氧化 三种离子被氧化 |
B.滤渣①、滤渣③、滤渣④的主要成分依次是 、 、 、 、 |
C.随滤液②可除去金属离子 、 、 、 、 、 、 及部分 及部分 、 、 |
D.“沉钒”中需要加入过量 ,利用同离子效应,促进 ,利用同离子效应,促进 尽可能析出完全 尽可能析出完全 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】已知常温下AgCl和AgBr的溶解度分别为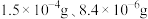 ,将AgCl与AgBr的饱和溶液等体积混合,再加入足量
,将AgCl与AgBr的饱和溶液等体积混合,再加入足量 溶液,发生的反应为
溶液,发生的反应为
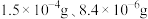 ,将AgCl与AgBr的饱和溶液等体积混合,再加入足量
,将AgCl与AgBr的饱和溶液等体积混合,再加入足量 溶液,发生的反应为
溶液,发生的反应为| A.只有AgBr沉淀生成 | B.AgCl和AgBr沉淀等量生成 |
| C.AgCl沉淀多于AgBr沉淀 | D.AgCl沉淀少于AgBr沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】298K时含大量 固体的溶液中离子浓度关系如图所示。
固体的溶液中离子浓度关系如图所示。

已知:298K时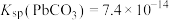 ,
, 固体溶解吸热。
固体溶解吸热。
下列说法正确的是
 固体的溶液中离子浓度关系如图所示。
固体的溶液中离子浓度关系如图所示。
已知:298K时
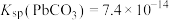 ,
, 固体溶解吸热。
固体溶解吸热。下列说法正确的是
| A.T小于298K,e点溶液中阴阳离子浓度相等 |
B.298K时碳酸铅的溶解度约为 g g |
| C.向d点浊液中滴加几滴蒸馏水,溶液由d点向f点迁移 |
D.298K时,向d点浊液加少量 ,溶液由d点向e点迁移 ,溶液由d点向e点迁移 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】氯化银(AgCl,白色)、铬酸银( ,砖红色)都是难溶电解质。T℃下,将
,砖红色)都是难溶电解质。T℃下,将 溶液分别逐滴滴入体积均为10mL、浓度均为
溶液分别逐滴滴入体积均为10mL、浓度均为 的NaCl溶液和
的NaCl溶液和 溶液中,所得的沉淀溶解平衡图像如图所示(X为
溶液中,所得的沉淀溶解平衡图像如图所示(X为 或
或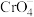 )。下列叙述正确的是
)。下列叙述正确的是
 ,砖红色)都是难溶电解质。T℃下,将
,砖红色)都是难溶电解质。T℃下,将 溶液分别逐滴滴入体积均为10mL、浓度均为
溶液分别逐滴滴入体积均为10mL、浓度均为 的NaCl溶液和
的NaCl溶液和 溶液中,所得的沉淀溶解平衡图像如图所示(X为
溶液中,所得的沉淀溶解平衡图像如图所示(X为 或
或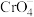 )。下列叙述正确的是
)。下列叙述正确的是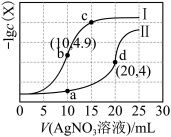
A.T℃下,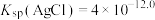 |
B.曲线Ⅱ表示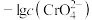 与V( 与V( 溶液)的变化关系 溶液)的变化关系 |
| C.向a点对应的体系中加入少量NaCl固体,白色固体逐渐变为砖红色 |
D.浓度均为 的 的 和 和 ,可通过分步沉淀进行分离 ,可通过分步沉淀进行分离 |
您最近一年使用:0次

 Y(g)+2Z(g),达到平衡后改变下述条件,气体Z的平衡浓度不变的是(
Y(g)+2Z(g),达到平衡后改变下述条件,气体Z的平衡浓度不变的是(
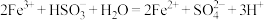
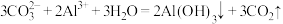
 ):
):