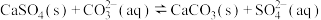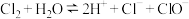科学探究是化学学科核心素养之一,下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 相同条件下,分别测量 和 和 '醋酸溶液的导电性,前者的导电性强 '醋酸溶液的导电性,前者的导电性强 | 醋酸浓度越大,电离程度越大 |
| B |  溶液蒸干灼烧后得到红色固体 溶液蒸干灼烧后得到红色固体 | 固体成分是 |
| C | 向 和 和 混合溶液中,加入少量 混合溶液中,加入少量 的固体,溶液颜色无变化。 的固体,溶液颜色无变化。 | 改变离子浓度不会引起平衡移动 |
| D | 向盛有2mL0.1mol/L 溶液中滴加2滴0.1mol/L 溶液中滴加2滴0.1mol/L 溶液,得白色沉淀,再向其中加4滴0.1mol/L 溶液,得白色沉淀,再向其中加4滴0.1mol/L 溶液,沉淀转化为黄色 溶液,沉淀转化为黄色 | 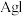 的 的 比 比 的大 的大 |
| A.A | B.B | C.C | D.D |
更新时间:2023-07-30 19:30:58
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在25℃时,下列关于水及水溶液的说法不正确 的是
A.0.02 mol/L氨水中 mol/L,则由水电离出的 mol/L,则由水电离出的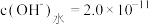 mol/L mol/L |
| B.向醋酸溶液中滴加同浓度的NaOH溶液至过量,水的电离程度先增大后减小 |
C. 的 的 和 和 的氨水等体积混合后溶液呈碱性 的氨水等体积混合后溶液呈碱性 |
D.NaR溶液 ,升温至50℃,测得 ,升温至50℃,测得 ,若 ,若 ,则HR是弱酸 ,则HR是弱酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,下列各组离子在指定溶液中一定能大量共存的是
A.常温下 =10-12的溶液:K+、Ba2+、Cl-、Br- =10-12的溶液:K+、Ba2+、Cl-、Br- |
B.在含有大量Al3+溶液中: 、Na+、Cl-、 、Na+、Cl-、 |
C.常温下pH=7的溶液中:Na+、Cl-、 、Fe3+ 、Fe3+ |
D.常温下由水电离产生的c(OH-)=10-12mol•L-1的溶液:K+、Al3+、Cl-、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】25℃时,相同体积和pH的CH3COONa、NaCN两种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示,已知:K(CH3COOH)>K(HCN)。下列说法正确的是
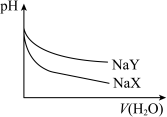

| A.图中曲线NaY代表的是NaCN溶液 |
| B.上述两种盐原溶液中水的电离度大小是NaCN>CH3COONa |
| C.上述两种盐原溶液中存在:c(CH3COOH)+c(CH3COO–)=c(HCN)+c(CN–) |
| D.在0.2mol·L-1 NaX溶液中加入等体积0.1mol·L-1的盐酸,所得混合液中存在c(H+)+c(HX)=c(OH-)+c(Cl-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】由下列实验及现象推出的相应结论正确的是
选项 | 实验 | 现象 | 结论 |
A | 某溶液中滴加K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 原溶液中有Fe2+,无Fe3+ |
B | 将10 mL 2 mol·L-1的KI溶液与1 mL 1 mol·L-1FeCl3溶液混合充分反应后滴加KSCN溶液 | 溶液颜色变红 | KI与FeCl3的反应有可逆性 |
C | 向含有ZnS和Na2S的悬浊液中滴加CuSO4溶液 | 生成黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
D | ①某溶液中加入Ba(NO3)2溶液 ②再加足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 检验 中是否混有HCl 中是否混有HCl | 将气体通入 溶液 溶液 |
| B | 检验乙醇消去反应的产物 | 加热乙醇与浓硫酸的混合液,将产生的气体通入酸性 溶液 溶液 |
| C | 除去乙酸乙酯中少量的乙酸 | 向混合液中加入饱和 溶液,充分振荡,静置,分液 溶液,充分振荡,静置,分液 |
| D | 比较AgCl和AgI的溶解度 | 向2mL 溶液中加入0.5mL 溶液中加入0.5mL NaCl溶液,振荡后再加入0.5mL NaCl溶液,振荡后再加入0.5mL KI溶液 KI溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次