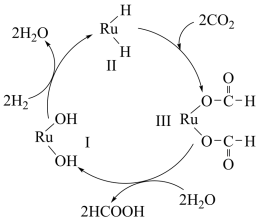
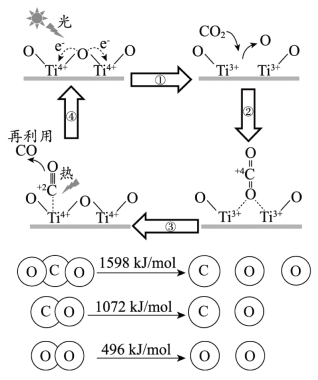
最近科学家在发展非金属催化剂实现CO2电催化还原制备甲醇(CH3OH)方向取得重要进展,反应历程如图所示,其中吸附在催化剂表面上的物质用“*”标注。下列说法正确的是
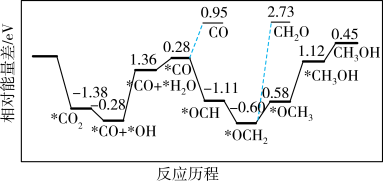

| A.得到的副产物有CO和CH2O(甲醛),其中相对较多的副产物为CH2O(甲醛) |
| B.生成副产物CH2O时,反应的活化能较小 |
| C.制备甲醇的主反应速率主要由过程*CO+*OH→*CO+*H2O决定 |
| D.电催化还原制备甲醇过程中,阳极的电势比阴极电势低 |
更新时间:2023-08-20 07:51:32
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】如图所示,相同温度下,在容器Ⅰ和Ⅱ中分别充入等物质的量的HI,发生反应2HI(g)  H2(g)+I2(g)。下列关于反应起始时容器Ⅰ和Ⅱ中活化分子的说法不正确的是
H2(g)+I2(g)。下列关于反应起始时容器Ⅰ和Ⅱ中活化分子的说法不正确的是
 H2(g)+I2(g)。下列关于反应起始时容器Ⅰ和Ⅱ中活化分子的说法不正确的是
H2(g)+I2(g)。下列关于反应起始时容器Ⅰ和Ⅱ中活化分子的说法不正确的是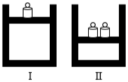
| A.Ⅰ和Ⅱ中活化分子数相同 |
| B.Ⅰ和Ⅱ中活化分子百分数相同 |
| C.Ⅰ和Ⅱ中单位体积内活化分子数相等 |
| D.Ⅰ中化学反应速率比Ⅱ中的小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】关于有效碰撞理论,下列说法正确的是
| A.分子间所发生的碰撞均为有效碰撞 |
| B.活化分子具有的能量就是活化能 |
| C.增大压强,活化分子数一定增加,化学反应速率一定加快 |
| D.升高温度可以加快化学反应速率,原因之一是提高了活化分子百分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在恒容条件下,能使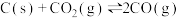 正反应速率增大且活化分子的数目也增大的措施是
正反应速率增大且活化分子的数目也增大的措施是
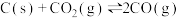 正反应速率增大且活化分子的数目也增大的措施是
正反应速率增大且活化分子的数目也增大的措施是A.温度不变,增大 的浓度 的浓度 | B.加入固体碳 |
C.温度不变,通入 使气体的压强增大 使气体的压强增大 | D.降低反应的温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
A.向某溶液中滴加硝酸酸化的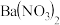 溶液,有白色沉淀生成,则原溶液中一定含有 溶液,有白色沉淀生成,则原溶液中一定含有 |
| B.合成氨工业中,使用铁触媒作催化剂,目的是打破原有平衡状态,从而建立新的平衡,提高氨气的产率 |
C.少量的 加入到过量的 加入到过量的 溶液中,充分振荡,再滴入 溶液中,充分振荡,再滴入 溶液,溶液无现象 溶液,溶液无现象 |
| D.合成氨工业的成功,改变了世界粮食生产的历史,使人类免受饥荒之苦 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】资料显示:自催化作用是指反应产物之一使该反应速率加快的作用。用稀硫酸酸化的KMnO4溶液进行下列三组实验,一段时间后溶液均褪色(0.01mol/L可以记做0.01M)。
下列说法不正确的是( )
| 实验① | 实验② | 实验③ |
 | 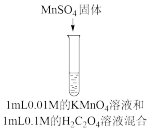 | 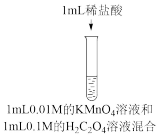 |
| 褪色 | 比实验①褪色快 | 比实验①褪色快 |
| A.实验①中发生氧化还原反应,H2C2O4是还原剂,产物MnSO4能起自催化作用 |
| B.实验③褪色比实验①快,是因为Cl-起催化作用加快了反应速率 |
| C.实验②褪色比实验①快,是因为MnSO4的催化作用加快了反应速率 |
| D.若用1mL0.2M的H2C2O4,做实验①,推测比实验①褪色快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列关于反应方向、速率和平衡的说法正确的是
| A.凡是放热反应均是自发进行的反应,吸热反应都是非自发的 |
| B.化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| C.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率 |
| D.反应NH3(g)+HCl(g)=NH4Cl(s)在常温下能自发进行,说明该反应的ΔH<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不正确的是
| A | B | C | D |
| 通电一段时间后, 搅拌均匀,溶液的 pH增大 | 甲电极上的电极反应为: 2Cl--2e-= Cl2↑ | Pt电极上的电极反应为: O2+2H2O+4e-==4OH- | 总反应的离子方程式 为:2Fe3++Cu=Cu2++ 2Fe2+ |
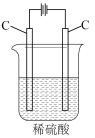 | 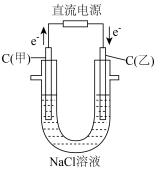 | 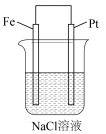 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】CuI是一种不溶于水的白色固体,它可由反应2Cu2++4I-=2CuI+I2而得到。现以石墨为阴极,以Cu为阳极电解KI溶液,通电前向电解液中加入少量酚酞和淀粉溶液。电解开始不久阴极区溶液呈红色,而阳极区溶液呈蓝色,对这些现象的正确解释是
①阳极4OH--4e-=2H2O+O2↑,O2将I-氧化为I2,I2遇淀粉变蓝 ②阳极2I--2e-=I2,I2遇淀粉变蓝 ③阳极2Cu-4e-+4I-=2CuI+I2,I2遇淀粉变蓝 ④阴极2H++2e-= H2↑,使c(OH-)>c(H+)
①阳极4OH--4e-=2H2O+O2↑,O2将I-氧化为I2,I2遇淀粉变蓝 ②阳极2I--2e-=I2,I2遇淀粉变蓝 ③阳极2Cu-4e-+4I-=2CuI+I2,I2遇淀粉变蓝 ④阴极2H++2e-= H2↑,使c(OH-)>c(H+)
| A.①② | B.①③ | C.②④ | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用石墨作电极电解溶有物质的量之比为3:1的NaCl和H2SO4的水溶液。根据反应产物,电解可明显分为三个阶段,下列叙述错误的是
| A.第一阶段为电解HCl溶液,阳极电极反应式为2Cl--2e-=Cl2↑ |
| B.第二阶段为电解NaCl溶液,阴极电极反应式为2H2O+2e-=2OH-+H2↑ |
| C.第三阶段为电解H2O,阳极电极反应式为2H2O-4e-=4H++O2↑ |
| D.三个阶段的阴极反应式均为2H++2e-=H2↑,电解过程中溶液的pH不断减小 |
您最近一年使用:0次

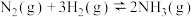 ]是人类科学技术的一项重大突破。已知:工业合成氨的主要设备是反应塔;合成氨反应的速率方程为
]是人类科学技术的一项重大突破。已知:工业合成氨的主要设备是反应塔;合成氨反应的速率方程为 (k为速率常数,与温度、催化剂有关,与浓度无关)。下列有关说法错误的是
(k为速率常数,与温度、催化剂有关,与浓度无关)。下列有关说法错误的是