 、CO、
、CO、 、
、 等都是重要的能源,也是重要为化工原料。
等都是重要的能源,也是重要为化工原料。(1)已知25℃,
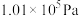 时,8.00g
时,8.00g  完全燃烧生成二氧化碳气体和液态水放出444.8kJ热量。写出该反应的热化学反应方程式:
完全燃烧生成二氧化碳气体和液态水放出444.8kJ热量。写出该反应的热化学反应方程式:(2)为倡导“节能减排”和“低碳经济”,降低大气中
 的含量及有效地开发利用
的含量及有效地开发利用 。工业可以用
。工业可以用 来生产燃料甲醇。在体积为2L的密闭容器中,充入1mol
来生产燃料甲醇。在体积为2L的密闭容器中,充入1mol  和3mol
和3mol  ,一定条件下发生反应:
,一定条件下发生反应:
 。经测定
。经测定 和
和 (g)的物质的量随时间变化如图所示。
(g)的物质的量随时间变化如图所示。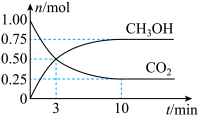
①从反应开始平衡时,
 的平均反应速率
的平均反应速率
②达到平衡时,
 的转化率为
的转化率为③下列措施不能提高反应速率的是
A.升高温度 B.加入催化剂
C.增大压强 D.及时分离出

(3)工业上也用
 和
和 为原料制备
为原料制备 ,反应方程式为:
,反应方程式为: ,在一体积固定的密闭容器中投入一定量的CO和
,在一体积固定的密闭容器中投入一定量的CO和 气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是A.反应中CO与
 的物质的量之比为1∶1
的物质的量之比为1∶1B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1mol CO,同时生成1mol

D.
 的质量分数在混合气体中保持不变
的质量分数在混合气体中保持不变E.混合气体的密度保持不变
(4)燃料电池是一种高效、环境友好的供电装置,如图为乙醇燃料电池的工作原理示意图,a、b均为惰性电极。

①使用时,空气从口通入
②a极的电极反应为:
更新时间:2023-09-04 07:17:11
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】X、Y、Z、W代表原子序数依次增大的四种短周期元素,X原子核内没有中子,在周期表中,Z与Y﹑W均相邻,Y﹑Z和W三种元素的原子最外层电子数之和为17,且Z﹑W最外层电子数相同。
(1)用电子式表示X与Y所组成化合物的形成过程_________________ 。
(2)W在周期表中的位置是____________________ 。
(3)已知,在101kPa时,X单质在1.00molO2中完全燃烧生成2.00mol液态H2O,放出571.6kJ的热量,则表示X单质燃烧热的热化学方程式为__________ 。
(1)用电子式表示X与Y所组成化合物的形成过程
(2)W在周期表中的位置是
(3)已知,在101kPa时,X单质在1.00molO2中完全燃烧生成2.00mol液态H2O,放出571.6kJ的热量,则表示X单质燃烧热的热化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】完成下列问题。
(1)节能减排是当今社会的热门话题,研发混合动力汽车对于中国汽车业的未来具有重要的战略意义。混合动力汽车持续工作时间长,动力性好的优点,无污染、低噪声的好处,汽车的热效率可提高10%以上,废气排放可改善30%以上,某种混合动力汽车的动力系统由“1.6L汽油机+自动变速器+20kW+200V镍氢电池”组成。
①混合动力汽车所用的燃料之一是乙醇,lg乙醇完全燃烧生成CO2气体和液态H2O放出30.0kJ热量,写出乙醇燃烧的燃烧热的热化学方程式_______ 。
②镍氢电池的使用可以减少对环境的污染,它采用储氢金属为负极,碱液NaOH为电解液,镍氢电池充电时发生反应Ni(OH)2=NiO(OH)+ H2。其放电时的正极的电极反应方程式为
H2。其放电时的正极的电极反应方程式为_______ 。
(2)二氧化锰、锌是制备干电池的重要原料,工业上用软锰矿(含MnO2)和闪锌矿(含ZnS)联合生产二氧化锰、锌的工艺如下:
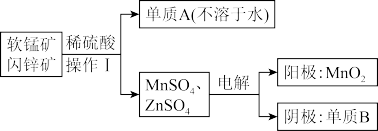
①操作I需要的玻璃仪器是_______ 。
②软锰矿(含MnO2)和闪锌矿与硫酸反应的化学方程式为_______ ,上述电解过程中,当阴极生成6.5gB时,阳极生成的MnO2的质量为_______ 。
③利用铝热反应原理,可以从软锰矿中提取锰,发生的化学方程式为_______ 。
(1)节能减排是当今社会的热门话题,研发混合动力汽车对于中国汽车业的未来具有重要的战略意义。混合动力汽车持续工作时间长,动力性好的优点,无污染、低噪声的好处,汽车的热效率可提高10%以上,废气排放可改善30%以上,某种混合动力汽车的动力系统由“1.6L汽油机+自动变速器+20kW+200V镍氢电池”组成。
①混合动力汽车所用的燃料之一是乙醇,lg乙醇完全燃烧生成CO2气体和液态H2O放出30.0kJ热量,写出乙醇燃烧的燃烧热的热化学方程式
②镍氢电池的使用可以减少对环境的污染,它采用储氢金属为负极,碱液NaOH为电解液,镍氢电池充电时发生反应Ni(OH)2=NiO(OH)+
 H2。其放电时的正极的电极反应方程式为
H2。其放电时的正极的电极反应方程式为(2)二氧化锰、锌是制备干电池的重要原料,工业上用软锰矿(含MnO2)和闪锌矿(含ZnS)联合生产二氧化锰、锌的工艺如下:

①操作I需要的玻璃仪器是
②软锰矿(含MnO2)和闪锌矿与硫酸反应的化学方程式为
③利用铝热反应原理,可以从软锰矿中提取锰,发生的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】工业制硫酸的流程如图所示:
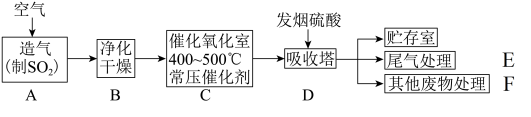
(1)早期以硫铁矿为原料造气,方程式为4FeS2+11O2 2Fe2O3+8SO2。若消耗了12gFeS2,上述反应有
2Fe2O3+8SO2。若消耗了12gFeS2,上述反应有___ mol电子发生了转移。
(2)如今大量改用固体硫为原料,同时生产过程中送入过量的空气,该改进从“减少污染物的排放”和___ 两个方面体现“绿色化学”。
(3)硫酸厂尾气处理的流程如图:
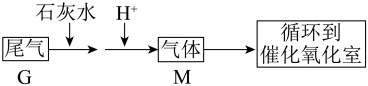
G的主要成分和M一样,如此处理的目的是___ ,将尾气G通入足量澄清石灰水,主要反应的离子方程式为___ 。
(4)如果C装置中生成0.1molSO3气体,可放出9.83kJ的热量。则该反应的热化学方程式为___ 。
(5)其他废弃物F中可能含有砷元素(As3+),处理工艺过程是在含砷废水中加入一定数量的硫酸亚铁,然后加碱调pH至8.5~9.0,反应温度90℃,鼓风氧化,废水中的砷、铁以砷酸铁(FeAsO4)沉淀析出,写出该过程的离子方程式___ 。

(1)早期以硫铁矿为原料造气,方程式为4FeS2+11O2
 2Fe2O3+8SO2。若消耗了12gFeS2,上述反应有
2Fe2O3+8SO2。若消耗了12gFeS2,上述反应有(2)如今大量改用固体硫为原料,同时生产过程中送入过量的空气,该改进从“减少污染物的排放”和
(3)硫酸厂尾气处理的流程如图:

G的主要成分和M一样,如此处理的目的是
(4)如果C装置中生成0.1molSO3气体,可放出9.83kJ的热量。则该反应的热化学方程式为
(5)其他废弃物F中可能含有砷元素(As3+),处理工艺过程是在含砷废水中加入一定数量的硫酸亚铁,然后加碱调pH至8.5~9.0,反应温度90℃,鼓风氧化,废水中的砷、铁以砷酸铁(FeAsO4)沉淀析出,写出该过程的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】化学研究的物质多种多样,按要求回答下列问题:
(1)过二硫酸钠( )可以看成过氧化氢的衍生物,
)可以看成过氧化氢的衍生物, 分子中的两个H原子被磺酸基(
分子中的两个H原子被磺酸基(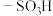 )取代后即为过二硫酸。
)取代后即为过二硫酸。
① 中硫元素的化合价为
中硫元素的化合价为_______ 。
②用 溶液可以检测废水中的
溶液可以检测废水中的 ,含有
,含有 的废水加入
的废水加入 溶液后会变为紫红色,
溶液后会变为紫红色, 被还原为稳定的
被还原为稳定的 。发生上述反应的氧化剂与还原剂的物质的量之比为
。发生上述反应的氧化剂与还原剂的物质的量之比为_______ 。
(2)硫代硫酸钠( )又名大苏打,造纸工业用作纸浆漂白后的除氯剂。
)又名大苏打,造纸工业用作纸浆漂白后的除氯剂。
① 在中性与碱性溶液中很稳定,遇酸则迅速反应。
在中性与碱性溶液中很稳定,遇酸则迅速反应。 溶液中加入稀硫酸时反应的离子方程式为
溶液中加入稀硫酸时反应的离子方程式为_______ 。
② 常用于防毒面具中吸收
常用于防毒面具中吸收 。若1 mol
。若1 mol  完全反应,失去8 mol电子,则其水溶液吸收
完全反应,失去8 mol电子,则其水溶液吸收 的离子方程式为
的离子方程式为_______ 。
(3)在室温下,化学反应 的反应物初始浓度、溶液中的
的反应物初始浓度、溶液中的 初始浓度及初始速率间的关系如下表所示。
初始浓度及初始速率间的关系如下表所示。
已知表中初始反应速率与有关离子浓度关系可以表示为: (温度一定时,k为常数)
(温度一定时,k为常数)
(1)计算b、c的值:b=_______ ,c=_______ 。
(2)若实验编号4的其他浓度不变,仅将溶液的酸碱值变更为 ,反应的初始速率v=
,反应的初始速率v=_______ mol⋅L ⋅s
⋅s 。
。
(1)过二硫酸钠(
 )可以看成过氧化氢的衍生物,
)可以看成过氧化氢的衍生物, 分子中的两个H原子被磺酸基(
分子中的两个H原子被磺酸基(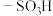 )取代后即为过二硫酸。
)取代后即为过二硫酸。①
 中硫元素的化合价为
中硫元素的化合价为②用
 溶液可以检测废水中的
溶液可以检测废水中的 ,含有
,含有 的废水加入
的废水加入 溶液后会变为紫红色,
溶液后会变为紫红色, 被还原为稳定的
被还原为稳定的 。发生上述反应的氧化剂与还原剂的物质的量之比为
。发生上述反应的氧化剂与还原剂的物质的量之比为(2)硫代硫酸钠(
 )又名大苏打,造纸工业用作纸浆漂白后的除氯剂。
)又名大苏打,造纸工业用作纸浆漂白后的除氯剂。①
 在中性与碱性溶液中很稳定,遇酸则迅速反应。
在中性与碱性溶液中很稳定,遇酸则迅速反应。 溶液中加入稀硫酸时反应的离子方程式为
溶液中加入稀硫酸时反应的离子方程式为②
 常用于防毒面具中吸收
常用于防毒面具中吸收 。若1 mol
。若1 mol  完全反应,失去8 mol电子,则其水溶液吸收
完全反应,失去8 mol电子,则其水溶液吸收 的离子方程式为
的离子方程式为(3)在室温下,化学反应
 的反应物初始浓度、溶液中的
的反应物初始浓度、溶液中的 初始浓度及初始速率间的关系如下表所示。
初始浓度及初始速率间的关系如下表所示。| 实验编号 |  的初始浓度(mol⋅L 的初始浓度(mol⋅L ) ) |  的初始浓度(mol⋅L 的初始浓度(mol⋅L ) ) |  的初始浓度(mol⋅L 的初始浓度(mol⋅L ) ) | 初始速率ν(mol⋅L ⋅s ⋅s ) ) |
| 1 |  |  | 1.00 |  |
| 2 | a |  | 1.00 |  |
| 3 |  | 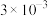 | 2.00 |  |
| 4 | 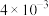 | 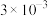 | 1.00 | 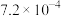 |
已知表中初始反应速率与有关离子浓度关系可以表示为:
 (温度一定时,k为常数)
(温度一定时,k为常数)(1)计算b、c的值:b=
(2)若实验编号4的其他浓度不变,仅将溶液的酸碱值变更为
 ,反应的初始速率v=
,反应的初始速率v= ⋅s
⋅s 。
。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】Ⅰ.氨气被广泛用于化工、轻工、化肥、合成纤维、制药等领域,已知工业合成氨的反应为 +3H2(g)
+3H2(g) 2NH3(g)。气态分子中1mol化学键解离成气态原子所吸收的能量称为键能(
2NH3(g)。气态分子中1mol化学键解离成气态原子所吸收的能量称为键能( ),一些共价键的键能如下表所示。
),一些共价键的键能如下表所示。
(1)请根据上表数据计算,一定条件下,氮气与氢气生成2mol氨气时___________ (填“放出”或“吸收”)的热量为 ,则
,则 为
为___________ kJ。
(2)在与(1)相同条件下,将1 mol氮气和3 mol氢气放入一密闭容器中发生上述反应,放出或吸收的热量为 ,则
,则 与
与 比较,正确的是
比较,正确的是___________ (填字母)。
A.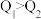 B.
B. C.
C.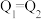
Ⅱ.一定条件下铁可以和 发生反应:
发生反应: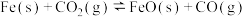 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和CO气体的浓度与时间的关系如图所示。
气体和CO气体的浓度与时间的关系如图所示。

(3) min时,正、逆反应速率的大小关系为
min时,正、逆反应速率的大小关系为
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)4min内,CO的平均反应速率
___________ 。
(5)下列条件的改变能减慢其反应速率的是___________ (填序号)。
①降低温度
②减小铁粉的质量
③保持压强不变,充入He使容器的容积增大
④保持容积不变,充入He便体系压强增大
(6)下列描述能说明上述反应已达到平衡状态的是___________ (填序号)。
①
②单位时间内生成n mol ,的同时生成n mol CO
,的同时生成n mol CO
③容器中气体压强不随时间变化而变化
⑥容器中气体的平均相对分子质量不随时间变化而变化
(7)燃料电池是燃料(如CO、 、
、 等)跟氧气(或空气)反应将化学能转变成电能的装置,若电解质溶液是强碱溶液,下列关于一氧化碳燃料电池的说法正确的是___________(填字母)。
等)跟氧气(或空气)反应将化学能转变成电能的装置,若电解质溶液是强碱溶液,下列关于一氧化碳燃料电池的说法正确的是___________(填字母)。
 +3H2(g)
+3H2(g) 2NH3(g)。气态分子中1mol化学键解离成气态原子所吸收的能量称为键能(
2NH3(g)。气态分子中1mol化学键解离成气态原子所吸收的能量称为键能( ),一些共价键的键能如下表所示。
),一些共价键的键能如下表所示。| 共价键 |  |  |  |
键能/( ) ) | 436 | 946 | 391 |
 ,则
,则 为
为(2)在与(1)相同条件下,将1 mol氮气和3 mol氢气放入一密闭容器中发生上述反应,放出或吸收的热量为
 ,则
,则 与
与 比较,正确的是
比较,正确的是A.
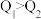 B.
B. C.
C.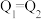
Ⅱ.一定条件下铁可以和
 发生反应:
发生反应: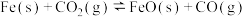 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和CO气体的浓度与时间的关系如图所示。
气体和CO气体的浓度与时间的关系如图所示。
(3)
 min时,正、逆反应速率的大小关系为
min时,正、逆反应速率的大小关系为
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)4min内,CO的平均反应速率

(5)下列条件的改变能减慢其反应速率的是
①降低温度
②减小铁粉的质量
③保持压强不变,充入He使容器的容积增大
④保持容积不变,充入He便体系压强增大
(6)下列描述能说明上述反应已达到平衡状态的是
①

②单位时间内生成n mol
 ,的同时生成n mol CO
,的同时生成n mol CO③容器中气体压强不随时间变化而变化
⑥容器中气体的平均相对分子质量不随时间变化而变化
(7)燃料电池是燃料(如CO、
 、
、 等)跟氧气(或空气)反应将化学能转变成电能的装置,若电解质溶液是强碱溶液,下列关于一氧化碳燃料电池的说法正确的是___________(填字母)。
等)跟氧气(或空气)反应将化学能转变成电能的装置,若电解质溶液是强碱溶液,下列关于一氧化碳燃料电池的说法正确的是___________(填字母)。A.正极反应式: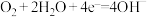 |
B.负极反应式: |
| C.随着放电的进行,溶液中氢氧根离子浓度保持不变 |
| D.放电时溶液中的阴离子向负极移动 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.恒温下,在容积为2L的恒容密闭容器A中通入1mol 与1mol
与1mol 的混合气体,发生如下反应:
的混合气体,发生如下反应:
 ,5min时,达到平衡,若平衡时氢气的物质的量为0.4mol
,5min时,达到平衡,若平衡时氢气的物质的量为0.4mol
(1)平衡时 的速率为
的速率为_______ 。
(2)此温度时该反应的平衡常数为_______ 。
(3)平衡时与起始时压强之比_______ 。
(4)该反应在什么温度下_______ (填“高温”“低温”“任何温度”)自发进行。
Ⅱ.在一定容积的密闭容器中,进行如下化学反应 ,其化学平衡常数K和温度T的关系如表:
,其化学平衡常数K和温度T的关系如表:
(5)800℃在恒容密闭容器中放入混合物,各物质的浓度为 ,
, ,
, ,
, ,此时
,此时
_______  (填“=”“>”“<”或“不能确定”),该反应正反应为
(填“=”“>”“<”或“不能确定”),该反应正反应为_______ 热。
 与1mol
与1mol 的混合气体,发生如下反应:
的混合气体,发生如下反应:
 ,5min时,达到平衡,若平衡时氢气的物质的量为0.4mol
,5min时,达到平衡,若平衡时氢气的物质的量为0.4mol(1)平衡时
 的速率为
的速率为(2)此温度时该反应的平衡常数为
(3)平衡时与起始时压强之比
(4)该反应在什么温度下
Ⅱ.在一定容积的密闭容器中,进行如下化学反应
 ,其化学平衡常数K和温度T的关系如表:
,其化学平衡常数K和温度T的关系如表:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
 ,
, ,
, ,
, ,此时
,此时
 (填“=”“>”“<”或“不能确定”),该反应正反应为
(填“=”“>”“<”或“不能确定”),该反应正反应为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】人们通过化学方法可以开辟新能源和提高能源的利用率,根据情景回答下列问题:
(1)工业合成氨反应 是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成
是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成 (g)可放出92kJ热量。如果将0.5mol
(g)可放出92kJ热量。如果将0.5mol (g)和足量
(g)和足量 (g)混合,使其充分反应,放出的热量
(g)混合,使其充分反应,放出的热量___________ (填“大于”“小于”或“等于”)46kJ。
(2)在容积为5L的密闭容器内模拟工业合成氨,反应经过5min后,生成10mol
①用 表示的化学反应速率为
表示的化学反应速率为___________ 
②一定条件下,能说明该反应进行到最大限度的是___________ 。
a. 的转化率达到最大值
的转化率达到最大值
b. 、
、 和
和 的分子数之比为
的分子数之比为
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
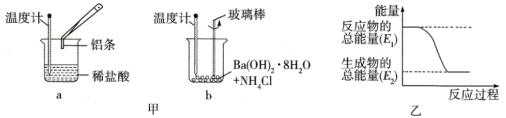
(3)某实验小组进行如图甲所示实验。请判断b中的温度___________ (填“升高”或“降低”)。反应过程___________ (填“a”或“b”)的能量变化可用图乙表示。
(4)用 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:

①电极c是___________ (填“正极”或“负极”),电极d的电极反应式为___________ 。
②若线路中转移1mol电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(1)工业合成氨反应
 是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成
是放热的可逆反应。已知1mol高温高压N2(g)完全反应生成 (g)可放出92kJ热量。如果将0.5mol
(g)可放出92kJ热量。如果将0.5mol (g)和足量
(g)和足量 (g)混合,使其充分反应,放出的热量
(g)混合,使其充分反应,放出的热量(2)在容积为5L的密闭容器内模拟工业合成氨,反应经过5min后,生成10mol

①用
 表示的化学反应速率为
表示的化学反应速率为
②一定条件下,能说明该反应进行到最大限度的是
a.
 的转化率达到最大值
的转化率达到最大值b.
 、
、 和
和 的分子数之比为
的分子数之比为
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
(3)某实验小组进行如图甲所示实验。请判断b中的温度

(4)用
 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
①电极c是
②若线路中转移1mol电子,则该燃料电池理论上消耗的
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、CO、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
(1)I.脱硝:已知:H2的燃烧热为285.8 kJ/mol
N2(g)+2O2(g)=2NO2(g) H= +133 kJ/mol
H= +133 kJ/mol
H2O(g)=H2O(l) H=- 44 kJ/mol
H=- 44 kJ/mol
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为___________ 。
(2)II.脱碳:
向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在适当的催化剂作用下,发生反应 CO2(g) + 3H2(g) =CH3OH(l) + H2O(l)。下列叙述能说明此反应达到平衡状态的是___________ 。
A.混合气体的平均式量保持不变
B.CO2和H2的体积分数保持不变
C.CO2和H2的转化率相等
D.混合气体的密度保持不变
E.1 mol CO2生成的同时有3 mol H—H键断裂
(3)III.脱硫:
如图电解装置可将雾霾中的NO、SO2分别转化为NH 和SO
和SO 。物质A的化学式为
。物质A的化学式为___________ ,阴极的电极反应式是___________ 。
(1)I.脱硝:已知:H2的燃烧热为285.8 kJ/mol
N2(g)+2O2(g)=2NO2(g)
 H= +133 kJ/mol
H= +133 kJ/molH2O(g)=H2O(l)
 H=- 44 kJ/mol
H=- 44 kJ/mol催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为
(2)II.脱碳:
向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在适当的催化剂作用下,发生反应 CO2(g) + 3H2(g) =CH3OH(l) + H2O(l)。下列叙述能说明此反应达到平衡状态的是
A.混合气体的平均式量保持不变
B.CO2和H2的体积分数保持不变
C.CO2和H2的转化率相等
D.混合气体的密度保持不变
E.1 mol CO2生成的同时有3 mol H—H键断裂
(3)III.脱硫:
如图电解装置可将雾霾中的NO、SO2分别转化为NH
 和SO
和SO 。物质A的化学式为
。物质A的化学式为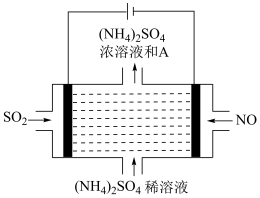
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】工业上处理含CO、SO2烟道气的一种方法是将其在催化剂作用下转化为S和CO2。
已知:①2CO(g)+O2(g)=2CO2(g) △H1=-566kJ•mol-1平衡常数K1。
②S(s)+O2(g)=SO2(g) △H2=-296kJ•mol-1平衡常数K2。
回答下面问题:
(1)CO(g)、SO2(g)烟道气在催化剂作用下转化为S(s)和CO2(g)的热化学方程式为:2CO(g)+SO2(g) S(s)+2CO2(g)△H=
S(s)+2CO2(g)△H=____ kJ•mol-1,平衡常数K=____ (用K1、K2表示)。
(2)向密闭容器中通入2molCO和1molO2发生反应①,下列方法不能加快化学反应速率的是____ 。
(3)一定温度下,向5L某刚性容器中通入2molCO(g)和1molSO2(g),在催化剂作用下发生2CO(g)+SO2(g) S(s)+2CO2(g),10min后容器内气体压强不再变化,此时压强变为开始的
S(s)+2CO2(g),10min后容器内气体压强不再变化,此时压强变为开始的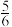 倍。
倍。
①10min后,反应是否达到化学平衡状态?____ (填“是”或“否”)。
②10min内,v(CO2)=____ mol•L-1•min-1。
③10min时,CO的转化率=____ %。
已知:①2CO(g)+O2(g)=2CO2(g) △H1=-566kJ•mol-1平衡常数K1。
②S(s)+O2(g)=SO2(g) △H2=-296kJ•mol-1平衡常数K2。
回答下面问题:
(1)CO(g)、SO2(g)烟道气在催化剂作用下转化为S(s)和CO2(g)的热化学方程式为:2CO(g)+SO2(g)
 S(s)+2CO2(g)△H=
S(s)+2CO2(g)△H=(2)向密闭容器中通入2molCO和1molO2发生反应①,下列方法不能加快化学反应速率的是
| A.采用较高的温度 |
| B.若容器体积不变,通入N2,增大压强 |
| C.采用合适的催化剂 |
| D.若容器体积可变,在气体物质的量不变时,缩小容器体积 |
 S(s)+2CO2(g),10min后容器内气体压强不再变化,此时压强变为开始的
S(s)+2CO2(g),10min后容器内气体压强不再变化,此时压强变为开始的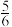 倍。
倍。①10min后,反应是否达到化学平衡状态?
②10min内,v(CO2)=
③10min时,CO的转化率=
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表列出了①~⑧所分别代表的八种元素在周期表中的位置,按要求填写下列问题:
(1)①~⑧八种元素中金属性最强的元素是_______ (填元素符号)。
(2)元素②与①组成的某化合物,其分子为18电子体,分子中两种元素原子个数的最简比为1:2,则该分子的电子式为_______ 。
(3)元素⑧的原子结构示意图为_______ 。
(4)Mg和元素⑤的单质作电极材料,氢氧化钠溶液作电解质溶液,能设计成原电池,则该电池负极反应式为_______ 。
(5)写出碳单质与元素②最高价氧化物对应水化物的浓溶液反应的化学方程式_______ 。
(6)第118号元素与⑥为同族元素,它位于元素周期表第_______ 周期。
周期 族 | IA | 0 | ||||||
1 | ① | lIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | |||||
4 | ⑦ | ⑧ |
(2)元素②与①组成的某化合物,其分子为18电子体,分子中两种元素原子个数的最简比为1:2,则该分子的电子式为
(3)元素⑧的原子结构示意图为
(4)Mg和元素⑤的单质作电极材料,氢氧化钠溶液作电解质溶液,能设计成原电池,则该电池负极反应式为
(5)写出碳单质与元素②最高价氧化物对应水化物的浓溶液反应的化学方程式
(6)第118号元素与⑥为同族元素,它位于元素周期表第
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】锌锰干电池由于其贮存和使用寿命较短,大都为一次性电池,用完之后被当作垃圾扔掉。这不仅浪费了宝贵的金属资源,而且还会产生严重的环境污染。下表是各类电池的综合成分分析结果:
通过简单的机械处理,将电池中各组分进行最大在限度的分离,从而使整个处理过程得到简化。再分别对锌皮和锰粉(MnO2)进行湿法处理,通过预处理、浸取、净化等工序制出产品。工艺流程如下图:

查阅资料知各离子沉淀完全的pH为
已知:锌元素与铝元素相似,具有两性。
(1)市售锌锰干电池为碱性电池,电解质溶液为KOH,则其正极反应为___________ ;电极总反应方程为___________ ;
(2)在预处理中,分离铁皮和锌皮的方法是___________ 。洗液加(NH4)2CO3在pH=7.5沉淀出一种碱式盐,该物质的化学式为___________ 。
(3)二氧化锰生产中,写出加入30%盐酸溶解时的离子方程式___________ ;盐酸溶解后回收的渣是___________ ;
(4)已知第二次加H2O2后调节pH≈9的目的为将Mn2+转化为MnO2,则第一次加H2O2后调节pH≈5,目的是___________ ;
(5)实验室中用高锰酸钾溶液检验Mn2+时,产生黑色沉淀,该反应的离子方程式为_______ :
(6)硫酸锰在高温条件下可以得到三种氧化物,该热分解的方程式为___________ 。
| 元素 | 锌 | 锰 | 铁 | 铜 | 碳 | 其它 |
| 质量百分含量 | 13~27 | 14~28 | 23~26 | 0.5~0.7 | 5~6 | 13 |

查阅资料知各离子沉淀完全的pH为
| 离子 | Fe3+ | Fe2+ | Cu2+ | Mn2+ |
| pH | 3.2 | 9.0 | 6.7 | 10.1 |
(1)市售锌锰干电池为碱性电池,电解质溶液为KOH,则其正极反应为
(2)在预处理中,分离铁皮和锌皮的方法是
(3)二氧化锰生产中,写出加入30%盐酸溶解时的离子方程式
(4)已知第二次加H2O2后调节pH≈9的目的为将Mn2+转化为MnO2,则第一次加H2O2后调节pH≈5,目的是
(5)实验室中用高锰酸钾溶液检验Mn2+时,产生黑色沉淀,该反应的离子方程式为
(6)硫酸锰在高温条件下可以得到三种氧化物,该热分解的方程式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】I.一定条件下,将2molA气体和2molB气体加入2L的恒容密闭容器中进行反应: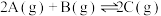 。2min后达化学平衡,测得C的浓度为
。2min后达化学平衡,测得C的浓度为 ,填写下列空白:
,填写下列空白:
(1)2min内用A表示的平均反应速率为_______ 。
(2)平衡时B的物质的量浓度为_______ 。
(3)平衡时A的转化率是B的转化率的_______ 倍。
(4)能说明该反应达到化学平衡状态的是:_______ 。
(5)要使该反应的化学反应速率加快,可采取的措施是:_______ (任写两种)。
II.理论上,任何自发的氧化还原反应都可以设计成原电池。利用反应 设计一种化学电池,回答下列问题:
设计一种化学电池,回答下列问题:
(6)正极上发生的电极反应式为_______ 。
(7)若导线上转移的电子为1mol,则消耗金属铜的质量为_______ 。
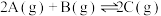 。2min后达化学平衡,测得C的浓度为
。2min后达化学平衡,测得C的浓度为 ,填写下列空白:
,填写下列空白:(1)2min内用A表示的平均反应速率为
(2)平衡时B的物质的量浓度为
(3)平衡时A的转化率是B的转化率的
(4)能说明该反应达到化学平衡状态的是:
| A.A表示的平均反应速率等于C表示的平均反应速率 |
| B.消耗1molA的同时生成0.5molB |
| C.分别用A、B、C表示的反应速率之比为2∶1∶2 |
| D.C的物质的量不再变化 |
II.理论上,任何自发的氧化还原反应都可以设计成原电池。利用反应
 设计一种化学电池,回答下列问题:
设计一种化学电池,回答下列问题:(6)正极上发生的电极反应式为
(7)若导线上转移的电子为1mol,则消耗金属铜的质量为
您最近一年使用:0次



