原子序数依次递增且都小于36的X、Y、Z、Q、W五种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Q原子基态时2p原子轨道上有2个未成对的电子,W元素的原子结构中3d能级有4个未成对电子。回答下列问题:
(1)Y2X2分子中σ键和π键个数比为_______ 。
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是_______ 。
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是_______ 。
(4)元素W能形成多种配合物,如:W(CO)5等。
①基态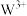 的M层电子排布式为
的M层电子排布式为_______ 。
②W(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断 晶体属于
晶体属于_______ (填晶体类型)。
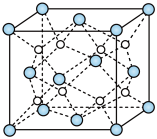
(5)Q和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为_______ 。已知该晶胞密度为 ,阿伏加德罗常数为NA,求晶胞边长a=
,阿伏加德罗常数为NA,求晶胞边长a=_______ nm。(用含ρ、NA的计算式表示)
(1)Y2X2分子中σ键和π键个数比为
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是
(4)元素W能形成多种配合物,如:W(CO)5等。
①基态
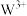 的M层电子排布式为
的M层电子排布式为②W(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断
 晶体属于
晶体属于(5)Q和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为
 ,阿伏加德罗常数为NA,求晶胞边长a=
,阿伏加德罗常数为NA,求晶胞边长a=
更新时间:2023/09/04 14:56:18
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】1869年,俄国化学家门捷列夫制作了第一张元素周期表,如表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

(1)e元素简化的电子排布式为_________
(2)元素h中质子数和中子数相等的同位素符号是_________ 。
(3)画出元素i的简单离子结构示意图为:_________ ,i元素的价层电子排布图为_________ 。
(4)与g同族的锗常用于液晶电视材料其基态原子的电子排布式为_________
(5)工业上用b的单质在电炉中还原g的氧化物制备g单质,写出化学反应方程式:_________ 。
(6)由表中两种元素形成的氢化物A含有18个电子,A是一种6原子分子,可作火箭发动机燃料。B是一种与水组成相同的常见绿色氧化剂。已知16克液态A与液态B充分反应生成一种液态的10电子分子和一种气态单质,并放出838kJ热量,写出A与B反应的热化学方程式_________

(1)e元素简化的电子排布式为
(2)元素h中质子数和中子数相等的同位素符号是
(3)画出元素i的简单离子结构示意图为:
(4)与g同族的锗常用于液晶电视材料其基态原子的电子排布式为
(5)工业上用b的单质在电炉中还原g的氧化物制备g单质,写出化学反应方程式:
(6)由表中两种元素形成的氢化物A含有18个电子,A是一种6原子分子,可作火箭发动机燃料。B是一种与水组成相同的常见绿色氧化剂。已知16克液态A与液态B充分反应生成一种液态的10电子分子和一种气态单质,并放出838kJ热量,写出A与B反应的热化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】金(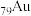 )是一种非常稳定的金属,但也可以形成多种化合物,并在化合物中呈正一价或正三价。
)是一种非常稳定的金属,但也可以形成多种化合物,并在化合物中呈正一价或正三价。
(1)已知 的基态原子的价电子排布式为
的基态原子的价电子排布式为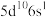 ,侧
,侧 位于周期表
位于周期表_______ 区。基态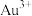 的价电子轨道表示式为
的价电子轨道表示式为_______ 。
(2) 可以被王水溶解,其反应的方程式为
可以被王水溶解,其反应的方程式为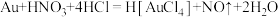 。
。
① 的空间结构为
的空间结构为_______ , 中心原子的杂化轨道类型为
中心原子的杂化轨道类型为_______ 。
②该反应中没有破坏的化学键有_______ 。
a.金属键 b.离子键 c.共价键 d.氢键 e.极性键 f.非极性键 g.配位键 h. 键 i.
键 i. 键
键
(3)金晶体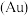 是面心立方堆积,其晶胞参数为
是面心立方堆积,其晶胞参数为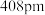 。已知阿伏加德罗常数的值为
。已知阿伏加德罗常数的值为 。写出金晶体密度的计算式:
。写出金晶体密度的计算式:_______  (不需要计算出结果)。
(不需要计算出结果)。
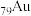 )是一种非常稳定的金属,但也可以形成多种化合物,并在化合物中呈正一价或正三价。
)是一种非常稳定的金属,但也可以形成多种化合物,并在化合物中呈正一价或正三价。(1)已知
 的基态原子的价电子排布式为
的基态原子的价电子排布式为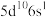 ,侧
,侧 位于周期表
位于周期表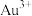 的价电子轨道表示式为
的价电子轨道表示式为(2)
 可以被王水溶解,其反应的方程式为
可以被王水溶解,其反应的方程式为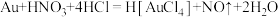 。
。①
 的空间结构为
的空间结构为 中心原子的杂化轨道类型为
中心原子的杂化轨道类型为②该反应中没有破坏的化学键有
a.金属键 b.离子键 c.共价键 d.氢键 e.极性键 f.非极性键 g.配位键 h.
 键 i.
键 i. 键
键(3)金晶体
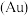 是面心立方堆积,其晶胞参数为
是面心立方堆积,其晶胞参数为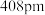 。已知阿伏加德罗常数的值为
。已知阿伏加德罗常数的值为 。写出金晶体密度的计算式:
。写出金晶体密度的计算式: (不需要计算出结果)。
(不需要计算出结果)。
您最近一年使用:0次
【推荐3】完成下列填空
(1)某元素基态原子电子排布式为[Ar]3d104s24p1,该元素处于周期表第___________ 周期,第___________ 族,位于___________ 区。
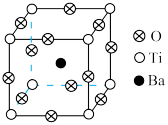
(2)钛酸钡是一种典型钙钛矿型结构晶体,其晶胞如图,写出其化学式:___________ 。
(3)图表法、图像法是常用的科学研究方法。短周期某主族元素M的电离能情况如图A所示。则M元素位于周期表的第___________ 族。图B是研究部分主族元素的氢化物的沸点变化规律的图像,折线c可以表达出第___________ 族元素氢化物的沸点的变化规律。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线,折线a和折线b,你认为正确的是___________ (填“a”或“b”),理由是___________ 。

(1)某元素基态原子电子排布式为[Ar]3d104s24p1,该元素处于周期表第
(2)钛酸钡是一种典型钙钛矿型结构晶体,其晶胞如图,写出其化学式:

(3)图表法、图像法是常用的科学研究方法。短周期某主族元素M的电离能情况如图A所示。则M元素位于周期表的第

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E为短周期元素且它们的原子序数依次增大,A原子的核外电子总数与其周期数相同:D原子的L能层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L能层中未成对电子数与D原子的相同,但有空轨道:D与E同族。回答下列问题。
(1)A与上述其他元素形成的二元共价化合物中,有一种化合物分子呈三角锥形,该分子的化学式为___________ ,其中心原子的杂化方式为___________ ,A分别与B、C、D形成的共价化合物中既含有极性共价键,又含有非极性共价键的化合物有___________ (填化学式,任意写出两种)。
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的酸根离子是___________ (填化学式,下同);酸根离子呈三角锥形结构的是___________ 。
(3) 分子的空间结构为
分子的空间结构为___________ ;根据电子云重叠方式的不同,该分子中共价键的类型为___________ 。
(4)B的一种氢化物的相对分子质量是26,其分子中 键和
键和 键的数目之比为
键的数目之比为___________ 。
(1)A与上述其他元素形成的二元共价化合物中,有一种化合物分子呈三角锥形,该分子的化学式为
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的酸根离子是
(3)
 分子的空间结构为
分子的空间结构为(4)B的一种氢化物的相对分子质量是26,其分子中
 键和
键和 键的数目之比为
键的数目之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】元素周期表中第四周期的某些过渡元素(如V、Zn、Cr等)在生产、生活中有着广泛的应用。
(1)钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。
①基态钒原子的价层电子排布式为____ 。
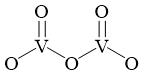
②V2O5的结构式如图所示,则V2O5分子中σ键和π键数目之比为____ 。
(2)根据价层电子对互斥理论,NH3、NO 、NO
、NO 中,中心原子价层电子对数不同于其他两种粒子的是
中,中心原子价层电子对数不同于其他两种粒子的是____ ;NO 与NO
与NO 中O—N—O的键角:NO
中O—N—O的键角:NO
____ NO (填“<”、“>”“=”),并说明原因:
(填“<”、“>”“=”),并说明原因:____ ,比较HNO3与HNO2酸性:HNO3____ HNO2(填“<”、“>”“=”)。
(1)钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。
①基态钒原子的价层电子排布式为
②V2O5的结构式如图所示,则V2O5分子中σ键和π键数目之比为

(2)根据价层电子对互斥理论,NH3、NO
 、NO
、NO 中,中心原子价层电子对数不同于其他两种粒子的是
中,中心原子价层电子对数不同于其他两种粒子的是 与NO
与NO 中O—N—O的键角:NO
中O—N—O的键角:NO
 (填“<”、“>”“=”),并说明原因:
(填“<”、“>”“=”),并说明原因:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钙是一种重要的化学元素,钙在地壳中含量较高且在多方面有着广泛的用途。回答下列问题:
(1)如图是石膏的部分层状结构,中间的虚线代表层与层的分界线。(已知:O:H2O、●:Ca2+、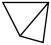 :硫氧四面体)
:硫氧四面体) 的空间构型是
的空间构型是___________ ,石膏中层与层之间的作用力主要是___________ 。

(2)钙钛矿材料是与钛酸钙(CaTiO3)具备相同晶体结构的一类“陶瓷氧化物”的统称,在太阳能电池中应用广泛。其化学式可表示为ABX3,A代表“大半径阳离子”,B代表“金属阳离子”,X代表“阴离子”。常见的A有MA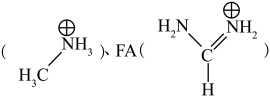 、Cs+,Rb+等,其中MA中N原子的杂化轨道类型是
、Cs+,Rb+等,其中MA中N原子的杂化轨道类型是___________ ,1molFA中存在___________ 个 键(NA表示阿伏加德罗常数的值)。
键(NA表示阿伏加德罗常数的值)。
(3)一种立方钙钛矿型晶体LaCrO3有两种晶胞结构,其三视图如下(重叠处仅画出大的微粒),La的配位数均是12。

①基态Cr原子的价层电子排布式为___________ ,同周期元素中与其最外层电子数相同的元素为___________ (填元素符号)。
②图a晶胞中O的位置为___________ (填“体心”“顶点”“面心”“棱心”,下同);图b晶胞中O的位置为___________ 。图a的晶胞参数为393.9pm,则O与O的最小核间距为___________ pm(写出表达式)。
(1)如图是石膏的部分层状结构,中间的虚线代表层与层的分界线。(已知:O:H2O、●:Ca2+、
 :硫氧四面体)
:硫氧四面体) 的空间构型是
的空间构型是
(2)钙钛矿材料是与钛酸钙(CaTiO3)具备相同晶体结构的一类“陶瓷氧化物”的统称,在太阳能电池中应用广泛。其化学式可表示为ABX3,A代表“大半径阳离子”,B代表“金属阳离子”,X代表“阴离子”。常见的A有MA
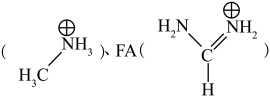 、Cs+,Rb+等,其中MA中N原子的杂化轨道类型是
、Cs+,Rb+等,其中MA中N原子的杂化轨道类型是 键(NA表示阿伏加德罗常数的值)。
键(NA表示阿伏加德罗常数的值)。(3)一种立方钙钛矿型晶体LaCrO3有两种晶胞结构,其三视图如下(重叠处仅画出大的微粒),La的配位数均是12。

①基态Cr原子的价层电子排布式为
②图a晶胞中O的位置为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】 是广泛使用的新型锂离子电池的正极材料,可用
是广泛使用的新型锂离子电池的正极材料,可用 、
、 、LiCl和苯胺(
、LiCl和苯胺(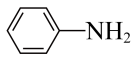 )等原料制备。回答下列问题:
)等原料制备。回答下列问题:
(1)下列不同状态的磷,电离最外层一个电子所需能量最大的是__________(填标号)。
(2) 中非ⅠA族元素的电负性由大到小的顺序为
中非ⅠA族元素的电负性由大到小的顺序为__________ (填元素符号);与 互为等电子体的离子为:
互为等电子体的离子为:__________ (填离子符号,写出一种即可)。
(3) 与
与 的结构相似,二者键角:
的结构相似,二者键角:
__________  (填“>”“=”或“<”),相同条件下,苯胺(
(填“>”“=”或“<”),相同条件下,苯胺(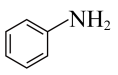 )比甲苯(
)比甲苯(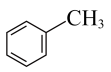 )更易溶于水的原因是
)更易溶于水的原因是__________ 。
(4)配合物 的沸点为103℃,则
的沸点为103℃,则 是
是__________ (填晶体类型);Fe的杂化方式为__________ (填标号)。
A. B.
B.  C.
C.  D.
D. 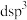
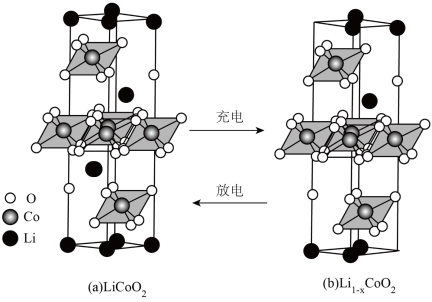
(5)正极材料 的晶胞结构如图(a)(Li位于晶胞顶点和内部,部分O位于晶胞之外),每个晶胞中含有
的晶胞结构如图(a)(Li位于晶胞顶点和内部,部分O位于晶胞之外),每个晶胞中含有__________ 个O;充电时, 脱出部分
脱出部分 ,形成
,形成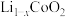 ,结构如图(b),则
,结构如图(b),则 =
=__________ 。
 是广泛使用的新型锂离子电池的正极材料,可用
是广泛使用的新型锂离子电池的正极材料,可用 、
、 、LiCl和苯胺(
、LiCl和苯胺( )等原料制备。回答下列问题:
)等原料制备。回答下列问题:(1)下列不同状态的磷,电离最外层一个电子所需能量最大的是__________(填标号)。
A.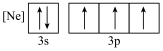 | B.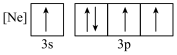 |
C.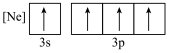 | D.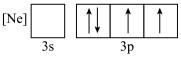 |
(2)
 中非ⅠA族元素的电负性由大到小的顺序为
中非ⅠA族元素的电负性由大到小的顺序为 互为等电子体的离子为:
互为等电子体的离子为:(3)
 与
与 的结构相似,二者键角:
的结构相似,二者键角:
 (填“>”“=”或“<”),相同条件下,苯胺(
(填“>”“=”或“<”),相同条件下,苯胺( )比甲苯(
)比甲苯( )更易溶于水的原因是
)更易溶于水的原因是(4)配合物
 的沸点为103℃,则
的沸点为103℃,则 是
是A.
 B.
B.  C.
C.  D.
D. 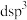
(5)正极材料
 的晶胞结构如图(a)(Li位于晶胞顶点和内部,部分O位于晶胞之外),每个晶胞中含有
的晶胞结构如图(a)(Li位于晶胞顶点和内部,部分O位于晶胞之外),每个晶胞中含有 脱出部分
脱出部分 ,形成
,形成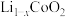 ,结构如图(b),则
,结构如图(b),则 =
=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一。
(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为___________ 。
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是___________ ,最小的是___________ (填标号)。
A. B.
B.  C.
C.  D.
D. 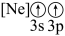
(3)配合物K[Cr(C2O4)(H2O)]中的配体是___________ ,H2O的沸点比CO2的高了许多,主要原因是___________ 。
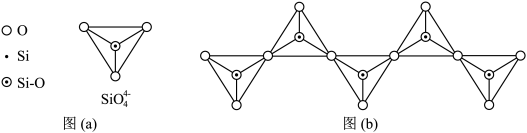
(4)在翡翠等硅酸盐中, 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为___________ ,其化学式为___________ 。低温石英中也存在有顶角相连的硅氧四面体形成螺旋上升的长链,没有封闭的环状结构,这一结构决定了它具有___________ 。
(5)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示,处于顶角位置的是___________ 原子。设Cr和Al原子半径分别为rCr和rAl,则金属原子空间占有率为___________ % (列出计算表达式)。

(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是
A.
 B.
B.  C.
C.  D.
D. 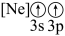
(3)配合物K[Cr(C2O4)(H2O)]中的配体是
(4)在翡翠等硅酸盐中,
 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
(5)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示,处于顶角位置的是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】三磷酸腺苷 和活性氧类(如
和活性氧类(如 和
和 )可在细胞代谢过程中产生。
)可在细胞代谢过程中产生。
(1) 分子式为
分子式为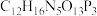 ,其中电负性最大的元素是
,其中电负性最大的元素是___________ ,基态 原子的电子排布式为
原子的电子排布式为___________ 。
(2) 分子的氧原子的杂化轨道类型为:
分子的氧原子的杂化轨道类型为:___________ ; 和
和 能以任意比例互溶的原因是
能以任意比例互溶的原因是___________ 。
(3)根据表中数据判断氧原子之间的共价键最稳定的微粒是___________ 。
(4)研究发现纳米 可催化
可催化 分解,
分解, 晶胞结构如图所示。
晶胞结构如图所示。

①阿伏加德罗常数的值为 摩尔质量为
摩尔质量为 ,晶体密度为
,晶体密度为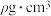 ,其晶胞边长a=
,其晶胞边长a=___________ nm。
②纳米 中位于晶粒表面的
中位于晶粒表面的 能发挥催化作用,在边长为
能发挥催化作用,在边长为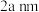 的立方体晶粒中位于表面的
的立方体晶粒中位于表面的 最多有
最多有___________ 个。
 和活性氧类(如
和活性氧类(如 和
和 )可在细胞代谢过程中产生。
)可在细胞代谢过程中产生。(1)
 分子式为
分子式为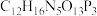 ,其中电负性最大的元素是
,其中电负性最大的元素是 原子的电子排布式为
原子的电子排布式为(2)
 分子的氧原子的杂化轨道类型为:
分子的氧原子的杂化轨道类型为: 和
和 能以任意比例互溶的原因是
能以任意比例互溶的原因是(3)根据表中数据判断氧原子之间的共价键最稳定的微粒是
| 粒子 |  |  |  |
键长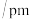 | 121 | 126 | 128 |
(4)研究发现纳米
 可催化
可催化 分解,
分解, 晶胞结构如图所示。
晶胞结构如图所示。
①阿伏加德罗常数的值为
 摩尔质量为
摩尔质量为 ,晶体密度为
,晶体密度为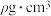 ,其晶胞边长a=
,其晶胞边长a=②纳米
 中位于晶粒表面的
中位于晶粒表面的 能发挥催化作用,在边长为
能发挥催化作用,在边长为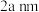 的立方体晶粒中位于表面的
的立方体晶粒中位于表面的 最多有
最多有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】IVA 族元素及其化合物在材料等方面有重要用途。回答下列问题:
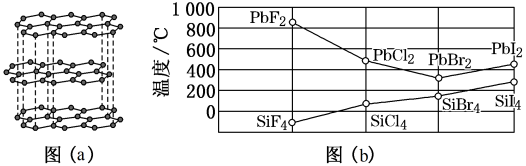
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为________________ ,依据电子云的重叠方式,原子间存在的共价键类型有_____________ ,碳原子的杂化轨道类型为_________ 。
(2)石墨烯是从石墨材料中剥离出来的、由单层碳原子组成的二维晶体。将氢气加入到石墨烯中可制得一种新材料石墨烷。下列判断错误的是___________ 。
A.石墨烯是一种强度很高的材料
B.石墨烯是电的良导体而石墨烷则为绝缘体
C.石墨烯与石墨烷均为高分子化合物
D.石墨烯与H2制得石墨烷的反应属于加成反应
(3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。
①SiX4的沸点依F、Cl、Br、I 次序升高的原因是_________________________________ 。
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I 次序,PbX2中的化学键的离子性___________ 、共价性______________ 。(填 “增 强”“不变”或“减 弱 ”)
(4)碳的另一种单质C60,晶胞结构与金属铜晶胞相似,其晶胞参数为a nm,晶体密度为_______ g·cm-3(只列计算式,不需化简)。
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为

(2)石墨烯是从石墨材料中剥离出来的、由单层碳原子组成的二维晶体。将氢气加入到石墨烯中可制得一种新材料石墨烷。下列判断错误的是
A.石墨烯是一种强度很高的材料
B.石墨烯是电的良导体而石墨烷则为绝缘体
C.石墨烯与石墨烷均为高分子化合物
D.石墨烯与H2制得石墨烷的反应属于加成反应
(3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。
①SiX4的沸点依F、Cl、Br、I 次序升高的原因是
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I 次序,PbX2中的化学键的离子性
(4)碳的另一种单质C60,晶胞结构与金属铜晶胞相似,其晶胞参数为a nm,晶体密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】金红石的主要成分是钛的一种氧化物,该氧化物的晶胞边长分别为 a pm, b pm, c pm。结构如下图所示。
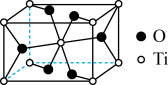
(1)由图可知该氧化物的化学式是___________ ,Ti 填充在 O 构成的___________ 空隙中。
A.三角形 B.四面体 C.八面体
(2)该氧化物的熔点为 1850 ℃,其晶体类型最不可能是___________ 。
A.共价晶体 B.离子晶体 C.分子晶体
(3)已知 m g 该氧化物晶体体积为 V cm3,则阿伏加德罗常数 NA=___________ 。

(1)由图可知该氧化物的化学式是
A.三角形 B.四面体 C.八面体
(2)该氧化物的熔点为 1850 ℃,其晶体类型最不可能是
A.共价晶体 B.离子晶体 C.分子晶体
(3)已知 m g 该氧化物晶体体积为 V cm3,则阿伏加德罗常数 NA=
您最近一年使用:0次
【推荐3】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
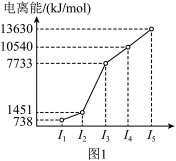
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有____ 种不同运动状态的电子。
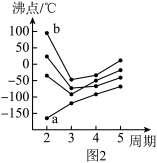
(2)图2中,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是____ (填化学式),图中b的沸点大于a,原因是____ 。
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于_____ 晶体。

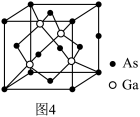
(4)GaAs晶体结构如图4所示,晶体中每个Ga原子与____ 个As原子相连,与同一个Ga原子相连的As原子构成的空间构型为____ 。
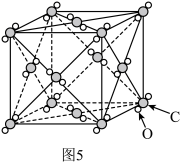
(5)干冰是分子晶体,晶体结构如图5所示,一个干冰晶胞中有____ 个CO2分子。
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有

(2)图2中,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于

(4)GaAs晶体结构如图4所示,晶体中每个Ga原子与

(5)干冰是分子晶体,晶体结构如图5所示,一个干冰晶胞中有

您最近一年使用:0次



