三磷酸腺苷 和活性氧类(如
和活性氧类(如 和
和 )可在细胞代谢过程中产生。
)可在细胞代谢过程中产生。
(1) 分子式为
分子式为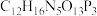 ,其中电负性最大的元素是
,其中电负性最大的元素是___________ ,基态 原子的电子排布式为
原子的电子排布式为___________ 。
(2) 分子的氧原子的杂化轨道类型为:
分子的氧原子的杂化轨道类型为:___________ ; 和
和 能以任意比例互溶的原因是
能以任意比例互溶的原因是___________ 。
(3)根据表中数据判断氧原子之间的共价键最稳定的微粒是___________ 。
(4)研究发现纳米 可催化
可催化 分解,
分解, 晶胞结构如图所示。
晶胞结构如图所示。

①阿伏加德罗常数的值为 摩尔质量为
摩尔质量为 ,晶体密度为
,晶体密度为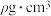 ,其晶胞边长a=
,其晶胞边长a=___________ nm。
②纳米 中位于晶粒表面的
中位于晶粒表面的 能发挥催化作用,在边长为
能发挥催化作用,在边长为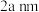 的立方体晶粒中位于表面的
的立方体晶粒中位于表面的 最多有
最多有___________ 个。
 和活性氧类(如
和活性氧类(如 和
和 )可在细胞代谢过程中产生。
)可在细胞代谢过程中产生。(1)
 分子式为
分子式为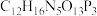 ,其中电负性最大的元素是
,其中电负性最大的元素是 原子的电子排布式为
原子的电子排布式为(2)
 分子的氧原子的杂化轨道类型为:
分子的氧原子的杂化轨道类型为: 和
和 能以任意比例互溶的原因是
能以任意比例互溶的原因是(3)根据表中数据判断氧原子之间的共价键最稳定的微粒是
| 粒子 |  |  |  |
键长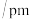 | 121 | 126 | 128 |
(4)研究发现纳米
 可催化
可催化 分解,
分解, 晶胞结构如图所示。
晶胞结构如图所示。
①阿伏加德罗常数的值为
 摩尔质量为
摩尔质量为 ,晶体密度为
,晶体密度为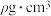 ,其晶胞边长a=
,其晶胞边长a=②纳米
 中位于晶粒表面的
中位于晶粒表面的 能发挥催化作用,在边长为
能发挥催化作用,在边长为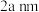 的立方体晶粒中位于表面的
的立方体晶粒中位于表面的 最多有
最多有
更新时间:2024-03-05 01:31:31
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】已知A、B、C、D、E为第二至第四周期的元素,其原子序数依次增大。A原子最外层电子数是其内层电子总数的2倍,B原子s轨道上的电子数与p轨道上的电子数相等,C在元素周期表的各元素中电负性最大,D的基态原子核外有6个能级且全部充满电子,E原子基态时未成对电子数是同周期元素中最多的。请回答下列问题:
(1)基态E原子的价电子排布式为____ 。
(2)A和B中,第一电离能较大的是___ (填元素符号);B的简单氢化物的立体构型是__ ,中心原子的杂化类型是___ 。
(3)A22-和B22+互为等电子体,B22+的电子式可表示为____ ,1 mol B22+中含有的π键数目为____ 。
(4)用氢键表示式写出C的氢化物水溶液中存在的所有氢键_______________ 。
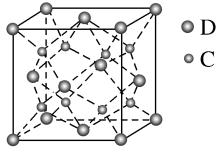
(5)化合物DC2的晶胞结构如图所示,该离子化合物晶体的密度为a g·cm-3,则晶胞的体积是_____ cm3(只要求列算式,阿伏加 德罗常数的值为NA)。
(1)基态E原子的价电子排布式为
(2)A和B中,第一电离能较大的是
(3)A22-和B22+互为等电子体,B22+的电子式可表示为
(4)用氢键表示式写出C的氢化物水溶液中存在的所有氢键
(5)化合物DC2的晶胞结构如图所示,该离子化合物晶体的密度为a g·cm-3,则晶胞的体积是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下图是元素周期表的一部分,图中所列字母分别代表一种化学元素。请回答下列问题:

(1)基态c原子中有___________ 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为___________ 形。
(2)元素f位于周期表中___________ 区,e基态原子有___________ 种空间运动状态不同的电子。
(3)与c同主族且位于第一个长周期的元素的基态原子的电子排布式表示为___________ 。 理论上为离子化合物。猜测其电子式为
理论上为离子化合物。猜测其电子式为___________ 。
(4)b、c、d三种元素电负性由大到小的顺序为___________ (填元素符号)。
(5)已知高温下化合物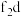 比化合物fd更稳定,试从核外电子排布的角度解释原因
比化合物fd更稳定,试从核外电子排布的角度解释原因_______ 。

(1)基态c原子中有
(2)元素f位于周期表中
(3)与c同主族且位于第一个长周期的元素的基态原子的电子排布式表示为
 理论上为离子化合物。猜测其电子式为
理论上为离子化合物。猜测其电子式为(4)b、c、d三种元素电负性由大到小的顺序为
(5)已知高温下化合物
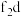 比化合物fd更稳定,试从核外电子排布的角度解释原因
比化合物fd更稳定,试从核外电子排布的角度解释原因
您最近一年使用:0次
【推荐3】在气体分析中,常用CuCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2CuCl+2CO+2H2O=Cu2Cl2•2CO•2H2O。
回答下列问题:
(1)研究人员发现在高温超导材料镧钡铜氧化物中含有Cu3+,基态Cu3+的电子排布式为_______ 。
(2)NO 离子的空间构型是
离子的空间构型是_______ 。
(3)CO与N2互称等电子体。
①它们的分子中都存在三个共价键,其中包含_______ 个π键。
②表为CO和N2的有关信息。
根据表中数据,说明CO比N2活泼的原因是_______ 。
(4)Cu2Cl2•2CO•2H2O是一种配合物,其结构如图所示:
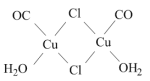
该配合物中,CO作配体时配位原子是C而不是O的原因是_______ 。
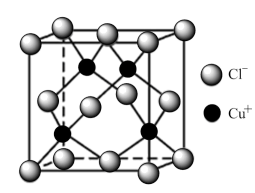
(5)阿伏加德罗常数的测定有多种方法,X射线衍射法就是其中的一种。通过对CuCl晶体的X射线衍射图象分析,可以得出CuCl的晶胞如图所示,若晶体中Cl-呈立方面心最密堆积方式排列,Cl-的半径为a pm,晶体的密度为ρg/cm3,阿伏加德罗常数NA=_______ (列计算式表达)。
回答下列问题:
(1)研究人员发现在高温超导材料镧钡铜氧化物中含有Cu3+,基态Cu3+的电子排布式为
(2)NO
 离子的空间构型是
离子的空间构型是(3)CO与N2互称等电子体。
①它们的分子中都存在三个共价键,其中包含
②表为CO和N2的有关信息。
| 键的类型 | A-B(单键) | A=B(双键) | A≡B(叁键) | |
| 键能(kJ/mol) | CO | 351 | 803 | 1071 |
| N2 | 159 | 418 | 946 | |
根据表中数据,说明CO比N2活泼的原因是
(4)Cu2Cl2•2CO•2H2O是一种配合物,其结构如图所示:

该配合物中,CO作配体时配位原子是C而不是O的原因是
(5)阿伏加德罗常数的测定有多种方法,X射线衍射法就是其中的一种。通过对CuCl晶体的X射线衍射图象分析,可以得出CuCl的晶胞如图所示,若晶体中Cl-呈立方面心最密堆积方式排列,Cl-的半径为a pm,晶体的密度为ρg/cm3,阿伏加德罗常数NA=

您最近一年使用:0次
【推荐1】金属钛被誉为“未来金属”,钛及其化合物被广泛应用于飞机、火箭、卫星、舰艇、医疗等领域。
(1)钛位于周期表的___________ 区,基态钛原子价电子排布式为___________ 。
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。请写出一个与BH 互为等电子体的微粒
互为等电子体的微粒___________ (化学式)。
(3)钛的某配合物可用于催化环烯烃聚合,其结构如图所示。

①该配合物中碳原子的杂化类型为___________ ;
②该配合物中存在的化学键有___________ (填标号)。
a.共价键 b.金属键 c.配位键 d.氢键
(4)钛与卤素形成的化合物TiF4、TiCl4、TiBr4、TiI4熔点依次为377℃、-24℃、38.3℃、153℃,其中TiCl4、TiBr4、TiI4熔点依次升高的原因是___________ 。
(5)CaTiO3的晶胞如图所示,Ti4+的配位数为___________ ,若Ca2+位于晶胞顶点,则O2-位于晶胞___________ 位置,若晶胞参数为anm,则晶体密度为___________ g·cm-3(列出计算式,阿伏加德罗常数用NA表示)。

(1)钛位于周期表的
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。请写出一个与BH
 互为等电子体的微粒
互为等电子体的微粒(3)钛的某配合物可用于催化环烯烃聚合,其结构如图所示。

①该配合物中碳原子的杂化类型为
②该配合物中存在的化学键有
a.共价键 b.金属键 c.配位键 d.氢键
(4)钛与卤素形成的化合物TiF4、TiCl4、TiBr4、TiI4熔点依次为377℃、-24℃、38.3℃、153℃,其中TiCl4、TiBr4、TiI4熔点依次升高的原因是
(5)CaTiO3的晶胞如图所示,Ti4+的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硼元素及其化合物具有各异的结构与性质。
(1)写出基态硼原子的价电子排布图:_______ ,同周期中第一电离能介于B和N之间的元素有_______ 种。
(2) 是合成氮化硼纳米管的原料之一,
是合成氮化硼纳米管的原料之一, 中B原子的杂化方式为
中B原子的杂化方式为_______ 。
(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图所示。
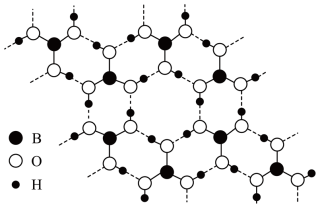
H3BO3的层状结构
① 晶体中含有
晶体中含有_______ mol氢键。
② 分子中的O—B—O的键角
分子中的O—B—O的键角_______ (填“大于”、“等于”或“小于”) 中的H—B—H的键角。
中的H—B—H的键角。
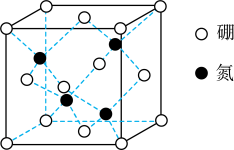
(4)氮化硼晶体有多种相结构,六方相氮化硼与石墨相似,具有层状结构,可作高温润滑剂,立方相氮化硼是超硬材料,有优异的耐磨性,它们的晶体结构如图所示。

①六方相氮化硼的化学式为_______ ,其晶体中存在的作用力有_______ (填字母序号)。
a.范德华力 b. 键 c.离子键
键 c.离子键
②六方相氮化硼晶体俗称“白石墨”,石墨能导电的主要原因是电子能在由电负性相同的碳原子所形成的大 键中流动。但六方氮化硼晶体不导电,可能的原因是
键中流动。但六方氮化硼晶体不导电,可能的原因是_______ 。
③立方氮化硼晶体其晶胞如图所示。晶胞中含有_______ 个硼原子,距离硼原子最近的氮原子有_______ 个。
(1)写出基态硼原子的价电子排布图:
(2)
 是合成氮化硼纳米管的原料之一,
是合成氮化硼纳米管的原料之一, 中B原子的杂化方式为
中B原子的杂化方式为(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图所示。

H3BO3的层状结构
①
 晶体中含有
晶体中含有②
 分子中的O—B—O的键角
分子中的O—B—O的键角 中的H—B—H的键角。
中的H—B—H的键角。(4)氮化硼晶体有多种相结构,六方相氮化硼与石墨相似,具有层状结构,可作高温润滑剂,立方相氮化硼是超硬材料,有优异的耐磨性,它们的晶体结构如图所示。

①六方相氮化硼的化学式为
a.范德华力 b.
 键 c.离子键
键 c.离子键②六方相氮化硼晶体俗称“白石墨”,石墨能导电的主要原因是电子能在由电负性相同的碳原子所形成的大
 键中流动。但六方氮化硼晶体不导电,可能的原因是
键中流动。但六方氮化硼晶体不导电,可能的原因是③立方氮化硼晶体其晶胞如图所示。晶胞中含有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】某绿色农药结构简式如图,回答下列问题。

(1)基态硒原子价电子排布式为__________ ,该农药组成元素中,第一电离能较大的前三种元素是________ (按由大到小顾序排列)。
(2)分子中编号为①的碳原子和与其成键的另外几个原子构成的空间结构为_________ ;CSe2首次是由H2Se 和CCl4 反应制取的,试比较上述三种分子的键角_____________ (按由大到小顺序排列)。
(3)H2SeO3 分子的中心原子杂化类型是____________ ,试比较H2SeO3、H2SeO4 和H2SO4三种酸的酸性强弱(按由强到弱顺序排列)_______________ 。
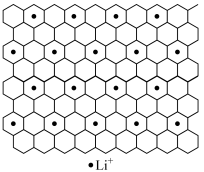
(4)石墨是碳元素的一种同素异形体,石墨晶体可看作ABABA...堆积方式。碱金属离子可填充在石墨层问形成石墨夹层化合物,同时堆积方式从ABABAB...变为AAAA...。下图为石墨夹层化合物W 的投影图,试写出W 的学式_____ ,微粒之间存在的化学键有______ 。

(1)基态硒原子价电子排布式为
(2)分子中编号为①的碳原子和与其成键的另外几个原子构成的空间结构为
(3)H2SeO3 分子的中心原子杂化类型是
(4)石墨是碳元素的一种同素异形体,石墨晶体可看作ABABA...堆积方式。碱金属离子可填充在石墨层问形成石墨夹层化合物,同时堆积方式从ABABAB...变为AAAA...。下图为石墨夹层化合物W 的投影图,试写出W 的学式

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】Pt-硼酸钴是一种高效催化剂,能够实现硝基化合物和醛类化合物进一步合成亚胺。回答下列问题:
(1)基态 原子的价电子轨道表示式是
原子的价电子轨道表示式是______ ,B原子的最低能级原子轨道电子云形状是______ 。
(2)将硼氢化钠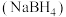 溶液加入钻盐溶液中得到硼酸钴载体。
溶液加入钻盐溶液中得到硼酸钴载体。 固体中含有的化学键有
固体中含有的化学键有______ (填序号), 的空间构型是
的空间构型是______ 。
a.离子键 b.共价键 c.金属键 d.配位键
(3) 是硼酸的酸酐,其气态分子结构如图1所示。
是硼酸的酸酐,其气态分子结构如图1所示。 遇到热的水蒸气时,反应生成偏硼酸
遇到热的水蒸气时,反应生成偏硼酸 ,其结构如图2所示,该反应中,B原子杂化轨道类型由
,其结构如图2所示,该反应中,B原子杂化轨道类型由______ 变为______ ,偏硼酸分子中各元素电负性由大到小的顺序是______ 。

(4)常温常压下,硼酸 晶体结构为层状,其二维平面结构如图所示,
晶体结构为层状,其二维平面结构如图所示,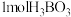 晶体中含有
晶体中含有______ mol氢键;请从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大的原因:______ 。

(1)基态
 原子的价电子轨道表示式是
原子的价电子轨道表示式是(2)将硼氢化钠
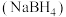 溶液加入钻盐溶液中得到硼酸钴载体。
溶液加入钻盐溶液中得到硼酸钴载体。 固体中含有的化学键有
固体中含有的化学键有 的空间构型是
的空间构型是a.离子键 b.共价键 c.金属键 d.配位键
(3)
 是硼酸的酸酐,其气态分子结构如图1所示。
是硼酸的酸酐,其气态分子结构如图1所示。 遇到热的水蒸气时,反应生成偏硼酸
遇到热的水蒸气时,反应生成偏硼酸 ,其结构如图2所示,该反应中,B原子杂化轨道类型由
,其结构如图2所示,该反应中,B原子杂化轨道类型由
(4)常温常压下,硼酸
 晶体结构为层状,其二维平面结构如图所示,
晶体结构为层状,其二维平面结构如图所示,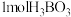 晶体中含有
晶体中含有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】联氨(N2H4)可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀,其中一种可能的反应机理如图所示,回答下列问题:
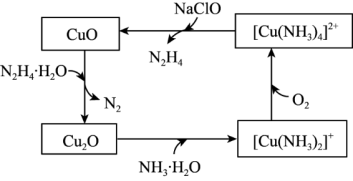
(1)[Cu(NH3)4]2+是一种常见的配离子,其中心离子为_______ ,配位原子为_______ ,配位数_______ 。
(2)写出碱性条件下,[Cu(NH3)4]2+与NaClO反应的离子方程式_______ 。
(3)N2H4中心原子的杂化类型是_______ 。N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃)沸点(114℃)分别远远高于O2的熔点(-218℃)、沸点(-183℃),原因是_______ 。
(4)NaClO发生水解可生成HClO。HClO的空间构型是_______ 。
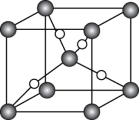
(5)已知Cu2O晶胞的结构如图所示:
①在该晶胞中,Cu+的配位数_______ 。
②已知该晶体密度为ρg/cm3,NA表示阿伏加德罗常数的数值,则晶胞参数a(立方体边长)为_______ pm(用含ρ和NA的代数式表示)。

(1)[Cu(NH3)4]2+是一种常见的配离子,其中心离子为
(2)写出碱性条件下,[Cu(NH3)4]2+与NaClO反应的离子方程式
(3)N2H4中心原子的杂化类型是
(4)NaClO发生水解可生成HClO。HClO的空间构型是
(5)已知Cu2O晶胞的结构如图所示:
①在该晶胞中,Cu+的配位数
②已知该晶体密度为ρg/cm3,NA表示阿伏加德罗常数的数值,则晶胞参数a(立方体边长)为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】前四周期中原子序数依次增大的五种元素A、B、C、D、E,其中A、B同周期,B、C同族,A元素2p原子轨道半充满,C原子有2个未成对电子,D元素原子核外有17种运动状态的电子;E元素次外层全充满,最外层只有1个电子。回答下列问题:
(1)E原子的价层电子排布图为___________ ,其p电子的原子轨道呈___________ 形;
(2)B的氢化物比同族相邻元素氢化物沸点高,原因是___________ ;
(3)C、D的最高价含氧酸中酸性较强的是___________ (填化学式);该酸中阴离子的空间构型是___________ ,中心原子的杂化类型为___________ ;
(4)A和D形成的化合物AD3的电子式为___________ ,该物质水解生成碱性气体和漂白性物质,写出该反应的化学方程式___________ ;
(5)A的氢化物通入到E2+溶液中发生的反应为___________ 、___________ ;
(1)E原子的价层电子排布图为
(2)B的氢化物比同族相邻元素氢化物沸点高,原因是
(3)C、D的最高价含氧酸中酸性较强的是
(4)A和D形成的化合物AD3的电子式为
(5)A的氢化物通入到E2+溶液中发生的反应为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】MnCO3常用于医药、电焊条辅料等,以软锰矿(主要成分为MnO2,还含有少量Fe2O3、Al2O3、SiO2、MgO、CaO等)为原料制备MnCO3的流程如下:

回答下列问题:
(1)废铁屑在使用前需要用热的纯碱溶液清洗表面油污,其清洗原理为_______ (结合离子方程式和必要的语言解释)。
(2)为了使废铁屑与软锰矿在“酸浸”中充分反应,可采取的措施为_______ ;“酸浸”时主要发生反应的离子方程式为_______ 。
(3)“滤渣1”中含有的主要成分为_______ 。
(4)“氧化”过程中加入H2O2的量远超理论量的原因为_______ 。
(5)加入CaCO3能“除铁、铝”的原因为_______ 。
(6)“沉锰”时发生反应的离子方程式为_______ 。
(7)MnO2的正交(棱与棱之间的夹角均为 )晶胞结构如下图所示,晶胞参数分别为
)晶胞结构如下图所示,晶胞参数分别为 、
、 、
、 。其中Mn的配位数为
。其中Mn的配位数为_______ ;用NA表示阿伏加德罗常数的值,该晶体的密度为_______ 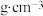 。
。


回答下列问题:
(1)废铁屑在使用前需要用热的纯碱溶液清洗表面油污,其清洗原理为
(2)为了使废铁屑与软锰矿在“酸浸”中充分反应,可采取的措施为
(3)“滤渣1”中含有的主要成分为
(4)“氧化”过程中加入H2O2的量远超理论量的原因为
(5)加入CaCO3能“除铁、铝”的原因为
(6)“沉锰”时发生反应的离子方程式为
(7)MnO2的正交(棱与棱之间的夹角均为
 )晶胞结构如下图所示,晶胞参数分别为
)晶胞结构如下图所示,晶胞参数分别为 、
、 、
、 。其中Mn的配位数为
。其中Mn的配位数为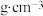 。
。
您最近一年使用:0次
【推荐2】公元前200年左右中国就开始使用镍。镍主要用于合金及用作催化剂,也可用来制造货币。以镍废渣(主要成分为Ni,还含有 、NiO、FeO、CaO和
、NiO、FeO、CaO和 )为原料制备纯镍的流程如图,回答下列问题:
)为原料制备纯镍的流程如图,回答下列问题:______ (填化学式)。常温下,“酸浸”中硫酸浓度与镍浸出率的关系如图所示。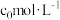 后,镍浸出率降低的可能原因是
后,镍浸出率降低的可能原因是____________ 。
(2)“氧化”时双氧水的作用是____________ (用离子方程式表示)。
(3)“沉铝”时NiO的作用是_______ ,“操作X”包括蒸发浓缩、______ 、过滤、洗涤。
(4) 在隔绝空气条件下的热失重曲线如下图2所示。a→b过程中失去的物质是
在隔绝空气条件下的热失重曲线如下图2所示。a→b过程中失去的物质是______ (填化学式,下同),c点对应的氧化物为______ 。 代表阿伏加德罗常数的值。该晶胞中Ni、Nb个数之比为
代表阿伏加德罗常数的值。该晶胞中Ni、Nb个数之比为____ ,该晶体的密度为___ (填表达式)g·cm 。
。
 、NiO、FeO、CaO和
、NiO、FeO、CaO和 )为原料制备纯镍的流程如图,回答下列问题:
)为原料制备纯镍的流程如图,回答下列问题: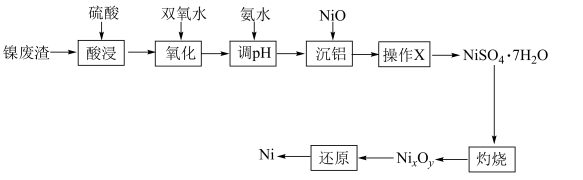
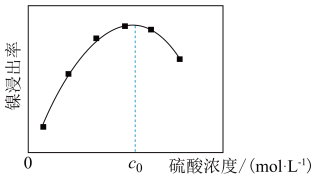
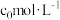 后,镍浸出率降低的可能原因是
后,镍浸出率降低的可能原因是(2)“氧化”时双氧水的作用是
(3)“沉铝”时NiO的作用是
(4)
 在隔绝空气条件下的热失重曲线如下图2所示。a→b过程中失去的物质是
在隔绝空气条件下的热失重曲线如下图2所示。a→b过程中失去的物质是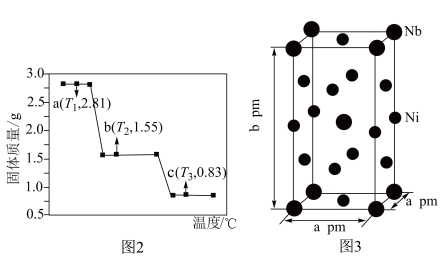
 代表阿伏加德罗常数的值。该晶胞中Ni、Nb个数之比为
代表阿伏加德罗常数的值。该晶胞中Ni、Nb个数之比为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铁被誉为“第一金属”,铁及其化合物广泛应用于生活、生产、国防等领域。
(1)基态Fe原子的价层电子的电子排布图为_______ ;其最外层电子的电子云形状为_______ 。
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为_______ 晶体。
(3) 俗称摩尔盐,其阴离子的立体构型名称为
俗称摩尔盐,其阴离子的立体构型名称为_______ 。写出一种与 互为等电子体的分子的电子式:
互为等电子体的分子的电子式:_______ 。
(4) 可用作催化剂、汽油抗爆剂等,其分子中
可用作催化剂、汽油抗爆剂等,其分子中 键和
键和 键的数目之比为
键的数目之比为_______ 。
(5)铁晶体有面心立方最密堆积和体心立方堆积两种晶体,这两种晶体铁原子的配位数之比为_______ 。
(6)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为_______ 。

(1)基态Fe原子的价层电子的电子排布图为
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为
(3)
 俗称摩尔盐,其阴离子的立体构型名称为
俗称摩尔盐,其阴离子的立体构型名称为 互为等电子体的分子的电子式:
互为等电子体的分子的电子式:(4)
 可用作催化剂、汽油抗爆剂等,其分子中
可用作催化剂、汽油抗爆剂等,其分子中 键和
键和 键的数目之比为
键的数目之比为(5)铁晶体有面心立方最密堆积和体心立方堆积两种晶体,这两种晶体铁原子的配位数之比为
(6)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次



