氧化锌是一种有独特物理化学性能的功能材料,利用锌焙砂(主要成分为ZnO,含As2O3及铅、铜、镉的氧化物)生产高纯氧化锌的工业流程如图所示。
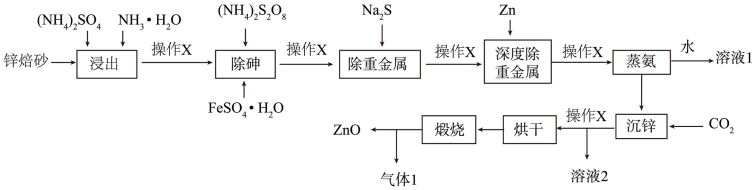
已知:As2O3微溶于水而生成亚砷酸H3AsO3,FeAsO4和ZnCO3难溶于水。回答下列问题:
(1)操作X为___________ 。
(2)锌元素位于元素周期表第___________ 周期,第___________ 族,As的价层电子轨道表达式为___________ 。
(3)“浸出”过程(NH4)2SO4和NH3·H2O按1:2比例参加反应生成了[Zn(NH3)4]2+,发生的离子反应方程式为___________ 。
(4)流程中可循环利用的含氮物质有___________ (填化学式)。
(5)已知“蒸氨”后锌元素以Zn(NH3)2SO4存在,写出“沉锌”的化学方程式:___________ 。
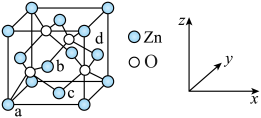
(6)ZnO晶胞如图所示。原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0);b为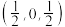 ;c为
;c为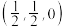 。则d的坐标参数为
。则d的坐标参数为___________ 。

已知:As2O3微溶于水而生成亚砷酸H3AsO3,FeAsO4和ZnCO3难溶于水。回答下列问题:
(1)操作X为
(2)锌元素位于元素周期表第
(3)“浸出”过程(NH4)2SO4和NH3·H2O按1:2比例参加反应生成了[Zn(NH3)4]2+,发生的离子反应方程式为
(4)流程中可循环利用的含氮物质有
(5)已知“蒸氨”后锌元素以Zn(NH3)2SO4存在,写出“沉锌”的化学方程式:
(6)ZnO晶胞如图所示。原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0);b为
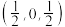 ;c为
;c为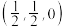 。则d的坐标参数为
。则d的坐标参数为
更新时间:2023-10-05 11:56:46
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】栲胶法脱除煤气中硫化氢的工艺流程示意如下:
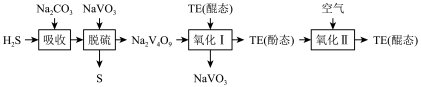
回答下列问题:
(1)“吸收”步骤除了生成 外,还生成了NaHS。NaHS的电离方程式为
外,还生成了NaHS。NaHS的电离方程式为___________ 。
(2)“脱硫”步骤的中间产物可与“吸收”步骤中生成的 反应,实现
反应,实现 的再生,再生反应的离子方程式为
的再生,再生反应的离子方程式为___________ 。
(3)“脱硫”步骤中,改变溶液pH,溶液中含硫微粒的浓度随时间变化结果如下图。
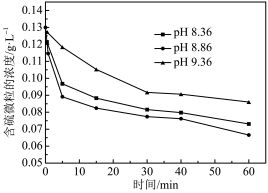
根据图象分析脱硫过程中常将pH维持在8.86的原因是___________ 。
(4)“氧化Ⅰ”步骤发生反应的化学方程式为: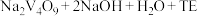 (醌态)
(醌态) (酚态)
(酚态)
则1mol TE(醌态)和1mol TE(酚态)在组成上相差_____ mol _____ (填写微粒符号)。
(5)“氧化Ⅰ”步骤和“氧化Ⅱ”步骤的作用分别是___________ ;___________ 。
(6)该流程总反应的化学方程式为___________ 。

回答下列问题:
(1)“吸收”步骤除了生成
 外,还生成了NaHS。NaHS的电离方程式为
外,还生成了NaHS。NaHS的电离方程式为(2)“脱硫”步骤的中间产物可与“吸收”步骤中生成的
 反应,实现
反应,实现 的再生,再生反应的离子方程式为
的再生,再生反应的离子方程式为(3)“脱硫”步骤中,改变溶液pH,溶液中含硫微粒的浓度随时间变化结果如下图。

根据图象分析脱硫过程中常将pH维持在8.86的原因是
(4)“氧化Ⅰ”步骤发生反应的化学方程式为:
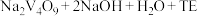 (醌态)
(醌态) (酚态)
(酚态)
则1mol TE(醌态)和1mol TE(酚态)在组成上相差
(5)“氧化Ⅰ”步骤和“氧化Ⅱ”步骤的作用分别是
(6)该流程总反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】利用氯元素价类二维图可以从不同角度研究含氯物质的性质及其转化关系。图中①~⑩均含氯元素。回答下列问题:
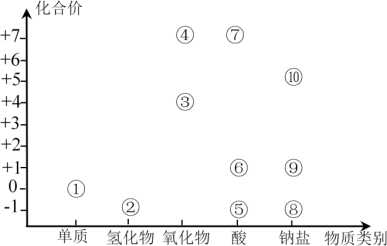
(1)④的化学式为___________ ,⑦的电离方程式为___________ 。
(2)②属于___________ (填“电解质”或“非电解质”)。
(3)⑤与⑨混合可产生①,反应的离子方程式为___________ 。
(4)①可与热的浓NaOH溶液反应生成⑧和⑩,该反应中氧化产物与还原产物个数之比为___________ 。
(5)含⑨的溶液可作为水处理剂除去水中的杂质离子。例如它可使酸性废水中的 转化为N2,反应的离子方程式为
转化为N2,反应的离子方程式为___________ 。

(1)④的化学式为
(2)②属于
(3)⑤与⑨混合可产生①,反应的离子方程式为
(4)①可与热的浓NaOH溶液反应生成⑧和⑩,该反应中氧化产物与还原产物个数之比为
(5)含⑨的溶液可作为水处理剂除去水中的杂质离子。例如它可使酸性废水中的
 转化为N2,反应的离子方程式为
转化为N2,反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】钪是一种稀土金属元素,在国防、航天、核能等领域具有重要应用。氯化钪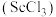 是制备钪的重要原料。工业上利用固体废料“赤泥”(含
是制备钪的重要原料。工业上利用固体废料“赤泥”(含 、
、 、
、 、
、 、
、 等)制取
等)制取 的流程如图。
的流程如图。 难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。
难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。
回答下列问题:
(1)酸浸中,滤渣的主要成分是_______ (填化学式), 溶解的离子反应方程式为
溶解的离子反应方程式为_______ 。
(2)“步骤Ⅰ”中加入 后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是
后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是_______ 。
(3)草酸用量过多时,钪的沉淀率反而下降,原因是_______ 。
(4)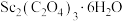 在空气中加热分解时,
在空气中加热分解时, %随温度变化如图所示。
%随温度变化如图所示。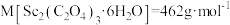 。
。
250℃时固体的主要成分是:_______ (填化学式)。
(5)传统制备 的方法是先得到
的方法是先得到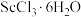 沉淀,再高温脱水得
沉淀,再高温脱水得 ,但通常含有
,但通常含有 杂质,原因是
杂质,原因是_______ 。
(6)“加热氯化”过程主要发生反应的化学方程式为:_______ 。
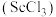 是制备钪的重要原料。工业上利用固体废料“赤泥”(含
是制备钪的重要原料。工业上利用固体废料“赤泥”(含 、
、 、
、 、
、 、
、 等)制取
等)制取 的流程如图。
的流程如图。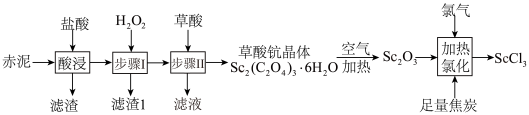
 难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。
难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。回答下列问题:
(1)酸浸中,滤渣的主要成分是
 溶解的离子反应方程式为
溶解的离子反应方程式为(2)“步骤Ⅰ”中加入
 后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是
后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是(3)草酸用量过多时,钪的沉淀率反而下降,原因是
(4)
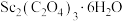 在空气中加热分解时,
在空气中加热分解时, %随温度变化如图所示。
%随温度变化如图所示。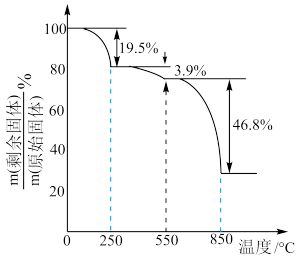
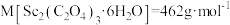 。
。250℃时固体的主要成分是:
(5)传统制备
 的方法是先得到
的方法是先得到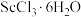 沉淀,再高温脱水得
沉淀,再高温脱水得 ,但通常含有
,但通常含有 杂质,原因是
杂质,原因是(6)“加热氯化”过程主要发生反应的化学方程式为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】一定温度范围内用氯化钠熔浸钾长石(主要成分为KAlSi3O8)可制得氯化钾,主要反应是:NaCl(l)+KAlSi3O8(s) KCl(l)+NaAlSi3O8(s) △H=-Q kJ/mol。
KCl(l)+NaAlSi3O8(s) △H=-Q kJ/mol。
(1)写出Cl原子的核外电子排布式_______ , NaCl的熔点比KCl______ (选填“高”或“低”)。
(2)指出钾长石中存在的化学键类型__________________ 。
(3)上述反应涉及的位于同一周期的几种元素中,有一种元素的最高价氧化物的水化物和其余元素的最高价氧化物的水化物均能发生反应,该元素是_______ 。
 KCl(l)+NaAlSi3O8(s) △H=-Q kJ/mol。
KCl(l)+NaAlSi3O8(s) △H=-Q kJ/mol。(1)写出Cl原子的核外电子排布式
(2)指出钾长石中存在的化学键类型
(3)上述反应涉及的位于同一周期的几种元素中,有一种元素的最高价氧化物的水化物和其余元素的最高价氧化物的水化物均能发生反应,该元素是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】太阳能电池的发展趋向于微型化、薄膜化。最新产品是铜镓(Ga)硒(Se)等化合物薄膜太阳能电池和Si系薄膜太阳能电池。完成下列填空:
(1)亚铜离子(Cu+)基态时的电子排布式_______ ;1mol配合离子[Cu(NH3)2]+ 中,含有σ键数目为 _______ 。
(2)已知硼元素与镓元素处于同一主族BF3分子的空间构型为_______ ,BF3与NH3以配位键结合生成BF3·NH3,该产物中B原子的杂化轨道类型为_________ 。
(3)与硒同周期相邻的元素为砷和溴),则这三种元素的第一电离能从大到小顺序为______ (用元素符号表示),H2Se的沸点比H2O的沸点低,其原因是________ 。
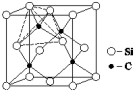
(4)单晶硅的结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得如图所示的金刚砂(SiC)结构;在SiC中,每个Si原子周围最近的Si原子数目为_________ 。
(1)亚铜离子(Cu+)基态时的电子排布式
(2)已知硼元素与镓元素处于同一主族BF3分子的空间构型为
(3)与硒同周期相邻的元素为砷和溴),则这三种元素的第一电离能从大到小顺序为
(4)单晶硅的结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得如图所示的金刚砂(SiC)结构;在SiC中,每个Si原子周围最近的Si原子数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)某二价金属离子有9个价电子,价电子的能级为3d。该元素位于周期表中的第四周期、第_______ 族。
(2)在氰酸钾(KOCN)的组成元素中,第一电离能最大的是_______ (填元素符号、下同)、电负性最小的是_______ ;其中阴离子的空间结构是_______ ,C的杂化方式为_______ 。
(3)将少量无水硫酸铜溶解在水中,形成蓝色溶液,再加入过量氨水,溶液变为蓝色。深蓝色离子的结构如图所示,1mol该离子中所含 键为
键为_______ mol(包括配位键);向深蓝色溶液中缓慢加入乙醇,得到蓝色晶体,加热该晶体先失去组分b的原因是_______
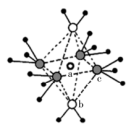
(4)已知阿伏加德罗常数为NA,立方硫化锌(M=97g/mol)晶胞如图所示:

其晶胞棱长为δpm、则其密度为_______ g/cm3(用含δ的代数式表示);其中顶点位置a的S2-离子与其相邻位置b的Zn2+离子之间的距离为_______ pm(用含δ的代数式表示)。b位置的Zn2+离子的原子分数坐标为:_______ 。(已知:1m=102cm=1012pm)
(1)某二价金属离子有9个价电子,价电子的能级为3d。该元素位于周期表中的第四周期、第
(2)在氰酸钾(KOCN)的组成元素中,第一电离能最大的是
(3)将少量无水硫酸铜溶解在水中,形成蓝色溶液,再加入过量氨水,溶液变为蓝色。深蓝色离子的结构如图所示,1mol该离子中所含
 键为
键为
(4)已知阿伏加德罗常数为NA,立方硫化锌(M=97g/mol)晶胞如图所示:

其晶胞棱长为δpm、则其密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】Fe3+可以与SCN-、CN-、有机分子等形成配合物,中国研究团队研发的一种智能比色微针贴片,用于按需治疗和实时报告伤口感染,可由聚乙烯吡咯烷酮(PVP) 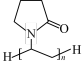 、没食子酸
、没食子酸 和铁离子之间的配位反应制备。回答下列问题:
和铁离子之间的配位反应制备。回答下列问题:
(1)基态Fe3+的价电子排布图(轨道表示式)为___________ 。
(2)写出一种与SCN-互为等电子体的分子:___________ (填化学式)。1mol [Fe(CN)6]3-中含有σ键的数目为___________ 。
(3)PVP 中N原子的杂化轨道类型为___________ ; 没食子酸沸点高于2, 3, 4-三羟基苯甲酸(如图所示) 的原因是___________ 。

(4)下表数据是部分氯化物的熔点:
判断FeCl3的晶体类型为___________ ; 400°C时FeCl3蒸气中有以配位键结合的双聚分子,画出该双聚分子结构: ___________ 。
(5)普鲁士蓝晶体属于立方晶系,晶体密度为ρg·cm-3,铁—氰骨架组成晶胞中的8个小立方体,Fe粒子在小立方体顶点,CN- 在小立方体的棱上,两端均与Fe粒子相连,小立方体中心空隙可容纳K+,如图所示(CN- 在图中已省略)。

该晶胞棱长为___________ pm(阿伏加德罗常数为NA)。
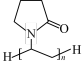 、没食子酸
、没食子酸 和铁离子之间的配位反应制备。回答下列问题:
和铁离子之间的配位反应制备。回答下列问题:(1)基态Fe3+的价电子排布图(轨道表示式)为
(2)写出一种与SCN-互为等电子体的分子:
(3)PVP 中N原子的杂化轨道类型为

(4)下表数据是部分氯化物的熔点:
| 编号 | ① | ② | ③ |
| 物质 | NaCl | AlCl3 | FeCl3 |
| 熔点°C | 801 | 160 | 306 |
(5)普鲁士蓝晶体属于立方晶系,晶体密度为ρg·cm-3,铁—氰骨架组成晶胞中的8个小立方体,Fe粒子在小立方体顶点,CN- 在小立方体的棱上,两端均与Fe粒子相连,小立方体中心空隙可容纳K+,如图所示(CN- 在图中已省略)。

该晶胞棱长为
您最近一年使用:0次
【推荐2】碳是形成化合物种类最多的元素。
(1)CH2=CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为________ (填最简整数比),写出该分子中所有碳原子的杂化方式:________________ 。
(2)乙醇(CH3CH2OH)和二甲醚(CH3OCH3)的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是_______________________________ 。
(3)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为________________ 。
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。如图所示为碳化硅的晶胞(其中 为碳原子,
为碳原子, 为硅原子)。
为硅原子)。
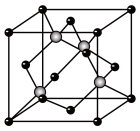
每个碳原子周围与其距离最近的硅原子有________ 个。
(5)写出下列物质的的电子式:①NaOH_____________ ②CO2___________
(1)CH2=CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为
(2)乙醇(CH3CH2OH)和二甲醚(CH3OCH3)的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是
(3)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。如图所示为碳化硅的晶胞(其中
 为碳原子,
为碳原子, 为硅原子)。
为硅原子)。
每个碳原子周围与其距离最近的硅原子有
(5)写出下列物质的的电子式:①NaOH
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】依据要求回答下列问题:
(1)利用离子液体 可电沉积还原金属
可电沉积还原金属 ,其熔点只有
,其熔点只有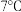 ,其中
,其中 结构如图所示:
结构如图所示:___________ 。
②在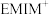 中碳原子的杂化方式有
中碳原子的杂化方式有___________ 。
(2)核酸在生物体的生长、繁殖、遗传和变异等生命现象中起着重要的作用,请从分子结构视角思考并回答下列问题:
①单链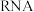 (图一)的水解产物之一——腺嘌呤核苷酸(图二)是生产核酸类药物的中间体,其中分子结构1、2、3的名称分别为
(图一)的水解产物之一——腺嘌呤核苷酸(图二)是生产核酸类药物的中间体,其中分子结构1、2、3的名称分别为___________ 。
②图三为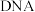 分子的两条多聚核苷酸链上的碱基互补配对时形成氢键的示意图。类比蛋白质的结构,磷酯键对应蛋白质的
分子的两条多聚核苷酸链上的碱基互补配对时形成氢键的示意图。类比蛋白质的结构,磷酯键对应蛋白质的___________ 部分(填“氨基”、“肽键”或“氢键”)。 的晶胞结构(晶胞中相同大小的原子相同)如图所示,其中
的晶胞结构(晶胞中相同大小的原子相同)如图所示,其中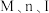 的原子坐标分别为
的原子坐标分别为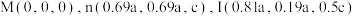 ,晶胞棱边夹角均为
,晶胞棱边夹角均为 。
。 原子数为
原子数为___________ 个。
②Q点的原子坐标为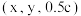 ,其中x=
,其中x=___________ ,y=___________ 。
③设 阿伏加德罗常数的值,该晶体的密度为
阿伏加德罗常数的值,该晶体的密度为___________  (写出表达式即可)。
(写出表达式即可)。
(1)利用离子液体
 可电沉积还原金属
可电沉积还原金属 ,其熔点只有
,其熔点只有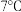 ,其中
,其中 结构如图所示:
结构如图所示: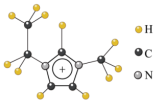
②在
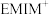 中碳原子的杂化方式有
中碳原子的杂化方式有(2)核酸在生物体的生长、繁殖、遗传和变异等生命现象中起着重要的作用,请从分子结构视角思考并回答下列问题:
①单链
 (图一)的水解产物之一——腺嘌呤核苷酸(图二)是生产核酸类药物的中间体,其中分子结构1、2、3的名称分别为
(图一)的水解产物之一——腺嘌呤核苷酸(图二)是生产核酸类药物的中间体,其中分子结构1、2、3的名称分别为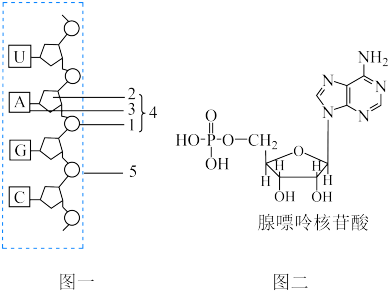
②图三为
 分子的两条多聚核苷酸链上的碱基互补配对时形成氢键的示意图。类比蛋白质的结构,磷酯键对应蛋白质的
分子的两条多聚核苷酸链上的碱基互补配对时形成氢键的示意图。类比蛋白质的结构,磷酯键对应蛋白质的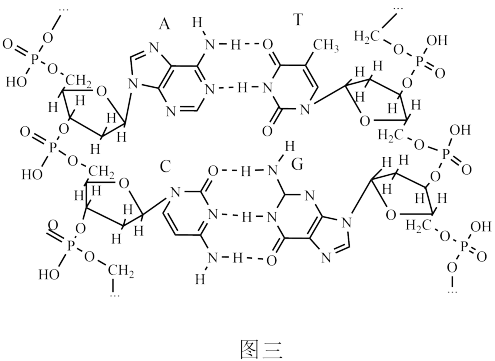
 的晶胞结构(晶胞中相同大小的原子相同)如图所示,其中
的晶胞结构(晶胞中相同大小的原子相同)如图所示,其中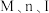 的原子坐标分别为
的原子坐标分别为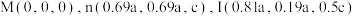 ,晶胞棱边夹角均为
,晶胞棱边夹角均为 。
。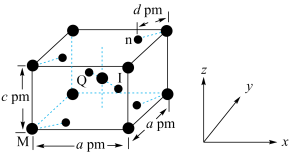
 原子数为
原子数为②Q点的原子坐标为
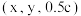 ,其中x=
,其中x=③设
 阿伏加德罗常数的值,该晶体的密度为
阿伏加德罗常数的值,该晶体的密度为 (写出表达式即可)。
(写出表达式即可)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】为了除去氯化钠样品中的杂质碳酸钠,某兴趣小组最初设计了如下所示方案进行实验。
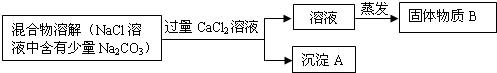
(1)沉淀A的化学式是________ 。
(2)加入过量氯化钙溶液后,分离除去沉淀A的实验操作过程是___________ 。
(3)他们在实验过程中,又发现了新的问题:此方案很容易引入新的杂质。固体物质B的成分为________ (用化学式表示)。
(4)他们继续探究后又提出了新的方案:将混合物溶解,滴加盐酸至不再产生气泡为止,然后加热煮沸。有关反应的化学方程式为______________ 。

(1)沉淀A的化学式是
(2)加入过量氯化钙溶液后,分离除去沉淀A的实验操作过程是
(3)他们在实验过程中,又发现了新的问题:此方案很容易引入新的杂质。固体物质B的成分为
(4)他们继续探究后又提出了新的方案:将混合物溶解,滴加盐酸至不再产生气泡为止,然后加热煮沸。有关反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】氯化铬晶体( )是深绿色结晶粉末,易溶于水、乙醇,不溶于乙醚,易水解,在高温下能被氧化。某兴趣小组以实验室中的红矾钠(
)是深绿色结晶粉末,易溶于水、乙醇,不溶于乙醚,易水解,在高温下能被氧化。某兴趣小组以实验室中的红矾钠( )为原料来制备
)为原料来制备 的流程如下:
的流程如下:

已知: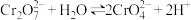 。
。
回答下列问题:
(1)“碱溶”后铬元素在溶液中主要存在形式是___________ 。
(2)“还原”过程中 中碳元素被氧化为+4价,还原反应中氧化剂与还原剂的物质的量之比为
中碳元素被氧化为+4价,还原反应中氧化剂与还原剂的物质的量之比为___________ ,先加入过量 再加入10%
再加入10% ,加入盐酸的目的是
,加入盐酸的目的是___________ 。
(3) 性质与
性质与 相似,用
相似,用 调节
调节 时,
时, 过高的后果是
过高的后果是___________ 。
(4)请补充完整由过滤得到的固体制备 :将过滤后的固体完全溶解在过量盐酸中,
:将过滤后的固体完全溶解在过量盐酸中,___________ ,冷却结晶,过滤,洗涤,低温干燥。
①洗涤 晶体的试剂宜选用
晶体的试剂宜选用___________ 。
② 直接加热脱水往往得到
直接加热脱水往往得到 ,反应的化学方程式为
,反应的化学方程式为___________ 。
 )是深绿色结晶粉末,易溶于水、乙醇,不溶于乙醚,易水解,在高温下能被氧化。某兴趣小组以实验室中的红矾钠(
)是深绿色结晶粉末,易溶于水、乙醇,不溶于乙醚,易水解,在高温下能被氧化。某兴趣小组以实验室中的红矾钠( )为原料来制备
)为原料来制备 的流程如下:
的流程如下:
已知:
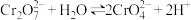 。
。回答下列问题:
(1)“碱溶”后铬元素在溶液中主要存在形式是
(2)“还原”过程中
 中碳元素被氧化为+4价,还原反应中氧化剂与还原剂的物质的量之比为
中碳元素被氧化为+4价,还原反应中氧化剂与还原剂的物质的量之比为 再加入10%
再加入10% ,加入盐酸的目的是
,加入盐酸的目的是(3)
 性质与
性质与 相似,用
相似,用 调节
调节 时,
时, 过高的后果是
过高的后果是(4)请补充完整由过滤得到的固体制备
 :将过滤后的固体完全溶解在过量盐酸中,
:将过滤后的固体完全溶解在过量盐酸中,①洗涤
 晶体的试剂宜选用
晶体的试剂宜选用②
 直接加热脱水往往得到
直接加热脱水往往得到 ,反应的化学方程式为
,反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某工业废液中含有Cu2+、Mg2+、Zn2+等离子,为将其回收利用,采用了如下工艺
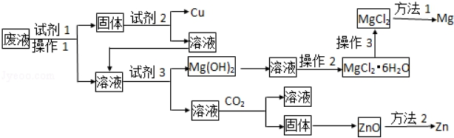
已知Zn(OH)2的性质与Al(OH)3相似,所用试剂在下列试剂中选择
①铁粉 ②锌粉 ③稀HNO3 ④稀H2SO4 ⑤稀HCl ⑥稀氨水 ⑦NaOH溶液 ⑧石灰水
请回答下列问题:
(1)试剂1、试剂2、试剂3分别可以是__________________ (填编号)
(2)操作2依次是______________ 、________________ 、 __________
(3)操作3是________________________________
(4)加过量CO2时发生反应的离子方程式_________________________________
(5)在金属冶炼方法中方法1是______________ 方法2是_____________________ .

已知Zn(OH)2的性质与Al(OH)3相似,所用试剂在下列试剂中选择
①铁粉 ②锌粉 ③稀HNO3 ④稀H2SO4 ⑤稀HCl ⑥稀氨水 ⑦NaOH溶液 ⑧石灰水
请回答下列问题:
(1)试剂1、试剂2、试剂3分别可以是
(2)操作2依次是
(3)操作3是
(4)加过量CO2时发生反应的离子方程式
(5)在金属冶炼方法中方法1是
您最近一年使用:0次



