下列有关实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向某加碘酸钾的食盐溶液中,加入淀粉,并滴入适量硝酸 | 溶液变为蓝色 | 硝酸与碘酸钾反应生成I2 |
| B | 向含相同浓度的KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色 | 氧化性:Cl2>I2,Br2>I2 |
| C | 将Cl2和H2S气体在集气瓶中混合 | 瓶壁上出现黄色固体 | Cl2的氧化性比S强 |
| D | 两支试管各盛4mL0.1mol·L-1酸性高锰酸钾溶液,分别加入2mL0.1mol·L-1草酸溶液和2mL0.2mol·L-1草酸溶液 | 加入0.2mol·L-1草酸溶液的试管中溶液紫色消失更快 | 其他条件相同,反应物浓度越大,反应速率越快 |
| A.A | B.B | C.C | D.D |
更新时间:2023-09-14 23:53:12
|
相似题推荐
【推荐1】硫化氢的转化是资源利用的研究课题。将 和空气的混合气体通入
和空气的混合气体通入 、
、 的混合溶液中反应回收S,反应历程如图。
的混合溶液中反应回收S,反应历程如图。

下列说法正确的是
 和空气的混合气体通入
和空气的混合气体通入 、
、 的混合溶液中反应回收S,反应历程如图。
的混合溶液中反应回收S,反应历程如图。
下列说法正确的是
A.①反应的离子方程式为: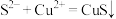 |
B.反应中, 、 、 可以循环利用 可以循环利用 |
C.由反应②③可知氧化性的强弱顺序: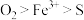 |
D.②反应中每生成64g硫,转移电子数为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】辉钼矿( )是最重要钼矿,它在130℃、高压氧条件下,跟苛性碱溶液发生反应,
)是最重要钼矿,它在130℃、高压氧条件下,跟苛性碱溶液发生反应,
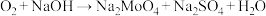 (未配平),下列说法正确的是
(未配平),下列说法正确的是
 )是最重要钼矿,它在130℃、高压氧条件下,跟苛性碱溶液发生反应,
)是最重要钼矿,它在130℃、高压氧条件下,跟苛性碱溶液发生反应,
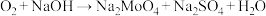 (未配平),下列说法正确的是
(未配平),下列说法正确的是A.上述反应中 是氧化剂, 是氧化剂, 是还原产物 是还原产物 |
B. 中Mo元素化合价为 中Mo元素化合价为 ;氧化性强于 ;氧化性强于 |
C.每生成  反应中转移 反应中转移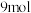  |
D.若通过原电池来实现上述反应,正极的电极反应为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列操作不能达到实验目的的是( )
| 目的 | 操作和现象 | |
| A | 除去溴苯中少量的溴 | 加入适量NaOH溶液,振荡、静置、分液 |
| B | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 |
| C | 氧化性: Cl2>Br2 | 向KBrO3溶液中,加入少量的苯,再通入少量氯气,振荡 |
| D | 探究浓度对速率的影响 | 室温下,向等体积等浓度的两份Na2SO3溶液,同时分别滴加0.1mol·L-1双氧水和1.0mol·L- 1双氧水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】下列有关反应的离子方程式书写错误的是
A.将少量 通入 通入 溶液中: 溶液中: |
B.少量的铁与稀硝酸反应: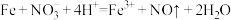 |
C.澄清石灰水中加入足量小苏打: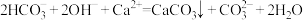 |
D.草酸使酸性高锰酸钾溶液褪色: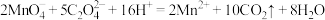 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】如图是用稀HNO3和Cu制取少量NO并验证氮氧化合物性质的装置.下列说法错误的是( )
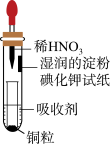

| A.吸收剂可以是NaOH溶液 | B.试管上部的气体始终为无色 |
| C.小试管中溶液最终呈蓝色 | D.试纸先变红后褪色 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】对于反应A(g)+3B(g) 3C(g),可加快物质A化学反应速率的措施是
3C(g),可加快物质A化学反应速率的措施是
 3C(g),可加快物质A化学反应速率的措施是
3C(g),可加快物质A化学反应速率的措施是| A.减小A的物质的量浓度 | B.增大B的物质的量浓度 |
| C.使用催化剂 | D.降低温度 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】某温度下, 的平衡常数
的平衡常数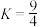 ,该温度下在甲、乙、丙三个恒容密闭容器中,投入
,该温度下在甲、乙、丙三个恒容密闭容器中,投入 和
和 ,其起始浓度如表所示,下列判断不正确的是
,其起始浓度如表所示,下列判断不正确的是
 的平衡常数
的平衡常数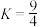 ,该温度下在甲、乙、丙三个恒容密闭容器中,投入
,该温度下在甲、乙、丙三个恒容密闭容器中,投入 和
和 ,其起始浓度如表所示,下列判断不正确的是
,其起始浓度如表所示,下列判断不正确的是| 起始浓度 | 甲 | 乙 | 丙 |
 | 0.010 | 0.020 | 0.020 |
 | 0.010 | 0.010 | 0.020 |
A.平衡时,乙中 的转化率大于60% 的转化率大于60% |
B.平衡时,甲中 的转化率是60%,而丙中 的转化率是60%,而丙中 的转化率<60%, 的转化率<60%, |
| C.反应开始时,丙中的反应速率最快,甲中的反应速率最慢 |
D.平衡时,丙中 是甲中的2倍,是 是甲中的2倍,是 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】如下图所示,在毛玻璃片上放有一张浸有含酚酞的饱和氯化钠溶液的滤纸,滤纸上点有A、B、C、D四个点(指靠近电极的溶液)。有关说法正确的是
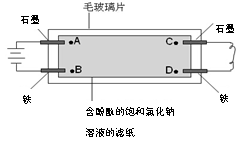

| A.A点比B点先出现红色 | B.B点比A点先出现红色 |
| C.A点比C点先出现红色 | D.D点比C点先出现红色 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列说法正确的是( )
| A.制乙酸丁酯时,可通过及时移去生成的水,提高1-丁醇的转化率 |
| B.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤 |
| C.测定镀锌铁皮厚度时,当将铁皮放入盐酸中至无气泡放出时即认为镀锌层反应完全 |
| D.制乙酸丁酯时,为防止温度过高,可将盛有反应液的试管放在石棉网上方的空气中 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】水合肼(N2H4·H2O)是一种强还原剂,在空气中可吸收CO2而产生烟雾。实验室用NaOH、NaClO的混合液和CO(NH2)2溶液反应并用分液漏斗控制滴加速率的方法进行制备,原理为CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCl,反应装置如图所示(加热和夹持装置略)。下列说法错误的是


| A.配制50g30%的NaOH溶液所需的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管 |
| B.分液漏斗内盛放的液体为CO(NH2)2溶液 |
| C.可根据温度计2的示数判断N2H4·H2O是否开始蒸出 |
| D.碱石灰的主要作用是防止空气中的CO2进入装置 |
您最近一年使用:0次

 溶液
溶液

 溶液中通入
溶液中通入


