周期表中VA族元素及其化合物应用广泛。氨是重要的化工原料,工业合成氨反应中每生成1molNH3,释放92.3kJ热量。“长征二号”运载火箭采用C2H8O2/N2O4作发动机推进剂,燃烧产物无污染。LiFePO4常作锂电池的正极材料,电池充电时,LiFePO4脱出部分Li+,形成Li1-xFePO4。砷化镓(GaAs)是制备第三代半导体材料Ga2O3的重要原料。下列说法正确的是


| A.NH3和NCl3都是非极性分子 | B.1mol磷酸根离子中含4mol 键 键 |
| C.Fe2+的外围电子排布式为3d54s1 | D.GaAs晶胞如图,距离As最近的As原子数为4 |
更新时间:2023-10-19 13:52:20
|
相似题推荐
【推荐1】草酸铁铵的制备原理为Fe(OH)3+3NH4HC2O4=(NH4)3Fe(C2O4)3+3H2O,下列说法正确的是
| A.NH4HC2O4中的组成元素的第一电离能大小为O>N>C>H |
| B.铁元素属于过渡元素,位于元素周期表的ds区 |
| C.草酸铁铵中的Fe元素呈+3价,Fe3+的价电子排布式为3d34s2 |
| D.(NH4)3Fe(C2O4)3中含有离子键、极性键和非极性键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
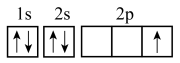
【推荐2】对核外电子运动状态的描述,较为全面的是
| A.轨道表达式 | B.电子式 | C.电子排布式 | D.结构示意图 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】氮化钠可与水发生反应Na3N+3H2O = 3NaOH+NH3 ↑,下列叙述不正确的是
A.NaOH的电子式为: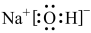 |
| B.H2O是极性分子 |
| C.Na3N中既含离子键也含共价键 |
| D.NH3的空间构型为三角锥形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列叙述正确的是( )
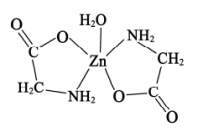
A. 该配合物中配体是H2NCH2CH2NH2,配位数是2。 该配合物中配体是H2NCH2CH2NH2,配位数是2。 |
B.I 离子的空间构型为V形,中心原子的杂化形式为sp3 离子的空间构型为V形,中心原子的杂化形式为sp3 |
| C.CO、CN-等与N2互为等电子体,则CO和CN-的结构式分别为C≡O、C≡N- |
| D.HNO3分子的中心原子的价层电子对数为4,该分子的VSEPR模型是正四面体形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列“类比”结果正确的是
A. 和 和 的原子总数、价电子总数均相等,故二者的性质完全相同 的原子总数、价电子总数均相等,故二者的性质完全相同 |
B. 为含极性键的非极性分子,则 为含极性键的非极性分子,则 也是含极性键的非极性分子 也是含极性键的非极性分子 |
C. 可以溶解在浓氨水中,则 可以溶解在浓氨水中,则 也可以溶解在浓氨水中 也可以溶解在浓氨水中 |
D. 的空间构型为正四面体型,则 的空间构型为正四面体型,则 碳骨架的空间构型为正四面体型 碳骨架的空间构型为正四面体型 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氮及其化合物在催化剂“铁素体”和催化剂“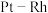 ”作用下发生转化的过程如图所示,下列分析合理的是
”作用下发生转化的过程如图所示,下列分析合理的是
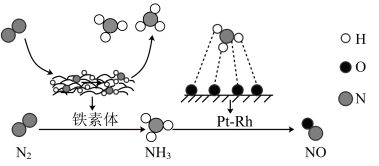
 ”作用下发生转化的过程如图所示,下列分析合理的是
”作用下发生转化的过程如图所示,下列分析合理的是
A. 与O的反应属于氮的固定过程 与O的反应属于氮的固定过程 |
| B.铁素体表面发生了非极性共价键的断裂和极性共价键的形成 |
C. 表面发生了非极性分子和极性分子的转化 表面发生了非极性分子和极性分子的转化 |
D.铁素体作用下的转化涉及电子转移, 作用下的转化不涉及电子转移 作用下的转化不涉及电子转移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 是球形分子,每个碳原子用3个电子与周围的碳原子形成
是球形分子,每个碳原子用3个电子与周围的碳原子形成 键,剩余的1个电子用于形成大
键,剩余的1个电子用于形成大 键。由
键。由 分子构成的晶体其晶胞属于面心立方结构(晶胞的边长为cpm),下列说法正确的是
分子构成的晶体其晶胞属于面心立方结构(晶胞的边长为cpm),下列说法正确的是

 是球形分子,每个碳原子用3个电子与周围的碳原子形成
是球形分子,每个碳原子用3个电子与周围的碳原子形成 键,剩余的1个电子用于形成大
键,剩余的1个电子用于形成大 键。由
键。由 分子构成的晶体其晶胞属于面心立方结构(晶胞的边长为cpm),下列说法正确的是
分子构成的晶体其晶胞属于面心立方结构(晶胞的边长为cpm),下列说法正确的是
A.1个 分子中有90个 分子中有90个 键 键 |
B.在 晶体中, 晶体中, 的配位数为8 的配位数为8 |
C. 晶体的密度为 晶体的密度为 |
D.假设 为理想球形,该球半径为 为理想球形,该球半径为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某二元半导体材料的立方晶胞如图所示,已知晶胞参数为anm,NA为阿伏加德罗常数的值。下列说法不正确的是

| A.该晶胞所表示的物质的化学式为MgSi |
| B.晶体中每个Si周围等距且紧邻的Si有12个 |
C.该晶体中两个Mg间的最短距离为 |
D.该晶体的密度为 |
您最近一年使用:0次

 、
、

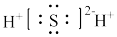
 的
的 模型
模型 溶液中通入足量
溶液中通入足量 ,无明显现象
,无明显现象 溶液中滴加
溶液中滴加 溶液,紫色褪去
溶液,紫色褪去 和单质溴混合,在一定条件下发生加成反应,可生成3种有机物
和单质溴混合,在一定条件下发生加成反应,可生成3种有机物 ,液流方向改变
,液流方向改变
 和干冰的化学式中,中心原子都是IVA主族元素,所以晶体类型相同
和干冰的化学式中,中心原子都是IVA主族元素,所以晶体类型相同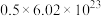
 晶体中含有
晶体中含有

