下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)基态n原子中,核外电子占据最高能层的符号是___________ ,
(2)基态i原子,电子占据最高能级的电子云轮廓图的形状是___________
(3)o元素价层电子的轨道表示式为___________ 。
(4)Li+与H-具有相同的电子结构,两离子半径大小关系为: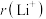 小于
小于 ,原因是
,原因是___________ 。
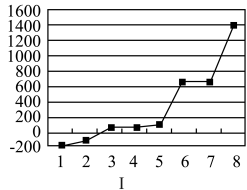
(5)第三周期8种元素按单质熔点高低的顺序如图Ⅰ所示,其中电负性最大的是___________  填元素符号
填元素符号 。
。
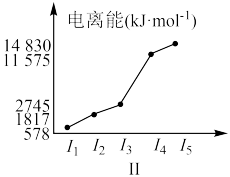
(6)表中所列的某主族元素的电离能情况如图Ⅱ所示,则该元素是___________  填元素符号
填元素符号 。
。
(7)o、p两元素的部分电离能数据列于下表:
比较两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态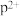 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是___________ 。
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | p | |||||||||||||||
(2)基态i原子,电子占据最高能级的电子云轮廓图的形状是
(3)o元素价层电子的轨道表示式为
(4)Li+与H-具有相同的电子结构,两离子半径大小关系为:
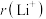 小于
小于 ,原因是
,原因是(5)第三周期8种元素按单质熔点高低的顺序如图Ⅰ所示,其中电负性最大的是
 填元素符号
填元素符号 。
。
(6)表中所列的某主族元素的电离能情况如图Ⅱ所示,则该元素是
 填元素符号
填元素符号 。
。
(7)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p | |
| 电离能/(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态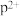 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是
更新时间:2023-09-21 08:37:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素原子的电子层数为n,最外层电子数为2n+1,A、B、C、E每种元素都能与D元素组成两种或两种以上的常见化合物。 回答下列问题:
(1)写出下列各元素符号:C___________ E____________
(2)A和C形成的最简单化合物的电子式为___________ ,A和D按原子数1:1形成的化合物的结构式为___________ 。
(3)已知: BA3DA(g)+A2D(g)=BD2(g)+3A2(g) △H= +49.0kJ/mol
BA3DA(g)+1/2D2(g)=BD2(g)+2A2(g) △H = 一192.9kJ/mol
试写出:气态BA3DA完全燃烧生成气态A2D的热化学方程式(用推出的元素符号写,下同)
______________________________________________________________ 。
利用该燃烧反应设计成的燃料电池正逐步得到推广,请写出该燃料电池负极电极反应式(电解质溶液为KOH):___________________________________________ 。
(1)写出下列各元素符号:C
(2)A和C形成的最简单化合物的电子式为
(3)已知: BA3DA(g)+A2D(g)=BD2(g)+3A2(g) △H= +49.0kJ/mol
BA3DA(g)+1/2D2(g)=BD2(g)+2A2(g) △H = 一192.9kJ/mol
试写出:气态BA3DA完全燃烧生成气态A2D的热化学方程式(用推出的元素符号写,下同)
利用该燃烧反应设计成的燃料电池正逐步得到推广,请写出该燃料电池负极电极反应式(电解质溶液为KOH):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、W是原子序数依次增大的短周期主族元素,X、Z在周期表中的相对位置 如右表所示;X的单质在氧气中燃烧能生成两种无色气体, Y的最简单气态氢化物的水溶液显碱性。

回答下列问题:
(1)元素X在周期表中位于________ 族;W和Z的气态氢化物稳定性比较,其较强的是_______ (填化学式)。
(2)W的单质与水反应生成的含氧酸的电子式为_____________ 。
(3)在BaCl2溶液中加入少量Y的最高价氧化物对应水化物溶液,再通入ZO2气体,能生成无色气体YO和白色沉淀___________ (填化学式);ZO2和YO还原性比较,其较强的是___________ (填化学式)。

回答下列问题:
(1)元素X在周期表中位于
(2)W的单质与水反应生成的含氧酸的电子式为
(3)在BaCl2溶液中加入少量Y的最高价氧化物对应水化物溶液,再通入ZO2气体,能生成无色气体YO和白色沉淀
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】如图为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答问题:
(1)②的最高价氧化物的结构式为_______ 。
(2)④⑥元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:_______ 。
(3)⑤和⑨的简单氢化物的稳定性强弱顺序是_______ (填化学式,用“>”连接)。
(4)写出⑨的单质与⑥的最高价氧化物对应的水化物反应的离子方程式_______ 。
(5)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。Se是第四周期与④同主族的元素,下列推断正确的是_______(填字母)。
(6)元素周期表中,某些主族元素与右下方的主族元素的性质具有相似性,如Be与Al,这种规律称为“对角线原则”。Be(OH)2与NaOH溶液反应的离子方程式为_______ 。
族 周期 | IA | 0 | |||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | ||
2 | ② | ③ | ④ | ⑤ | |||||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)④⑥元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:
(3)⑤和⑨的简单氢化物的稳定性强弱顺序是
(4)写出⑨的单质与⑥的最高价氧化物对应的水化物反应的离子方程式
(5)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。Se是第四周期与④同主族的元素,下列推断正确的是_______(填字母)。
| A.SeO2具有还原性 | B.Se的最低负化合价为-1 |
| C.H2SeO3的酸性强于H2SO4 | D. SeO2在一定条件下可与NaOH溶液反应 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、D、E、G、M ,六种元素位于元素周期表前四周期,原子序数依次增大。其中元素A是宇宙中含量最多的元素,其一种核素原子核内无中子,B的单质既可以由分子组成也可以形成空间网状结构,化合物DE2为通常条件下为红棕色气体, G是前四周期中电负性最小的元素,M的原子最外层只有一个电子,其次外层内的所有轨道的电子均成对。请回答下列问题:
(1)基态G原子的简化电子排布式是_______ ,M在元素周期表中的位置是_______ 。
(2)元素B、D、E的第一电离能由大到小的顺序为_______ (用元素符号表示,下同),电负性由大到小的顺序为_______ 。
(3)M的同周期元素中,核外未成对电子数最多的元素的价层电子轨道表示式_______ 。
(4)写出由A、B、D、E四种元素组成的,最简单的、具有两性的共价化合物的结构简式_______ 。
(1)基态G原子的简化电子排布式是
(2)元素B、D、E的第一电离能由大到小的顺序为
(3)M的同周期元素中,核外未成对电子数最多的元素的价层电子轨道表示式
(4)写出由A、B、D、E四种元素组成的,最简单的、具有两性的共价化合物的结构简式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】I.下列说法中正确的是_______ 。
A.丙烯分子中有8个σ键,1个π键
B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C.NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力
D.NCl3和BC13分子中,中心原子都采用sp3杂化
Ⅱ.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”。试回答下列问题:
(1)Ti元素在元素周期表中的位置是第______ 周期第________ 族,
其基态原子的电子排布式为________ 。
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如图所示,它的化学式是___________ ,其中Ti4+的氧配位数为_________ ,Ba2+的氧配位数为_________ ;

(3)常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,所以TiCl4应是________ 化合物,其固体是____ 晶体。TiCl4在潮湿空气中易挥发,水解而冒白烟,这是因为水解后有________ 生成。
(4)已知Ti3+可形成配位数为6的配合物,其空间构型为正八面体,如下图1所示,我们通常可以用下图2所示的方法来表示其空间构型(其中A表示配体,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空间构型也为八面体型,它有_______ 种同分异构体,请在下图方框中将其画出____ 。

A.丙烯分子中有8个σ键,1个π键
B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C.NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力
D.NCl3和BC13分子中,中心原子都采用sp3杂化
Ⅱ.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”。试回答下列问题:
(1)Ti元素在元素周期表中的位置是第
其基态原子的电子排布式为
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如图所示,它的化学式是

(3)常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,所以TiCl4应是
(4)已知Ti3+可形成配位数为6的配合物,其空间构型为正八面体,如下图1所示,我们通常可以用下图2所示的方法来表示其空间构型(其中A表示配体,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空间构型也为八面体型,它有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E是原子序数依次增大的前四周期元素。已知A元素基态原子的核外电子分占四个原子轨道;B元素基态原子的成对电子数是未成对电子数的6倍;C元素是同周期元素中电负性最大的元素;D元素基态原子的L层与M层的电子数相等,且与s能级的电子总数相等;E元素可与C元素形成2种常见化合物,其中一种为棕黄色,另一种为浅绿色。
请回答下列问题:
(1)E元素基态原子的价层电子排布式为________ ,属于________ 区的元素。
(2)A、B两元素的氧化物的晶体类型分别为________ 、________ ;写出B元素的最高价氧化物与HF溶液反应的化学方程式:_____________________________ 。
(3)元素A的一种氢化物是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,该分子中σ键和π键的数目分别为________ 和________ 。
(4)原子总数和价电子总数都相同的分子、离子或基团属于等电子体,由A~E中的元素形成的微粒中,与SO42-互为等电子体的分子是________ (填分子式,任写一种),SO42-中的键角为________ 。
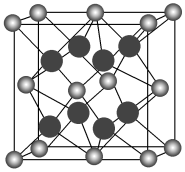
(5)D元素与最活泼的非金属元素形成的化合物的晶胞结构如图所示,其中“ ”代表的微粒是
”代表的微粒是________ (用元素符号或离子符号表示),该离子化合物晶体的密度为a g/cm3,则晶胞的体积是________ (写出表达式即可)。
请回答下列问题:
(1)E元素基态原子的价层电子排布式为
(2)A、B两元素的氧化物的晶体类型分别为
(3)元素A的一种氢化物是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,该分子中σ键和π键的数目分别为
(4)原子总数和价电子总数都相同的分子、离子或基团属于等电子体,由A~E中的元素形成的微粒中,与SO42-互为等电子体的分子是
(5)D元素与最活泼的非金属元素形成的化合物的晶胞结构如图所示,其中“
 ”代表的微粒是
”代表的微粒是
您最近一年使用:0次
【推荐1】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。基态A元素原子的价电子排布式为 ;C元素为最活泼的非金属元素;D元素原子核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素原子核外有三个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素基态的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能
(2)基态D元素原子的价电子排布式为
(3)基态C元素原子的电子排布图为
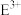 的离子符号为
的离子符号为(4)F元素位于元素周期表的
(5)G元素可能的性质是______(填字母)。
| A.其单质可作为半导体材料 | B.其电负性大于磷 |
| C.其原子半径大于锗 | D.其第一电离能小于硒 |
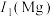
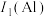 ,其原因是
,其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列小题
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。
基态Co原子简化电子排布式为_____ ,第四电离能I4(Co)_____ I4(Fe)(填“>”或“<”), 的空间构型为
的空间构型为_____ 。
(2)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基配合物。在CO分子中, 键与
键与 键数目之比为
键数目之比为_____ 。
(3)铁与K2O、 (环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,碳原子杂化方式有
(环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,碳原子杂化方式有_____ 。二茂铁熔点为446K,不溶于水,易溶于乙醚、苯、乙醇等有机溶剂,373K即升华;它是典型的_____ 晶体。
(4)Fe催化芳香烃硝化反应时会产生亚硝酰正离子 。试比较
。试比较 亚硝酰正离子与亚硝酸根
亚硝酰正离子与亚硝酸根 的键角大小:
的键角大小:
_____  (选填“>”、“<”或“=”),并利用价层电子对互斥理论(VSEPR)简要解释原因:
(选填“>”、“<”或“=”),并利用价层电子对互斥理论(VSEPR)简要解释原因:_____ 。
(5)铁单质的堆积方式有两种,其剖面图分别如图a、b所示。

在图a所示堆积方式里铁原子的堆积方式为_____ 。在图b所示堆积方式里铁原子的空间利用率为_____ (用含圆周率的代数式表示)。
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。
基态Co原子简化电子排布式为
 的空间构型为
的空间构型为(2)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基配合物。在CO分子中,
 键与
键与 键数目之比为
键数目之比为(3)铁与K2O、
 (环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,碳原子杂化方式有
(环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,碳原子杂化方式有(4)Fe催化芳香烃硝化反应时会产生亚硝酰正离子
 。试比较
。试比较 亚硝酰正离子与亚硝酸根
亚硝酰正离子与亚硝酸根 的键角大小:
的键角大小:
 (选填“>”、“<”或“=”),并利用价层电子对互斥理论(VSEPR)简要解释原因:
(选填“>”、“<”或“=”),并利用价层电子对互斥理论(VSEPR)简要解释原因:(5)铁单质的堆积方式有两种,其剖面图分别如图a、b所示。

在图a所示堆积方式里铁原子的堆积方式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】N、O、S、Cl、Cu五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:
(1)第一电离能:N___________ (填“ ”或“
”或“ ”,下同)O,电负性:S
”,下同)O,电负性:S___________ Cl。
(2)前四周期元素中,未成对电子数为5的元素符号是___________ ;
(3)SO3的空间构型是___________ ,分子中的大 键可用符号
键可用符号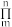 表示,其中m代表参与形成的大
表示,其中m代表参与形成的大 键原子数,n代表参与形成大
键原子数,n代表参与形成大 键的电子数
键的电子数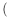 如苯分子中的大
如苯分子中的大 键可表示为
键可表示为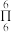 ,则SO3中的大
,则SO3中的大 键应表示为
键应表示为___________ 。
(4)亚硒酸根离子( )的VSEPR模型为
)的VSEPR模型为___________ ;
(5)与 互为等电子体的微粒有
互为等电子体的微粒有___________ 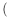 任写两种
任写两种
(1)第一电离能:N
 ”或“
”或“ ”,下同)O,电负性:S
”,下同)O,电负性:S(2)前四周期元素中,未成对电子数为5的元素符号是
(3)SO3的空间构型是
 键可用符号
键可用符号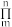 表示,其中m代表参与形成的大
表示,其中m代表参与形成的大 键原子数,n代表参与形成大
键原子数,n代表参与形成大 键的电子数
键的电子数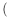 如苯分子中的大
如苯分子中的大 键可表示为
键可表示为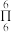 ,则SO3中的大
,则SO3中的大 键应表示为
键应表示为(4)亚硒酸根离子(
 )的VSEPR模型为
)的VSEPR模型为(5)与
 互为等电子体的微粒有
互为等电子体的微粒有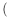 任写两种
任写两种
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】已知A、B、C、D、E是原子序数依次增大的前四周期元素,A是短周期中族序数等于周期数的非金属元素,B元素形成的化合物种类最多;D的最外层电子数与电子层数之比为3∶1;E是第四周期元素,最外层只有一个电子,其余各层电子均充满。请回答下列问题(用元素符号或化学式表示):
(1)E在周期表中位于_____ 区,E+的电子排布式为___________ 。
(2)D元素原子的价层电子排布图为________ ,A2D2的电子式为_______ ,分子中D原子杂化类型为______________ 。
(3)元素B、C、D的第一电离能由大到小的顺序为_____________ ,A分别与B、C、D能形成10电子的化合物,它们的沸点由高到低的顺序是__________ (写分子式)。
(4)C2A4在碱性溶液中能够将ED还原为E2D,已知当1mol C2A4完全参加反应时转移了4 mol电子,则该反应的化学方程式可表示为:___________________ 。
(5)已知EA晶体结构单元如图所示(A原子在体对角线的1/4处),该化合物的密度为ρg·cm-3,阿伏伽德罗常数的值为NA,则该晶胞中E原子与A原子之间的最短距离为_______ cm(用含ρ和NA的式子表示)。

(1)E在周期表中位于
(2)D元素原子的价层电子排布图为
(3)元素B、C、D的第一电离能由大到小的顺序为
(4)C2A4在碱性溶液中能够将ED还原为E2D,已知当1mol C2A4完全参加反应时转移了4 mol电子,则该反应的化学方程式可表示为:
(5)已知EA晶体结构单元如图所示(A原子在体对角线的1/4处),该化合物的密度为ρg·cm-3,阿伏伽德罗常数的值为NA,则该晶胞中E原子与A原子之间的最短距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】O、S、Cl、Fe、Cu、五种元素的单质及其化合物在工农业生产和生活中有着广泛的应用。请回答下列问题:
(1)Fe元素有_______ 种不同运动状态的电子,基态Fe原子价电子的轨道表示式为_______ 。
(2)O、S、Cl的电负性由大到小的顺序是_______ (填元素符号)。
(3)O、S的最简单氢化物中键角较大的是_______ (填化学式),原因是_______ 。
(4) 的空间结构为
的空间结构为_______ 。
(5)O、Cu组成的一种化合物的晶胞结构示意图如下。
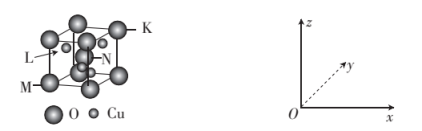
①该化合物的化学式为_______ 。
②原子坐标参数表示了晶胞内部各微粒的相对位置。若原子M、N、K的原子坐标参数分别为(0,0,0)、( ,
, ,
, )、(1,1,1),则L坐标参数为
)、(1,1,1),则L坐标参数为_______ 。
③晶胞边长:描述晶胞的大小和形状。若晶胞边长为anm,设NA为阿伏加德罗常数的值,该化合物的密度为_______ (用含a、NA的代数式表示) 。
。
(1)Fe元素有
(2)O、S、Cl的电负性由大到小的顺序是
(3)O、S的最简单氢化物中键角较大的是
(4)
 的空间结构为
的空间结构为(5)O、Cu组成的一种化合物的晶胞结构示意图如下。
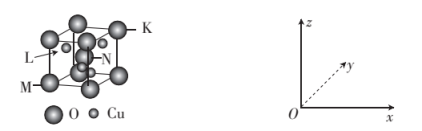
①该化合物的化学式为
②原子坐标参数表示了晶胞内部各微粒的相对位置。若原子M、N、K的原子坐标参数分别为(0,0,0)、(
 ,
, ,
, )、(1,1,1),则L坐标参数为
)、(1,1,1),则L坐标参数为③晶胞边长:描述晶胞的大小和形状。若晶胞边长为anm,设NA为阿伏加德罗常数的值,该化合物的密度为
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】硅晶体常用作太阳能电池材料。
(1)硅在元素周期表中的位置为___________ ,硅的基态原子的电子排布式为___________ 。
(2)GaAlAs也可作太阳能电池材料,同周期元素As(ⅤA族)的第一电离能___________ Se(ⅥA族)的第一电离能(填“>”“<”或“=”),原因是___________ 。基态Ga原子核外电子占据的最高能级为___________ 。
(3)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。

①化合物Ⅲ也是一种汞解毒剂,下列说法正确的有___________ 。
A.在Ⅰ中S原子采取 杂化 B.在Ⅱ中O元素的电负性最大
杂化 B.在Ⅱ中O元素的电负性最大
C.在Ⅲ中C-C-C键角是180° D.在Ⅳ中硫氧键的键能均相等
②汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是___________ 。
③化合物Ⅳ(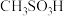 )是一种强酸,写出其电离方程式
)是一种强酸,写出其电离方程式___________ 。
(1)硅在元素周期表中的位置为
(2)GaAlAs也可作太阳能电池材料,同周期元素As(ⅤA族)的第一电离能
(3)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。

①化合物Ⅲ也是一种汞解毒剂,下列说法正确的有
A.在Ⅰ中S原子采取
 杂化 B.在Ⅱ中O元素的电负性最大
杂化 B.在Ⅱ中O元素的电负性最大C.在Ⅲ中C-C-C键角是180° D.在Ⅳ中硫氧键的键能均相等
②汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是
③化合物Ⅳ(
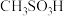 )是一种强酸,写出其电离方程式
)是一种强酸,写出其电离方程式
您最近一年使用:0次



