某小组同学探究 与新制
与新制 悬浊液的反应。
悬浊液的反应。
资料: 为白色固体,难溶于水,能溶于浓盐酸;能与氨水反应生成
为白色固体,难溶于水,能溶于浓盐酸;能与氨水反应生成 ,该物质在空气中会立即被氧化成
,该物质在空气中会立即被氧化成 而使溶液显蓝色。
而使溶液显蓝色。
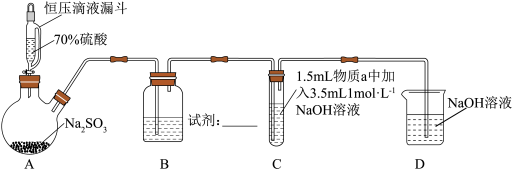
(1)装置B的作用是控制 气体的流速,则B中试剂是
气体的流速,则B中试剂是_____ 。
(2)通入 前,实验Ⅰ、Ⅱ中产生蓝色絮状沉淀的离子方程式为
前,实验Ⅰ、Ⅱ中产生蓝色絮状沉淀的离子方程式为_____ 。
(3)实验Ⅰ通入 后产生砖红色沉淀
后产生砖红色沉淀 ,该反应的化学方程式为
,该反应的化学方程式为_____ 。分析实验Ⅰ一段时间后砖红色沉淀消失的可能原因_____ 。
(4)同学们对实验Ⅱ中白色沉淀的成分继续探究。
①甲同学取少量白色沉淀,洗净后加入氨水,得到蓝色溶液,此过程中反应的离子方程式为: 、
、_____ 。
②乙同学用另一种方法证明了该白色沉淀为 ,实验方案如下:
,实验方案如下:
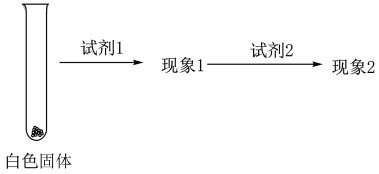
填写下表空格:
(5)实验Ⅰ和实验Ⅱ中 与新制
与新制 悬浊液均发生了
悬浊液均发生了_____ 反应,反应现象的不同与_____ 有关。
 与新制
与新制 悬浊液的反应。
悬浊液的反应。资料:
 为白色固体,难溶于水,能溶于浓盐酸;能与氨水反应生成
为白色固体,难溶于水,能溶于浓盐酸;能与氨水反应生成 ,该物质在空气中会立即被氧化成
,该物质在空气中会立即被氧化成 而使溶液显蓝色。
而使溶液显蓝色。
| 序号 | 物质a | C中实验现象 | |
通入 前 前 | 通入 后 后 | ||
| Ⅰ |   溶液 溶液 | 产生蓝色絮状沉淀 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| Ⅱ |   溶液 溶液 | 产生蓝色絮状沉淀 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)装置B的作用是控制
 气体的流速,则B中试剂是
气体的流速,则B中试剂是(2)通入
 前,实验Ⅰ、Ⅱ中产生蓝色絮状沉淀的离子方程式为
前,实验Ⅰ、Ⅱ中产生蓝色絮状沉淀的离子方程式为(3)实验Ⅰ通入
 后产生砖红色沉淀
后产生砖红色沉淀 ,该反应的化学方程式为
,该反应的化学方程式为(4)同学们对实验Ⅱ中白色沉淀的成分继续探究。
①甲同学取少量白色沉淀,洗净后加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:
 、
、②乙同学用另一种方法证明了该白色沉淀为
 ,实验方案如下:
,实验方案如下:
填写下表空格:
| 试剂1 | 试剂2 | 蒸馏水 | |
| 现象1 | 现象2 |
(5)实验Ⅰ和实验Ⅱ中
 与新制
与新制 悬浊液均发生了
悬浊液均发生了
2023·陕西渭南·模拟预测 查看更多[2]
更新时间:2023-10-25 06:33:37
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
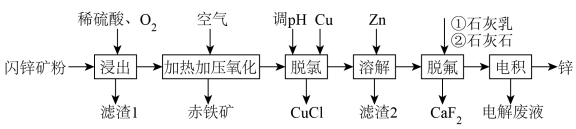
【推荐1】工业利用闪锌矿(主要成分 ZnS,还含有FeS、 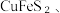 石英及F-、Cl⁻等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
石英及F-、Cl⁻等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
已知:①酸性条件下,亚铜离子易发生歧化反应;② 易形成胶体;③碱性环境下
易形成胶体;③碱性环境下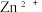 以
以  形式存在。回答下列问题:
形式存在。回答下列问题:
(1)“浸出”前闪锌矿石要碾碎为粉末的原因是___________ 。
(2)“浸出”过程原理如图所示,ZnS“浸出”的总反应化学方程式为___________ 。
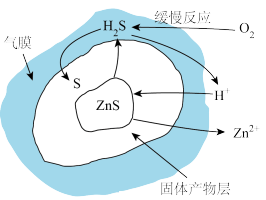
(3)“滤渣1”主要成分为S和___________ ;“加热加压氧化”发生反应的离子方程式为___________ 。
(4)“电积”时,F、Cl⁻会腐蚀电极板,需提前除净。
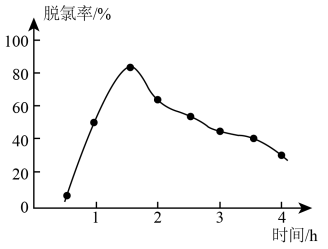
①“脱氯”时,脱氯率随时间变化如图所示,约1.5h后脱氯率减小的原因可能为___________ 。
②“脱氟时,先按物质的量之比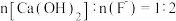 加入
加入  脱氟,充分反应后,
脱氟,充分反应后, 

___________ 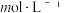 [已知
[已知  且不考虑
且不考虑  沉淀];后加入石灰石,目的为
沉淀];后加入石灰石,目的为___________ 。
(5)写出“电积”生成锌的电极反应式:___________ 。
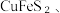 石英及F-、Cl⁻等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
石英及F-、Cl⁻等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
已知:①酸性条件下,亚铜离子易发生歧化反应;②
 易形成胶体;③碱性环境下
易形成胶体;③碱性环境下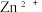 以
以  形式存在。回答下列问题:
形式存在。回答下列问题:(1)“浸出”前闪锌矿石要碾碎为粉末的原因是
(2)“浸出”过程原理如图所示,ZnS“浸出”的总反应化学方程式为

(3)“滤渣1”主要成分为S和
(4)“电积”时,F、Cl⁻会腐蚀电极板,需提前除净。
①“脱氯”时,脱氯率随时间变化如图所示,约1.5h后脱氯率减小的原因可能为

②“脱氟时,先按物质的量之比
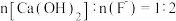 加入
加入  脱氟,充分反应后,
脱氟,充分反应后, 

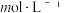 [已知
[已知  且不考虑
且不考虑  沉淀];后加入石灰石,目的为
沉淀];后加入石灰石,目的为(5)写出“电积”生成锌的电极反应式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】某废铁铬催化剂(含 、
、 、MgO、
、MgO、 及少量不溶性杂质)回收铁、铬的工艺流程如下图所示:
及少量不溶性杂质)回收铁、铬的工艺流程如下图所示:

已知:I.已知Cr的金属性强于Fe
II.
III.0.1mol/L金属离子形成氢氧化物沉淀与氢氧化物沉淀溶解的pH范围如下:
(1)加入铁粉发生反应的离子方程式为___________ 。
(2)由滤渣1得到滤液3发生反应的离子方程式为___________ 。
(3)滤渣3成分的化学式为___________ ;回收铬时,铬的存在形式为___________ (填化学式)。
(4)由滤液2得到结晶水合物的操作是___________ 、___________ 、过滤、洗涤、干燥。
(5)滤液2中
___________ mol/L。
(6)滤渣2与 混合后隔绝空气焙烧,总反应的化学方程式为
混合后隔绝空气焙烧,总反应的化学方程式为___________ 。
 、
、 、MgO、
、MgO、 及少量不溶性杂质)回收铁、铬的工艺流程如下图所示:
及少量不溶性杂质)回收铁、铬的工艺流程如下图所示:
已知:I.已知Cr的金属性强于Fe
II.

III.0.1mol/L金属离子形成氢氧化物沉淀与氢氧化物沉淀溶解的pH范围如下:
| 金属离子 |  |  |  |  |  | |||
| 开始沉淀的pH | 1.5 | 4.0 | 4.6 | 7.6 | 9.5 | |||
| 沉淀完全的pH | 2.8 | 5.2 | 6.8 | 9.7 | 11.1 | |||
| 金属氢氧化物 |  |  | ||||||
| 开始溶解的pH | 7.8 | 12 | ||||||
| 溶解完全的pH | 10.8 | >14 | ||||||
(2)由滤渣1得到滤液3发生反应的离子方程式为
(3)滤渣3成分的化学式为
(4)由滤液2得到结晶水合物的操作是
(5)滤液2中

(6)滤渣2与
 混合后隔绝空气焙烧,总反应的化学方程式为
混合后隔绝空气焙烧,总反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】叠氨化钠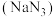 是制备医药、炸药的一种重要原料,
是制备医药、炸药的一种重要原料, 不溶于乙醚,微溶于乙醇,溶于水并能水解。工业上采用“亚硝酸甲酯
不溶于乙醚,微溶于乙醇,溶于水并能水解。工业上采用“亚硝酸甲酯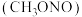 ——水合肼
——水合肼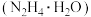 法”制备叠氮化钠的生产流程如下:
法”制备叠氮化钠的生产流程如下:
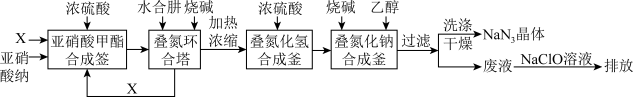
回答下列问题:
(1)叠氮环合塔中生成叠氮化钠的化学方程式为_______ 。
(2)叠氮环合塔中加入的烧碱溶液要适当过量,目的是_______ 。
(3)向“叠氮化钠合成釜”中加入乙醇的目的是_______ ,洗涤操作时选用的洗涤试剂最好的是_______ 。
(4)该生产过程中可循环使用的物质X的结构简式为_______ 。
(5)调节废液的 约为5,加入适量
约为5,加入适量 溶液。
溶液。
① 将废液中的叠氮化钠转化为
将废液中的叠氮化钠转化为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
②研究发现,废液中叠氮化钠去除率随温度升高呈先升后降趋势。当温度大于 时,废水中叠氮化钠去除率随着温度升高而降低,其原因是
时,废水中叠氮化钠去除率随着温度升高而降低,其原因是_______ 。
(6)测定产品 晶体纯度的实验操作如下:取
晶体纯度的实验操作如下:取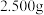 晶体配成
晶体配成 溶液,取
溶液,取 溶液置于锥形瓶中,加入
溶液置于锥形瓶中,加入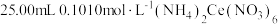 溶液,充分反应后,将溶液稀释,向溶液中加入4mL浓硫酸,滴入3滴指示剂,用
溶液,充分反应后,将溶液稀释,向溶液中加入4mL浓硫酸,滴入3滴指示剂,用 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗溶液体积为
,消耗溶液体积为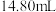 。有关反应为:
。有关反应为: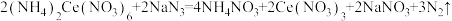 ;
;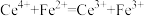 。试样中
。试样中 的质量分数为
的质量分数为_______ (计算结果保留1位小数)。
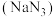 是制备医药、炸药的一种重要原料,
是制备医药、炸药的一种重要原料, 不溶于乙醚,微溶于乙醇,溶于水并能水解。工业上采用“亚硝酸甲酯
不溶于乙醚,微溶于乙醇,溶于水并能水解。工业上采用“亚硝酸甲酯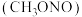 ——水合肼
——水合肼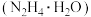 法”制备叠氮化钠的生产流程如下:
法”制备叠氮化钠的生产流程如下:
回答下列问题:
(1)叠氮环合塔中生成叠氮化钠的化学方程式为
(2)叠氮环合塔中加入的烧碱溶液要适当过量,目的是
(3)向“叠氮化钠合成釜”中加入乙醇的目的是
(4)该生产过程中可循环使用的物质X的结构简式为
(5)调节废液的
 约为5,加入适量
约为5,加入适量 溶液。
溶液。①
 将废液中的叠氮化钠转化为
将废液中的叠氮化钠转化为 ,该反应的离子方程式为
,该反应的离子方程式为②研究发现,废液中叠氮化钠去除率随温度升高呈先升后降趋势。当温度大于
 时,废水中叠氮化钠去除率随着温度升高而降低,其原因是
时,废水中叠氮化钠去除率随着温度升高而降低,其原因是(6)测定产品
 晶体纯度的实验操作如下:取
晶体纯度的实验操作如下:取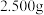 晶体配成
晶体配成 溶液,取
溶液,取 溶液置于锥形瓶中,加入
溶液置于锥形瓶中,加入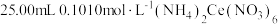 溶液,充分反应后,将溶液稀释,向溶液中加入4mL浓硫酸,滴入3滴指示剂,用
溶液,充分反应后,将溶液稀释,向溶液中加入4mL浓硫酸,滴入3滴指示剂,用 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗溶液体积为
,消耗溶液体积为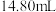 。有关反应为:
。有关反应为: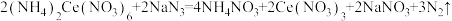 ;
;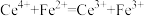 。试样中
。试样中 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】元素周期表中第四周期的某些元素在生产、生活中有着广泛的应用。
(1)硒常用作光敏材料,基态硒原子的价电子排布图为__________ ;与硒同周期的p区元素中第一电离能大于硒的元素有__________ 种;SeO3的空间构型是_______________ 。
(2)科学家在研究金属矿物质组分的过程中,发现了Cu—Ni—Fe等多种金属互化物。确定某种金属互化物是晶体还是非晶体的方法是_____________________________________ 。
(3)镍能与类卤素(SCN)2反应生成Ni(SCN)2。(SCN)2分子中硫原子的杂化方式是__________________ ,σ键和π键数目之比为_____________ 。
(4)Co(NH3)5Cl3是钴的一种配合物,向100mL0.2mol·L-1该配合物的溶液中加入足量AgNO3溶液,生成5.74g白色沉淀,则该配合物的化学式为_____________ ,中心离子的配位数为________________ 。
(5)已知:r(Fe2+)为61pm,r(Co2+)为65pm。在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3的分解温度低于CoCO3,原因是__________________________________ 。
(6)某离子型铁的氧化物晶胞如下图所示,它由X、Y组成,则该氧化物的化学式为________________________ 。已知该晶体的密度为dg·cm-3,阿伏伽德罗常数的值为NA,则该晶体的晶胞参数a=_______ pm(用含d和NA的代数式表示)。

(1)硒常用作光敏材料,基态硒原子的价电子排布图为
(2)科学家在研究金属矿物质组分的过程中,发现了Cu—Ni—Fe等多种金属互化物。确定某种金属互化物是晶体还是非晶体的方法是
(3)镍能与类卤素(SCN)2反应生成Ni(SCN)2。(SCN)2分子中硫原子的杂化方式是
(4)Co(NH3)5Cl3是钴的一种配合物,向100mL0.2mol·L-1该配合物的溶液中加入足量AgNO3溶液,生成5.74g白色沉淀,则该配合物的化学式为
(5)已知:r(Fe2+)为61pm,r(Co2+)为65pm。在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3的分解温度低于CoCO3,原因是
(6)某离子型铁的氧化物晶胞如下图所示,它由X、Y组成,则该氧化物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】(1)基态溴原子的价层电子轨道排布式为________ 。第四周期中,与溴原子未成对电子数相同的金属元素有_______ 种。
(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有___________ (填标号)。
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)Al元素可形成[AlF6]3-、[AlCl4]-配离子,而B元素只能形成[BF4]-配离子,由此可知决定配合物中配位数多少的因素是________________ ;[AlCl4]-的立体构型名称为______ 。
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是________________
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是_________ 。
A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
(5)F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-Cl键的键能(242.7kJ/mol),原因是_________ 。
(6)金属钾的晶胞结构如图。若该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,则表示K原子半径的计算式为______ 。

(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)Al元素可形成[AlF6]3-、[AlCl4]-配离子,而B元素只能形成[BF4]-配离子,由此可知决定配合物中配位数多少的因素是
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是

A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
(5)F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-Cl键的键能(242.7kJ/mol),原因是
(6)金属钾的晶胞结构如图。若该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,则表示K原子半径的计算式为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】锌及锌合金(如黄铜)广泛应用于生产、生活。某小组拟以锌矿(主要成分是ZnS,含少量FeS等杂质)为原料采用多种方法冶炼锌,流程如图。回答下列问题:

已知:① 是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应: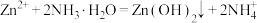 、
、
②常温下,几种金属离子转化成氢氧化物沉淀的pH如表:
(1)已知 中
中 采用
采用 杂化,则
杂化,则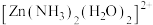 有
有___________ 种结构。
(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内,封裹泥固,……然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红……冷定,毁罐取出。……即倭铅也。”(炉甘石主要成分是 ,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的
,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的___________ (填标号,下同)。从环保的角度来看,这三种方法中,最佳方法是___________ 。
a.半湿法 b.火法 c.全湿法
(3)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入 ,除生成
,除生成 外,还能回收非金属单质。ZnS参与反应的离子方程式为
外,还能回收非金属单质。ZnS参与反应的离子方程式为___________ 。
(4)“氧化,调pH”时试剂A不宜选择NaOH溶液,也不宜选择氨水,原因是___________ 。
(5)“电解沉积”(以惰性材料为电极)时阳极的电极反应式为___________ 。航母外壳常镶嵌一些锌块,这种保护航母的方法叫___________ 。
(6)通常认为离子浓度 时表示该离子已完全除尽。根据表格数据计算
时表示该离子已完全除尽。根据表格数据计算
___________ 。

已知:①
 是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应: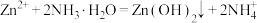 、
、
②常温下,几种金属离子转化成氢氧化物沉淀的pH如表:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
 | 6.5 | 9.7 |
 | 5.4 | 8.0 |
 | 2.3 | 4.1 |
 中
中 采用
采用 杂化,则
杂化,则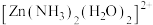 有
有(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内,封裹泥固,……然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红……冷定,毁罐取出。……即倭铅也。”(炉甘石主要成分是
 ,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的
,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的a.半湿法 b.火法 c.全湿法
(3)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入
 ,除生成
,除生成 外,还能回收非金属单质。ZnS参与反应的离子方程式为
外,还能回收非金属单质。ZnS参与反应的离子方程式为(4)“氧化,调pH”时试剂A不宜选择NaOH溶液,也不宜选择氨水,原因是
(5)“电解沉积”(以惰性材料为电极)时阳极的电极反应式为
(6)通常认为离子浓度
 时表示该离子已完全除尽。根据表格数据计算
时表示该离子已完全除尽。根据表格数据计算
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】某校研究性学习小组,探究一定量的浓硫酸与足量锌充分反应产生的气体产物,进行如下实验:按图组装好实验装置,在A中加入5 mL 98%的浓硫酸和足量的锌粒,微热试管A,观察到C、D、E中均有气泡产生;随后气泡量减少,品红溶液褪色,D中先出现浑浊后浑浊消失;反应较长时间后,C、D、E中的气泡量又会明显增加。


试回答:
(1)写出A中从反应开始到停止可能发生反应的化学方程式:_______ 。
(2)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接_______ 、_______ 接b,c接_______ 、_______ 接d。
(3)能证明浓硫酸具有强氧化性的实验现象为_______ 。
(4)D中浑浊消失的离子反应方程式为_______ 。
(5)D、E两支试管中CCl4的作用是_______ 。
(6)若A中Zn足量,充分反应后得到气体的成分是_______ 。


试回答:
(1)写出A中从反应开始到停止可能发生反应的化学方程式:
(2)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接
(3)能证明浓硫酸具有强氧化性的实验现象为
(4)D中浑浊消失的离子反应方程式为
(5)D、E两支试管中CCl4的作用是
(6)若A中Zn足量,充分反应后得到气体的成分是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】【发现问题】研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液。
【实验探究】在体积相同盛满CO2的两集气瓶中,分别加入等体积的饱和石灰水和浓NaOH溶液。实验装置和现象如图所示。请你一起参与。

【现象结论】甲装置中产生该实验现象的化学方程式为______________________ 。解释通常用石灰水而不用NaOH溶液检验CO2的原因________________________________________________ ;乙装置中的实验现象是___________________________ 。吸收CO2较多的装置是__________________ 。
【计算验证】另一位同学小李通过计算发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH。因此,他认为通过吸收CO2应该用饱和石灰水。
【思考评价】请你对小李同学的结论进行评价:________________________________________________________ 。
【实验探究】在体积相同盛满CO2的两集气瓶中,分别加入等体积的饱和石灰水和浓NaOH溶液。实验装置和现象如图所示。请你一起参与。

【现象结论】甲装置中产生该实验现象的化学方程式为
【计算验证】另一位同学小李通过计算发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH。因此,他认为通过吸收CO2应该用饱和石灰水。
【思考评价】请你对小李同学的结论进行评价:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”,请就“三大酸”的性质,回答下列问题:
⑴稀盐酸与铜不反应,但向稀盐酸中加入H2O2后,则可使铜溶解。该反应的化学方程式为________________________________________________________ 。
某同学未加入氧化剂,而是设计了一个实验装置,也能使铜很快溶于稀盐酸.请在下面的方框中画出该装置:

⑵某课外活动小组设计了以下实验方案验证Cu与浓硝酸反应的过程中可能产生NO。其实验流程图如下:

①若要测定NO的体积,从上图所示的装置中,你认为应选用_______ 装置进行Cu与浓硝酸反应实验,选用的理由是____________________________________ 。
②选用如上图所示仪器组合一套可用来测定生成NO体积的装置,其合理的连接顺序是
__________________ (填各导管口编号)。
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置_______ (“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平。
⑶工业制硫酸时,硫铁矿(FeS2)高温下空气氧化产生二氧化硫:4FeS2+11O2→8SO2+2Fe2O3,设空气中N2、O2的含量分别为0.800和0.200(体积分数),4.8t FeS2完全制成硫酸,需要空气的体积(标准状况)为_______ L。
⑴稀盐酸与铜不反应,但向稀盐酸中加入H2O2后,则可使铜溶解。该反应的化学方程式为
某同学未加入氧化剂,而是设计了一个实验装置,也能使铜很快溶于稀盐酸.请在下面的方框中画出该装置:

⑵某课外活动小组设计了以下实验方案验证Cu与浓硝酸反应的过程中可能产生NO。其实验流程图如下:

 |
①若要测定NO的体积,从上图所示的装置中,你认为应选用
②选用如上图所示仪器组合一套可用来测定生成NO体积的装置,其合理的连接顺序是
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置
⑶工业制硫酸时,硫铁矿(FeS2)高温下空气氧化产生二氧化硫:4FeS2+11O2→8SO2+2Fe2O3,设空气中N2、O2的含量分别为0.800和0.200(体积分数),4.8t FeS2完全制成硫酸,需要空气的体积(标准状况)为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】(1)在初中化学课堂上,硫酸铜溶液与氢氧化钠溶液反应可得到蓝色沉淀,将沉淀加热可生成黑色物质,请写出有关反应的化学方程式:①_______________ ,②_______________ 。
(2)某同学也做了这个实验。他在试管中倒入2mL CuSO4溶液,再加入一定量NaOH溶液,结果得到的沉淀并不是蓝色的,而是浅绿色的;将此浊液加热直至沸腾,观察不到有分解变黑生成CuO的迹象。这是为什么呢?该同学通过查找资料得知,该浅绿色沉淀物可能是溶解度极小的碱式硫酸铜,其化学式为Cu4(OH)6SO4
①请写出生成浅绿色沉淀的有关反应的化学方程式:__________________ 。
②请设计一个实验,证明该浅绿色沉淀中含有硫酸根:_________________ 。
(2)某同学也做了这个实验。他在试管中倒入2mL CuSO4溶液,再加入一定量NaOH溶液,结果得到的沉淀并不是蓝色的,而是浅绿色的;将此浊液加热直至沸腾,观察不到有分解变黑生成CuO的迹象。这是为什么呢?该同学通过查找资料得知,该浅绿色沉淀物可能是溶解度极小的碱式硫酸铜,其化学式为Cu4(OH)6SO4
①请写出生成浅绿色沉淀的有关反应的化学方程式:
②请设计一个实验,证明该浅绿色沉淀中含有硫酸根:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某校研究性学习小组选用下图装置组装制备纯净干燥的NH3并探究NH3与CuO发生的反应,同时检验和收集非固态产物。请回答下列问题:

(1)完成实验所需装置按气流方向从左到右的连接顺序为___________________________ 。
(2)连接好装置后应首先____________________________ ,然后添加药品进行实验。
(3)装置A中发生反应的化学方程式为__________________________________ 。
(4)D中盛放碱石灰的仪器名称是________________ ,E装置的作用是___________________ 。
(5)通过进一步检测发现F中收集到的气体是一种常见的单质气体,硬质玻璃管中得到一种固体单质。试描述该小组同学还能观察到的其它现象为:___________________________ ;C中反应的化学方程式为:__________________________________ 。

(1)完成实验所需装置按气流方向从左到右的连接顺序为
(2)连接好装置后应首先
(3)装置A中发生反应的化学方程式为
(4)D中盛放碱石灰的仪器名称是
(5)通过进一步检测发现F中收集到的气体是一种常见的单质气体,硬质玻璃管中得到一种固体单质。试描述该小组同学还能观察到的其它现象为:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】铜及其化合物在工业生产中应用广泛。
Ⅰ.某同学设计如下实验装置测定铜的相对原子质量(夹持和加热仪器已略去),并检验氯气的氧化性。
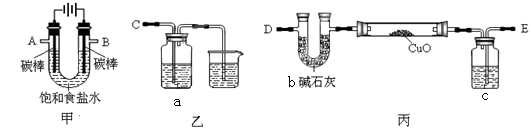
(1)该实验装置的连接顺序为:A连接________ ,B连接________ (填字母)。
(2)乙装置a瓶中的溶液可以是_______
A.NaOH溶液 B.Na2S溶液 C.酸性KMnO4溶液 D.含少量KSCN的FeCl2溶液
(3)对丙装置进行加热前需要________ 。
(4)准确称量 m g CuO进行实验,当CuO完全反应后测出b中增重n g。则Cu的相对原子质量为________ (只要求列出算式)。该实验方案的装置有不合理之处,若不加以改正会导致测定结果________ (填“偏大”、”偏小“或”不变“)。
Ⅱ.研究发现Cu与稀盐酸不反应,但在持续通入空气的条件下可反应生成CuCl2。
(5)已知Fe3+对该反应有催化作用,其催化原理如图所示:
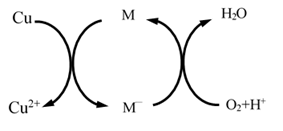
则图中的M‘为________ (填化学符号)
(6)向CuCl2溶液中通入H2S气体,可产生CuS沉淀,反应离子方程式为:Cu2++H2S=CuS(s)+2H+ , 则该反应的平衡常数K=________ (保留一位小数)。已知:CuS溶度积KSP=1.0×10-36 , H2S电离常数Ka1=1.3×10-7 , Ka2=7.0×10-15。
Ⅰ.某同学设计如下实验装置测定铜的相对原子质量(夹持和加热仪器已略去),并检验氯气的氧化性。

(1)该实验装置的连接顺序为:A连接
(2)乙装置a瓶中的溶液可以是
A.NaOH溶液 B.Na2S溶液 C.酸性KMnO4溶液 D.含少量KSCN的FeCl2溶液
(3)对丙装置进行加热前需要
(4)准确称量 m g CuO进行实验,当CuO完全反应后测出b中增重n g。则Cu的相对原子质量为
Ⅱ.研究发现Cu与稀盐酸不反应,但在持续通入空气的条件下可反应生成CuCl2。
(5)已知Fe3+对该反应有催化作用,其催化原理如图所示:

则图中的M‘为
(6)向CuCl2溶液中通入H2S气体,可产生CuS沉淀,反应离子方程式为:Cu2++H2S=CuS(s)+2H+ , 则该反应的平衡常数K=
您最近一年使用:0次



