钙钛矿型材料具有与天然钙矿( )相同的晶体结构,其化学通式为ABX3
)相同的晶体结构,其化学通式为ABX3 通过元素的替换和掺杂,可以调控钙钛矿型材料的催化性能。
通过元素的替换和掺杂,可以调控钙钛矿型材料的催化性能。
(1)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是___________ 。
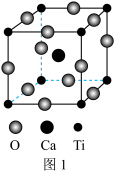
(2)CaTiO3的晶胞如图1所示,其组成元素的电负性大小顺序是___________ ;与每个Ti4+距离最近且相等的 的个数为
的个数为___________ ;金属离子与氧离子间的作用力为___________ , 的配位数是
的配位数是___________ 。
(3)一种立方钙钛矿结构的金属卤化物光电材料的组成为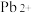 、I-和有机碱离子
、I-和有机碱离子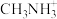
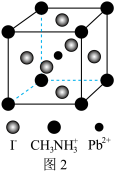
 其晶胞如图2所示。其中
其晶胞如图2所示。其中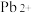 与图1中
与图1中___________ 的空间位置相同,有机碱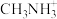 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是___________ ;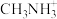 与
与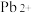 是否形成配位键?
是否形成配位键?___________ 。为什么?___________ 。若晶胞参数为anm,则晶体密度为___________ g∙cm−3(列出计算式)。
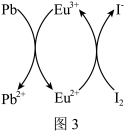
(4)用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了器件效率和使用寿命,我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图3所示,用离子方程式表示该原理:___________ 。
 )相同的晶体结构,其化学通式为ABX3
)相同的晶体结构,其化学通式为ABX3 通过元素的替换和掺杂,可以调控钙钛矿型材料的催化性能。
通过元素的替换和掺杂,可以调控钙钛矿型材料的催化性能。(1)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -2412 | 38.3 | 155 |
 的个数为
的个数为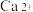 的配位数是
的配位数是
(3)一种立方钙钛矿结构的金属卤化物光电材料的组成为
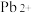 、I-和有机碱离子
、I-和有机碱离子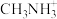
 其晶胞如图2所示。其中
其晶胞如图2所示。其中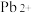 与图1中
与图1中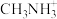 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是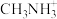 与
与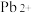 是否形成配位键?
是否形成配位键?
(4)用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了器件效率和使用寿命,我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图3所示,用离子方程式表示该原理:

更新时间:2023-10-31 08:56:08
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】SDIC是一种性能稳定的高效广谱杀菌消毒剂,广泛用于环境水处理、食品加工、公共场所等清洁消毒,结构如图甲所示。其中W、X、Y、R、Z均为短周期元素且原子序数依次增大,Z在同周期主族元素中原子半径最小,且Z与Y位于不同周期。

回答下列问题:
(1)SDIC中,电负性最小的元素是____ (填元素名称) ,其中W最外层的孤电子对数为__________ 。
(2)基态X3-的核外电子排布式为____ 。某离子晶体中含有X3-和M+两种离子,其中M+核外电子正好充满K、L、M3个能层,则M的元素符号是___ ,该晶体晶胞结构如图乙所示,则X3-的配位数为____ 。
(3)X≡X的键能为942kJ/mol,X-X单键的键能为247kJ/mol,则X的最常见单质中____ (填“σ”或“π”)键更稳定。
(4)X的最简单氢化物是___ 分子(填“极性”或“非极性”),该分子与1个H+结合形成离子时键角___ (填“变大”、“变小”或“不变”),原因是____ 。
(5)SDIC的原子发射光谱中呈现特征颜色的微观原因是____ 。
(6)在由R和Y的单核离子组成的晶体中,阴离子的排列方式为面心立方最密堆积,阳离子填充在全部的正四面体空隙中。已知晶胞参数为anm,阿伏加 德罗常数的值为NA,则该晶体密度为____ g/cm3 (列出计算式)。

回答下列问题:
(1)SDIC中,电负性最小的元素是
(2)基态X3-的核外电子排布式为
(3)X≡X的键能为942kJ/mol,X-X单键的键能为247kJ/mol,则X的最常见单质中
(4)X的最简单氢化物是
(5)SDIC的原子发射光谱中呈现特征颜色的微观原因是
(6)在由R和Y的单核离子组成的晶体中,阴离子的排列方式为面心立方最密堆积,阳离子填充在全部的正四面体空隙中。已知晶胞参数为anm,阿伏加 德罗常数的值为NA,则该晶体密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】短周期元素 T、X、Y、Z 的原子序数依次增大,其中元素 T、X 基态原子均有 2 个未成对电子,元素 Y 基态原子 s 能级的电子总数与 p 能级的电子总数相等,元素 Z 的价电子数等于电子层数。元素 W 位于第四周期,其基态原子所含未成对电子数在该周期中最多。
(1)①元素X、Y、Z 的第一电离能由大到小的顺序为_______ 。(用元素符号表示)
②元素W 在周期表中具体位置_______ ,元素 Y 在周期表_______ 区。
(2)T、X分别与氢组成的 T2H2与H2X2分子中,T、X 原子轨道的杂化类型分别是_______ 。
(3)T 与X 可形成TX 离子和 TX2分子。
离子和 TX2分子。
①TX 的空间构型为
的空间构型为_______ (用文字描述)。
②N 离子与 TX2分子互为等电子体,则N
离子与 TX2分子互为等电子体,则N 的电子式为
的电子式为_______ 。
(4)如图是由元素W、Z 两种元素所形成的某种合金的晶胞结构示意图。
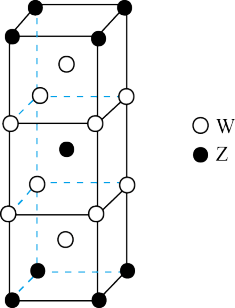
①元素W 基态原子的核外电子排布式为_______ 。
②该合金中W 与 Z 的原子个数比为_______ 。
(1)①元素X、Y、Z 的第一电离能由大到小的顺序为
②元素W 在周期表中具体位置
(2)T、X分别与氢组成的 T2H2与H2X2分子中,T、X 原子轨道的杂化类型分别是
(3)T 与X 可形成TX
 离子和 TX2分子。
离子和 TX2分子。①TX
 的空间构型为
的空间构型为②N
 离子与 TX2分子互为等电子体,则N
离子与 TX2分子互为等电子体,则N 的电子式为
的电子式为(4)如图是由元素W、Z 两种元素所形成的某种合金的晶胞结构示意图。

①元素W 基态原子的核外电子排布式为
②该合金中W 与 Z 的原子个数比为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】著名化学家徐光宪在稀土化学等领域取得了卓越成就,被誉为“稀土界的袁隆平”。稀土元素包括钪、钇和镧系元素。请回答下列问题:
(1)写出基态二价钪离子(Sc2+)电子占据的轨道数为____ 。
(2)在用重量法测定镧系元素和使镧系元素分离时,总是使之先转换成草酸盐,然后经过灼烧而得其氧化物,如2LnCl3+3H2C2O4+nH2O=Ln2(C2O4)3•nH2O+6HCl。
①1molH2C2O4分子中含σ键和π键的数目之比为___ 。
②写出与H2O互为等电子体的一种阴离子的化学式____ 。
③HCl和H2O可以形成相对稳定的水合氢离子盐晶体,如HCl•2H2O,HCl•2H2O中含有H5O ,结构为
,结构为 ,在该离子中,存在的作用力有
,在该离子中,存在的作用力有____ 。
a.非极性键 b.极性键 c.配位键 d.离子键 e.σ键 f氢键 g.范德华力 h.π键 i.金属键
(3)磷青铜是含少量锡、磷的铜合金,某磷青铜晶胞结构如图所示:
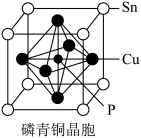
若晶体密度为8.82g/cm3,则最近的Cu原子核间距为___ pm(用含NA的代数式表示)。
(1)写出基态二价钪离子(Sc2+)电子占据的轨道数为
(2)在用重量法测定镧系元素和使镧系元素分离时,总是使之先转换成草酸盐,然后经过灼烧而得其氧化物,如2LnCl3+3H2C2O4+nH2O=Ln2(C2O4)3•nH2O+6HCl。
①1molH2C2O4分子中含σ键和π键的数目之比为
②写出与H2O互为等电子体的一种阴离子的化学式
③HCl和H2O可以形成相对稳定的水合氢离子盐晶体,如HCl•2H2O,HCl•2H2O中含有H5O
 ,结构为
,结构为 ,在该离子中,存在的作用力有
,在该离子中,存在的作用力有a.非极性键 b.极性键 c.配位键 d.离子键 e.σ键 f氢键 g.范德华力 h.π键 i.金属键
(3)磷青铜是含少量锡、磷的铜合金,某磷青铜晶胞结构如图所示:

若晶体密度为8.82g/cm3,则最近的Cu原子核间距为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】黄铁矿(主要成分为FeS2)是工业制硫酸的主要原料。回答下列问题
(1)基态铁原子的价电子排布图_____________ 。
(2) 制硫酸的过程中会产生SO3, SO3的空间构型是_____ 。
(3) 配合物[Fe(H2N-CH2-CH2-NH2)3]SO4的名称是硫酸三乙二胺合铁(II)。 其中的乙二胺 (H2N-CH2-CH2-NH2)是配体。
① [Fe(H2N-CH2-CH2-NH2)3]SO4的晶体类型属于______ ,其 中 C、N、O的电负性由大到小的顺序为______
③乙二胺分于中氮原子的杂化轨道类型是______ 。乙二胺和偏二甲肼(CH3)2NNH2互为同分异构体。乙二胺的沸点117.2℃,偏二甲肼的沸点63℃。两者沸点不同的主要原因是_________________ 。
(4)铁和铜的电离能数据如下表:
第一电离能与第二电离能之间的差值铜比铁大得多的原因是______ 。

(5)铁原子有两种堆积方式,相应地形成两种晶胞(如图甲、乙所示),其中晶胞乙的堆积方式是______ , 晶胞甲中原子的空间利用率为______ (用含 的代数式表示)。
的代数式表示)。
(1)基态铁原子的价电子排布图
(2) 制硫酸的过程中会产生SO3, SO3的空间构型是
(3) 配合物[Fe(H2N-CH2-CH2-NH2)3]SO4的名称是硫酸三乙二胺合铁(II)。 其中的乙二胺 (H2N-CH2-CH2-NH2)是配体。
① [Fe(H2N-CH2-CH2-NH2)3]SO4的晶体类型属于
③乙二胺分于中氮原子的杂化轨道类型是
(4)铁和铜的电离能数据如下表:
铁 | 铜 | |
第一电能能(kJ/mol) | 759 | 746 |
第二电离能(kJ/mol) | 1561 | 1958 |
第一电离能与第二电离能之间的差值铜比铁大得多的原因是

(5)铁原子有两种堆积方式,相应地形成两种晶胞(如图甲、乙所示),其中晶胞乙的堆积方式是
 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
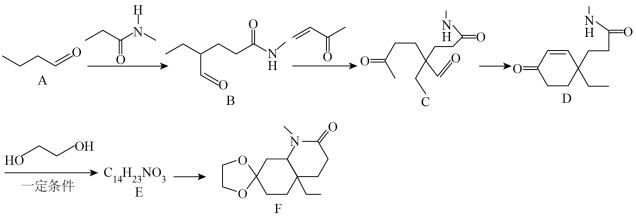
【推荐2】化合物F是一种重要的有机合成中间体,某研究小组按下列路线进行合成:
已知: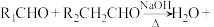
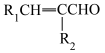
请回答下列问题:
(1)有机物B所含的官能团名称是___________ ,B→C的反应类型为___________ 。
(2)化合物E的结构简式是___________ 。
(3)写出D→E的化学方程式:___________ 。
(4)1分子有机物F分子中含有的手性碳原子数为___________ 。
(5)上述流程涉及的非金属元素中,电负性由大到小的顺序为___________ ,第一电离能最大的为___________ (填元素符号)。
(6)有机物H是D的同分异构体,写出符合下列条件的H的结构简式:___________ (任写一种)。
①IR谱检测表明:分子中含有一个苯环,有 键,无
键,无 、
、 键。
键。
② 谱检测表明:分子中共有5种不同化学环境的氢原子。
谱检测表明:分子中共有5种不同化学环境的氢原子。
③仅含有两种官能团,其中一种为 ,且氨基与苯环直接相连。
,且氨基与苯环直接相连。

已知:
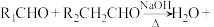
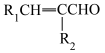
请回答下列问题:
(1)有机物B所含的官能团名称是
(2)化合物E的结构简式是
(3)写出D→E的化学方程式:
(4)1分子有机物F分子中含有的手性碳原子数为
(5)上述流程涉及的非金属元素中,电负性由大到小的顺序为
(6)有机物H是D的同分异构体,写出符合下列条件的H的结构简式:
①IR谱检测表明:分子中含有一个苯环,有
 键,无
键,无 、
、 键。
键。②
 谱检测表明:分子中共有5种不同化学环境的氢原子。
谱检测表明:分子中共有5种不同化学环境的氢原子。③仅含有两种官能团,其中一种为
 ,且氨基与苯环直接相连。
,且氨基与苯环直接相连。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】C、Si在元素周期表中属于同主族元素,其常见的氧化物分别为CO2、SiO2。请回答下列问题:
(1)锗与碳、硅同主族,写出锗原子基态时的核外电子排布式:____________ 。
(2)C、O、Si三种元素的电负性由大到小的顺序为____________ (用元素符号表示)。
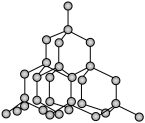
(3)二氧化硅结构跟硅晶体结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察下图中硅晶体的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目为____________ ;晶体硅中硅原子与共价键的数目比为____________ 。
(4)下图是二氧化碳的晶胞模型,从晶体类型来看,CO2属于_______ 晶体。图中显示出的二氧化碳分子数有________ 个,实际上一个二氧化碳晶胞中含有_______ 个二氧化碳分子。标准状况下2.24 L的CO2分子中含有的π键的数目为______ 。
(5)在二氧化碳晶胞中,最近的两个二氧化碳分子间的距离为a nm,NA为阿伏加 德罗常数的值,则晶体密度为____________ g·cm-3。
(1)锗与碳、硅同主族,写出锗原子基态时的核外电子排布式:
(2)C、O、Si三种元素的电负性由大到小的顺序为
(3)二氧化硅结构跟硅晶体结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察下图中硅晶体的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目为
(4)下图是二氧化碳的晶胞模型,从晶体类型来看,CO2属于
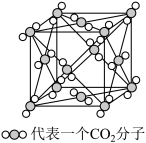
(5)在二氧化碳晶胞中,最近的两个二氧化碳分子间的距离为a nm,NA为阿伏加 德罗常数的值,则晶体密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】工业废水中的亚硝酸盐常常需要处理。回答下列问题:
(1)尿素( )可将
)可将 还原为
还原为 。在尿素分子所含的原子中,第一电离能最大的是
。在尿素分子所含的原子中,第一电离能最大的是_____________ ,其中原子半径最大者的电子排布式为_____________ 。
(2) 离子的空间构型为
离子的空间构型为_______________ ,写出一个 离子的等电子体
离子的等电子体_____________ 。从分子结构角度, 酸性弱于
酸性弱于 的原因是
的原因是____________ 。
(3)尿素中所有原子共平面,据此推断其中 原子的杂化轨道类型为
原子的杂化轨道类型为_____________ 。尿素晶体的熔点为 ,比相同摩尔质量的乙酸熔点(
,比相同摩尔质量的乙酸熔点(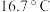 )高
)高 ,这主要是因为尿素分子之间存在更多的
,这主要是因为尿素分子之间存在更多的____________ 。
(4)氨基磺酸( )也可将
)也可将 还原为
还原为 。氨基磺酸结构中接受孤对电子的是
。氨基磺酸结构中接受孤对电子的是_____________ (填“ ”或“
”或“ ”)。
”)。
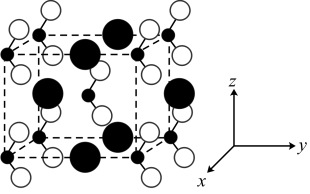
(5)亚硝酸钠晶胞结构如图所示,假设 为阿伏加德罗常数的值,已知晶胞参数
为阿伏加德罗常数的值,已知晶胞参数 (单位为
(单位为 ),则晶体密度d为
),则晶体密度d为_____________  。图示晶胞中
。图示晶胞中 呈体心正交堆积,
呈体心正交堆积, 的原子坐标除
的原子坐标除 外还有
外还有_____________ 。
(1)尿素(
 )可将
)可将 还原为
还原为 。在尿素分子所含的原子中,第一电离能最大的是
。在尿素分子所含的原子中,第一电离能最大的是(2)
 离子的空间构型为
离子的空间构型为 离子的等电子体
离子的等电子体 酸性弱于
酸性弱于 的原因是
的原因是(3)尿素中所有原子共平面,据此推断其中
 原子的杂化轨道类型为
原子的杂化轨道类型为 ,比相同摩尔质量的乙酸熔点(
,比相同摩尔质量的乙酸熔点(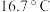 )高
)高 ,这主要是因为尿素分子之间存在更多的
,这主要是因为尿素分子之间存在更多的(4)氨基磺酸(
 )也可将
)也可将 还原为
还原为 。氨基磺酸结构中接受孤对电子的是
。氨基磺酸结构中接受孤对电子的是 ”或“
”或“ ”)。
”)。(5)亚硝酸钠晶胞结构如图所示,假设
 为阿伏加德罗常数的值,已知晶胞参数
为阿伏加德罗常数的值,已知晶胞参数 (单位为
(单位为 ),则晶体密度d为
),则晶体密度d为 。图示晶胞中
。图示晶胞中 呈体心正交堆积,
呈体心正交堆积, 的原子坐标除
的原子坐标除 外还有
外还有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】锰及其化合物的用途非常广泛。回答下列问题:
Ⅰ.一种锰化合物在不同条件下能高效催化 还原为CO或HCOOH,反应如下:
还原为CO或HCOOH,反应如下:

(1)基态Mn原子的价层电子排布为__________ 。含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物,则1mol该锰化合物中通过螯合作用形成的配位键有__________ mol。
(2) 中C的杂化方式为
中C的杂化方式为__________ ,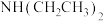 中N的杂化方式为
中N的杂化方式为__________ 。
(3)N、O和C三种元素的第一电离能大小顺序为__________ 。
(4)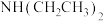 的碱性强于
的碱性强于 的主要原因为
的主要原因为__________ 。
Ⅱ.一种锰氧化物的晶胞结构如图所示。

(5)该锰氧化物的化学式为__________ 。
(6)已知该晶胞参数为a nm,阿伏加德罗常数为 ,则该锰氧化物的摩尔体积
,则该锰氧化物的摩尔体积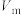 为
为__________  (列出计算式)。
(列出计算式)。
Ⅰ.一种锰化合物在不同条件下能高效催化
 还原为CO或HCOOH,反应如下:
还原为CO或HCOOH,反应如下:
(1)基态Mn原子的价层电子排布为
(2)
 中C的杂化方式为
中C的杂化方式为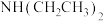 中N的杂化方式为
中N的杂化方式为(3)N、O和C三种元素的第一电离能大小顺序为
(4)
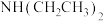 的碱性强于
的碱性强于 的主要原因为
的主要原因为Ⅱ.一种锰氧化物的晶胞结构如图所示。

(5)该锰氧化物的化学式为
(6)已知该晶胞参数为a nm,阿伏加德罗常数为
 ,则该锰氧化物的摩尔体积
,则该锰氧化物的摩尔体积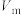 为
为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】AA705合金(含Al、Zn、Mg和Cu)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。但这种合金很难被焊接。最近科学家将碳化钛纳米颗粒(大小仅为十亿分之一米)注入AA7075的焊丝内,让这些纳米颗粒充当连接件之间的填充材料。注入了纳米粒子的填充焊丝也可以更容易地连接其他难以焊接的金属和金属合金。回答下列问题:
(1)基态铜原子的价层电子排布式为__________ 。
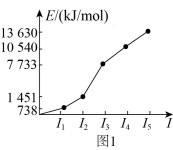
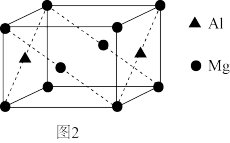
(2)第三周期某元素的前5个电子的电离能如图1所示。该元素是_____ (填元素符号),判断依据是_______ 。
(3)CN—、NH3、H2O和OH—等配体都能与Zn2+形成配离子。1mol [Zn(NH3)4]2+含___ molσ键,中心离子的配位数为_____ 。
(4)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图2所示。1个铝原子周围有_____ 个镁原子最近且等距离。
(5)在二氧化钛和光照条件下,苯甲醇可被氧化成苯甲醛:
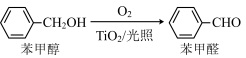
①苯甲醇中C原子杂化类型是__________ 。
②苯甲醇的沸点高于苯甲醛,其原因是__________ 。
(6)钛晶体有两种晶胞,如图所示。
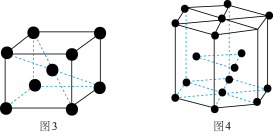
①如图3所示,晶胞的空间利用率为______ (用含п的式子表示)。
②已知图4中六棱柱边长为x cm,高为y cm。该钛晶胞密度为D g·cm-3,NA为______ mol—1(用含x y和D的式子表示)。
(1)基态铜原子的价层电子排布式为
(2)第三周期某元素的前5个电子的电离能如图1所示。该元素是


(3)CN—、NH3、H2O和OH—等配体都能与Zn2+形成配离子。1mol [Zn(NH3)4]2+含
(4)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图2所示。1个铝原子周围有
(5)在二氧化钛和光照条件下,苯甲醇可被氧化成苯甲醛:

①苯甲醇中C原子杂化类型是
②苯甲醇的沸点高于苯甲醛,其原因是
(6)钛晶体有两种晶胞,如图所示。

①如图3所示,晶胞的空间利用率为
②已知图4中六棱柱边长为x cm,高为y cm。该钛晶胞密度为D g·cm-3,NA为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】铜的单质及其化合物在工农业、国防、科技等领域具有广泛应用。回答下列问题:
(1)基态Cu+的价层电子排布式为_______ 。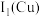
_______ (填“ ”或“
”或“ ”)
”)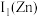 ,原因是
,原因是_______ 。
(2)研究发现,阳离子的颜色与未成对电子数有关。例如:Cu2+、Fe2+、Fe3+等。Cu+呈无色,其原因是_______ 。
(3)合成氨工业中,铜(I)氨溶液常用于除去原料气(N2和H2等)中少量的CO,发生的化学反应为: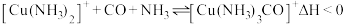 。
。
①NH3分子中N原子的杂化轨道类型是_______ ,NH3和[Cu(NH3)4]2+中H-N-H键角的大小:NH3_______ [Cu(NH3)4]2+ (填“ ”或“
”或“ ”)。
”)。
②铜(Ⅰ)氨液吸收CO适宜的生产条件是_______ (填序号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
③[Cu(NH3)3CO]+配离子中配体是_______ 。
(4)CuCl2与乙二胺(H2NCH2CH2NH2)可形成配离子[Cu(En)2]2+ (En是乙二胺的简写),其结构简式如图所示:
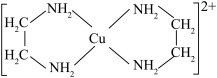
①H2NCH2CH2NH2 (乙二胺)和N(CH3)3(三甲胺)均属于胺,二者相对分子质量相近,但乙二胺的沸点比三甲胺的高得多,原因是_______ 。
②配合物[Cu(En)2]Cl2中不存在的作用力类型有_______ (填选项字母)。
A.配位键 B.极性键 C.离子键 D.非极性键 E.范德华力 F.金属键
(5)金属合金MgCux的结构可看作以Cu4四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置Mg原子(四面体的4个顶点代表Cu原子,圆球代表Mg原子),结构如图所示。

①
_______ 。
②若Mg原子A的原子坐标为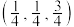 ,则C的原子坐标为
,则C的原子坐标为_______ 。
③晶胞参数为 ,则AB原子之间的距离为
,则AB原子之间的距离为_______ nm。
(1)基态Cu+的价层电子排布式为
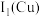
 ”或“
”或“ ”)
”)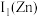 ,原因是
,原因是(2)研究发现,阳离子的颜色与未成对电子数有关。例如:Cu2+、Fe2+、Fe3+等。Cu+呈无色,其原因是
(3)合成氨工业中,铜(I)氨溶液常用于除去原料气(N2和H2等)中少量的CO,发生的化学反应为:
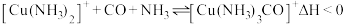 。
。①NH3分子中N原子的杂化轨道类型是
 ”或“
”或“ ”)。
”)。②铜(Ⅰ)氨液吸收CO适宜的生产条件是
A.高温高压 B.高温低压 C.低温高压 D.低温低压
③[Cu(NH3)3CO]+配离子中配体是
(4)CuCl2与乙二胺(H2NCH2CH2NH2)可形成配离子[Cu(En)2]2+ (En是乙二胺的简写),其结构简式如图所示:

①H2NCH2CH2NH2 (乙二胺)和N(CH3)3(三甲胺)均属于胺,二者相对分子质量相近,但乙二胺的沸点比三甲胺的高得多,原因是
②配合物[Cu(En)2]Cl2中不存在的作用力类型有
A.配位键 B.极性键 C.离子键 D.非极性键 E.范德华力 F.金属键
(5)金属合金MgCux的结构可看作以Cu4四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置Mg原子(四面体的4个顶点代表Cu原子,圆球代表Mg原子),结构如图所示。

①

②若Mg原子A的原子坐标为
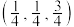 ,则C的原子坐标为
,则C的原子坐标为③晶胞参数为
 ,则AB原子之间的距离为
,则AB原子之间的距离为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】N、A、B、D、E均为原子序数依次递增的前四周期元素,M原子内的电子只有一种运动状态,N原子的双原子分子内的键能在同周期非金属元素的单质中最大,A与B同主族,且A元素的原子序数是B元素原子序数的 ,D属于第IIB的元素,E元素原子的4p轨道上有3个未成对电子。
,D属于第IIB的元素,E元素原子的4p轨道上有3个未成对电子。
(1)A原子核外电子能量最高的能层的符号是_______ ,D原子价电子的排布式为________ 。
(2)设计实验,比较A元素与B元素非金属活泼性__________ 。
(3)NM3的键角________ (填“﹥”“﹤”“=”)EM3的键角,NM3的沸点_______ (填“高于”、“低于”“等于”)EM3的沸点。
(4)与E同周期的主族元素中,第一电离能最大的是_______ (填元素名称)。A和E形成分子的结构如图所示,该分子的分子式为________ ,E原子的杂化类型为_________ 。

(5)与BA2分子的中心原子价电子对几何构型不同但分子构型相同的是_________ 。
A.BeCl2 B.PH3 C.H2O D.OF2
(6)金属D晶体中的原子堆积方式如图所示,这种堆积方式称为_______ ,D原子的配位数为_________ ,六棱柱高为ccm,底边边长为acm,阿伏加德罗常数的值为NA,D晶体的密度为_______ g·cm–3(列出计算式)。

 ,D属于第IIB的元素,E元素原子的4p轨道上有3个未成对电子。
,D属于第IIB的元素,E元素原子的4p轨道上有3个未成对电子。(1)A原子核外电子能量最高的能层的符号是
(2)设计实验,比较A元素与B元素非金属活泼性
(3)NM3的键角
(4)与E同周期的主族元素中,第一电离能最大的是

(5)与BA2分子的中心原子价电子对几何构型不同但分子构型相同的是
A.BeCl2 B.PH3 C.H2O D.OF2
(6)金属D晶体中的原子堆积方式如图所示,这种堆积方式称为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】磷及其化合物是生活生产中重要的组成部分,以下是一些常见的磷的化合物:
(1)与磷同主族、比磷多一个周期的元素基态原子的价层电子排布为___________ .
(2)磷与同周期相邻的两种元素的第一电离能由大到小的顺序为__________ 。(用元素符号表示)。
(3)亚磷酸(H3PO3)是一种常见的无机酸,其与过量的NaOH溶液反应生成Na2HPO3,请画出亚磷酸的分子结构_______ 。亚磷酸可作还原剂将Cu2+还原为单质,得到的电子填充到________ 轨道。
(4)已知PBr5晶体中存在PBr4+,和Br-两种离子,则PBr4+,中心P原子杂化类型为___ ,该离子的几何构型为______ 。而PCl5晶体中存在PCl4+和另一种阴离子,该阴离子配位数为6,请写出该离子的化学式:______ 。PBr5晶体中不能形成与PCl5晶体一样的阴离子的原因可能是:_________ 。
(5)铝和白磷在一定条件下可以制备磷化铝(AlP),磷化铝晶胞的结构如图,可以将其看做Si晶体的“广义等电子体”,可做半导体材料.

①根据“广义等电子原理”,下列物质中,可能是半导体的有____________ .
A. SiC B.CaO2C. GaAs D.Si3N4E.BN
②磷化铝中,Al原子的配位数为_______ ,若该晶胞密度为dg/cm3,用NA表示阿伏伽德罗常数,则该晶体的边长为_______ 。
(1)与磷同主族、比磷多一个周期的元素基态原子的价层电子排布为
(2)磷与同周期相邻的两种元素的第一电离能由大到小的顺序为
(3)亚磷酸(H3PO3)是一种常见的无机酸,其与过量的NaOH溶液反应生成Na2HPO3,请画出亚磷酸的分子结构
(4)已知PBr5晶体中存在PBr4+,和Br-两种离子,则PBr4+,中心P原子杂化类型为
(5)铝和白磷在一定条件下可以制备磷化铝(AlP),磷化铝晶胞的结构如图,可以将其看做Si晶体的“广义等电子体”,可做半导体材料.

①根据“广义等电子原理”,下列物质中,可能是半导体的有
A. SiC B.CaO2C. GaAs D.Si3N4E.BN
②磷化铝中,Al原子的配位数为
您最近一年使用:0次



