在某一恒容容器中发生反应: 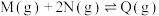 ΔH<0。当反应达到平衡时,改变某一条件,逆反应速率与反应时间的曲线关系如图。下列说法错误的是
ΔH<0。当反应达到平衡时,改变某一条件,逆反应速率与反应时间的曲线关系如图。下列说法错误的是
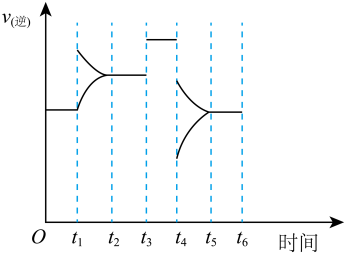
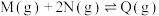 ΔH<0。当反应达到平衡时,改变某一条件,逆反应速率与反应时间的曲线关系如图。下列说法错误的是
ΔH<0。当反应达到平衡时,改变某一条件,逆反应速率与反应时间的曲线关系如图。下列说法错误的是
| A.t1时刻,改变的条件可能是适当升高温度 |
| B.t3~t4内,该反应的正反应速率最大 |
| C.图示中v(逆)保持不变时,该反应处于平衡状态 |
| D.Q(g)的体积分数最高的时间段是0~t1 |
更新时间:2023-11-05 18:53:41
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列实验操作和现象与结论关系不正确 的是
操作和现象 | 结论 | |
| A | 将大小相同的K和Na放入等体积的水中,钾比钠反应剧烈 | 钾元素的金属性比钠元素强 |
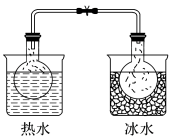
| B | 将Ba(OH)2·8H2O和NH4Cl晶体在小烧杯中混合搅拌,用手触摸烧杯外壁感觉变凉 | Ba(OH)2·8H2O与NH4Cl的反应是吸热反应 |
| C | 在催化剂存在的条件下,石蜡油加强热生成的气体通入溴的四氯化碳溶液中,溶液褪色 | 石蜡油的分解产物都是烯烃 |
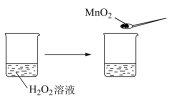
| D | 向盛有H2O2溶液的试管中,加入少量FeCl3溶液,产生气泡的速率比不加FeCl3溶液的快 | FeCl3可以加快H2O2分解的速率,起了催化作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一定温度下,在某固定容积的密闭容器中发生反应: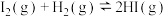 ,改变下列条件,能加快反应速率的是
,改变下列条件,能加快反应速率的是
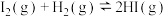 ,改变下列条件,能加快反应速率的是
,改变下列条件,能加快反应速率的是A.充入一定量 | B.充入一定量 ,增大压强 ,增大压强 |
| C.降低温度 | D.分离出 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】温度相同,向甲、乙两体积相同的密闭容器中,各通入2mol SO2和1 mol O2发生反应;
2SO2(g)+O2(g) 2SO3(g)达到平衡时,甲容器中SO2的转化率大于乙容器中SO2的转化率。下列判断正确的是
2SO3(g)达到平衡时,甲容器中SO2的转化率大于乙容器中SO2的转化率。下列判断正确的是
2SO2(g)+O2(g)
 2SO3(g)达到平衡时,甲容器中SO2的转化率大于乙容器中SO2的转化率。下列判断正确的是
2SO3(g)达到平衡时,甲容器中SO2的转化率大于乙容器中SO2的转化率。下列判断正确的是 | A.甲保持压强不变,乙保持体积不变 |
| B.甲保持体积不变,乙保持压强不变 |
| C.混合气体密度甲小于乙 |
| D.混合气体的平均相对分子质量甲小于乙 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知反应: 。起始以物质的量之比为1:1充入反应物,不同压强条件下,
。起始以物质的量之比为1:1充入反应物,不同压强条件下, 的平衡转化率随温度的变化情况如图所示(M、N点标记为▲)。下列有关说法正确的是
的平衡转化率随温度的变化情况如图所示(M、N点标记为▲)。下列有关说法正确的是

 。起始以物质的量之比为1:1充入反应物,不同压强条件下,
。起始以物质的量之比为1:1充入反应物,不同压强条件下, 的平衡转化率随温度的变化情况如图所示(M、N点标记为▲)。下列有关说法正确的是
的平衡转化率随温度的变化情况如图所示(M、N点标记为▲)。下列有关说法正确的是
A.降低温度, 的转化率可达到100% 的转化率可达到100% |
| B.N点时的反应速率一定比M点的快 |
| C.降低温度,该反应平衡常数K一定减小 |
D.从平衡混合气中分离出 和 和 ,可提高 ,可提高 和 和 的利用率 的利用率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】CH4与CO2催化重整可以同时利用两种温室气体,其工艺过程中涉及如下反应:
反应I:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH1=247.4kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=41.2kJ·mol-1
反应Ⅲ:CH4(g)+ O2(g)⇌CO(g)+2H2(g) ΔH3=-35.6 kJ·mol-1
O2(g)⇌CO(g)+2H2(g) ΔH3=-35.6 kJ·mol-1
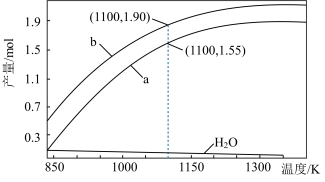
一定条件下,向体积为VL的密闭容器中通入CH4、CO2各1.0mol及少量O2,测得不同温度下反应平衡时各产物产量如图所示。下列说法正确的是
反应I:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH1=247.4kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=41.2kJ·mol-1
反应Ⅲ:CH4(g)+
 O2(g)⇌CO(g)+2H2(g) ΔH3=-35.6 kJ·mol-1
O2(g)⇌CO(g)+2H2(g) ΔH3=-35.6 kJ·mol-1一定条件下,向体积为VL的密闭容器中通入CH4、CO2各1.0mol及少量O2,测得不同温度下反应平衡时各产物产量如图所示。下列说法正确的是

| A.图中曲线b表示H2的平衡产量随温度的变化曲线 |
B.1100K时,CH4与CO2的转化率分别为95%、90%,反应I的平衡常数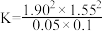 |
| C.反应CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH=206.2kJ·mol-1 |
| D.若选用其它催化剂可能使平衡时H2O的产量随着温度升高而增加 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在密闭容器中进行下列反应:M(g)+N(g) R(g)+2L此反应符合下面图象。下列叙述正确的是
R(g)+2L此反应符合下面图象。下列叙述正确的是
 R(g)+2L此反应符合下面图象。下列叙述正确的是
R(g)+2L此反应符合下面图象。下列叙述正确的是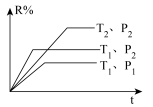
| A.正反应吸热,L是气体 |
| B.正反应吸热,L是固体 |
| C.正反应放热,L是液体 |
| D.正反应放热,L是气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
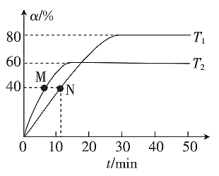
【推荐3】一定温度下,在 恒容密闭容器中充入一定量
恒容密闭容器中充入一定量 和
和 ,发生反应:
,发生反应: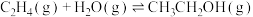
 ,其反应速率
,其反应速率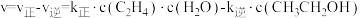 (k是速率常数,只与温度有关)。测得
(k是速率常数,只与温度有关)。测得 的转化率
的转化率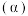 与时间
与时间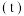 的关系如图所示,其中
的关系如图所示,其中 、
、 均表示温度,下列说法中错误的是
均表示温度,下列说法中错误的是
 恒容密闭容器中充入一定量
恒容密闭容器中充入一定量 和
和 ,发生反应:
,发生反应: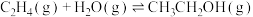
 ,其反应速率
,其反应速率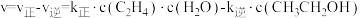 (k是速率常数,只与温度有关)。测得
(k是速率常数,只与温度有关)。测得 的转化率
的转化率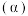 与时间
与时间 的关系如图所示,其中
的关系如图所示,其中 、
、 均表示温度,下列说法中错误的是
均表示温度,下列说法中错误的是
A.温度为 时,M点: 时,M点: |
B.平衡常数: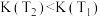 |
C.温度为 时,平衡体系中 时,平衡体系中 |
| D.向反应体系中加入合适的催化剂,能降低反应的活化能,但平衡常数K却保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】反应 2SiHCl3(g) SiH2Cl2(g) + SiCl4(g)在催化剂作用下,于 323 K 和 343 K 时充分反应,SiHCl3的转化率随时间变化的结果如图所示:
SiH2Cl2(g) + SiCl4(g)在催化剂作用下,于 323 K 和 343 K 时充分反应,SiHCl3的转化率随时间变化的结果如图所示:
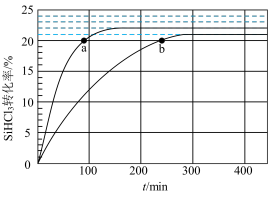
下列说法不正确的是
 SiH2Cl2(g) + SiCl4(g)在催化剂作用下,于 323 K 和 343 K 时充分反应,SiHCl3的转化率随时间变化的结果如图所示:
SiH2Cl2(g) + SiCl4(g)在催化剂作用下,于 323 K 和 343 K 时充分反应,SiHCl3的转化率随时间变化的结果如图所示:
下列说法不正确的是
| A.343 K 时反应物的平衡转化率为 22% |
| B.a、b 处反应速率大小:va>vb |
| C.要提高 SiHCl3转化率,可采取的措施是降温和及时移去反应产物 |
D.已知反应速率 ,k正、k逆分别为正、逆反应速率常数,x为物质的量分数,则 343 K 时 ,k正、k逆分别为正、逆反应速率常数,x为物质的量分数,则 343 K 时  |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,将等物质的量的A、B、C、D四种物质混合于一恒容密闭容器中,发生如下反应:aA(g)+bB(g) cC(g)+dD(s)。当反应进行一段时间后,测得A减少了nmol,B减少了n/2mol,C增加了3n/2mol,D增加了nmol,此时达到化学平衡状态。则下列说法正确的是 ( )
cC(g)+dD(s)。当反应进行一段时间后,测得A减少了nmol,B减少了n/2mol,C增加了3n/2mol,D增加了nmol,此时达到化学平衡状态。则下列说法正确的是 ( )

 cC(g)+dD(s)。当反应进行一段时间后,测得A减少了nmol,B减少了n/2mol,C增加了3n/2mol,D增加了nmol,此时达到化学平衡状态。则下列说法正确的是 ( )
cC(g)+dD(s)。当反应进行一段时间后,测得A减少了nmol,B减少了n/2mol,C增加了3n/2mol,D增加了nmol,此时达到化学平衡状态。则下列说法正确的是 ( )
| A.达到化学平衡时A的消耗速率与C的消耗速率相等 |
| B.保持温度不变,再向容器中充人llmolA和n/2molB,平衡不移动 |
| C.上图表示该反应的正反应速率随时间的变化情况,t1时刻可能是减少了A的浓度,增加了C的浓度 |
| D.保持温度不变,再向容器中充人nmolA和nmolB,A、B的转化率均不变 |
您最近一年使用:0次

 P(g)+Q(g)
P(g)+Q(g)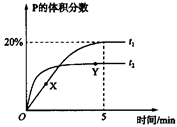
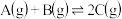
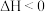 。
。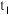 时刻达到平衡后,在
时刻达到平衡后,在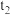 时刻改变条件,其反应过程如图。下列说法正确的是
时刻改变条件,其反应过程如图。下列说法正确的是
 时,
时,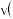 正
正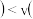 逆
逆


