H2在石墨烯负载型Pd单原子催化剂(Pd/SVG)上还原NO生成N2和 NH3的路径机理及活化能(kJ/mol)如图所示。下列说法错误的是
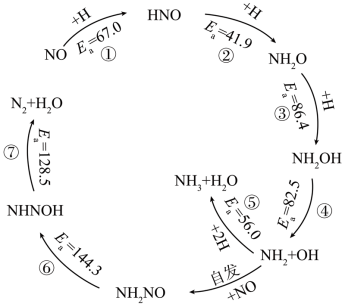
| A.H2还原NO生成N2过程中,速率最慢的步骤为⑥ |
| B.Pd/SVG上H2还原NO, 更容易生成NH3 |
C.根据如图数据可计算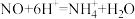 的ΔH 的ΔH |
| D.由图可知,相同催化剂条件下反应可能存在多种反应历程 |
更新时间:2023-11-05 18:53:41
|
相似题推荐
【推荐1】 是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:
第一步 (快反应)
(快反应)
第二步 (慢反应)
(慢反应)
第三步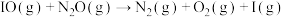 (快反应)
(快反应)
实验表明,含碘时 的分解速率方程
的分解速率方程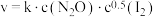 (k为速率常数)。下列表述正确的是
(k为速率常数)。下列表述正确的是
 是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:第一步
 (快反应)
(快反应)第二步
 (慢反应)
(慢反应)第三步
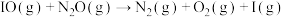 (快反应)
(快反应)实验表明,含碘时
 的分解速率方程
的分解速率方程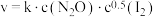 (k为速率常数)。下列表述正确的是
(k为速率常数)。下列表述正确的是| A.IO为反应的中间产物 | B.第一步对总反应速率起决定作用 |
C. 浓度与 浓度与 分解速率无关 分解速率无关 | D.第二步活化能比第三步小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应以回收S,物质循环转化过程如图所示。下列叙述正确的是
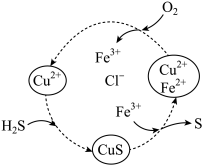

| A.设计循环的目的是降低活化能,减慢总反应速率 |
| B.循环转化过程中有置换反应发生 |
| C.能循环利用的物质只有CuCl2 |
| D.若1mol H2S发生图示转化的同时消耗0.4 molO2,则混合液中Fe3+浓度将减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知反应2NO + 2H2 = N2 + 2H2O的速率方程为υ= kc2(NO)· c(H2)(k为速率常数),其反应历程如下:
① 2NO + H2 → N2+H2O2 慢 ; ② H2O2 + H2 → 2H2O 快
下列说法不正确 的是
① 2NO + H2 → N2+H2O2 慢 ; ② H2O2 + H2 → 2H2O 快
下列说法
| A.升高温度,可提高反应①、②的反应速率 |
| B.c (NO) 、c(H2)增大相同的倍数,对总反应的反应速率的影响程度相同 |
| C.该反应的快慢主要取决于反应① |
| D.可逆反应使用催化剂加快反应速率时,正逆反应的活化能均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 与
与 是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应:
是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应: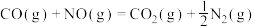
 ,
, ,反应速率较小。有关该反应的说法正确的是
,反应速率较小。有关该反应的说法正确的是
 与
与 是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应:
是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应: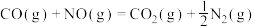
 ,
, ,反应速率较小。有关该反应的说法正确的是
,反应速率较小。有关该反应的说法正确的是A. 与 与 在排入大气之前未反应完全 在排入大气之前未反应完全 |
B.增大压强,平衡将向右移动, |
| C.升高温度,既增大反应速率又增大K |
| D.选用适宜催化剂,可以增大K,使尾气排放达到标准 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实不能用勒夏特列原理解释的是
| A.打开汽水瓶有气泡从溶液中冒出 |
| B.由H2、I2(g)、HI气体组成的平衡减压后颜色变浅 |
| C.实验室用排饱和食盐水法收集氯气 |
| D.合成氨工厂采用增大压强以提高原料的利用率 |
您最近一年使用:0次

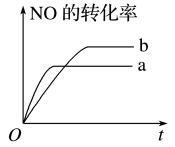
 N2(g)+2CO2(g)+Q(Q>0),图曲线a表示该反应过程中NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是
N2(g)+2CO2(g)+Q(Q>0),图曲线a表示该反应过程中NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是