材料是入类进步的基石,深入认识物质的结构有助于进一步开发新的材料。回答下列问题。
(1)B和Ni均为新材料的主角。
①按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成 。杂化前,处于激发态的B原子的价电子轨道表示式为
。杂化前,处于激发态的B原子的价电子轨道表示式为___________ (填编号)。
A.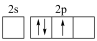 B.
B.  C.
C.  D.
D.
② 常温下呈液态,其分子空间构型为正四面体形。其易溶
常温下呈液态,其分子空间构型为正四面体形。其易溶 、苯等有机溶剂的原因是
、苯等有机溶剂的原因是___________ 。
(2)亚铁氰化钾具有防止食盐结块、保持食盐松散等作用,其化学式为 ,所含元素电负性由大到小的顺序为
,所含元素电负性由大到小的顺序为___________ ,1mol  含有σ键的物质的量为
含有σ键的物质的量为___________ 。
(3)铀氮化合物是核燃料循环系统中的重要物质。已知 。反应所得的气态产物中属于非极性分子的有
。反应所得的气态产物中属于非极性分子的有___________ (填化学式);反应中断裂的化学键有___________ 。(填编号)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(4)某锂电池的负极材料是锂原子嵌入石墨烯层间,其晶胞结构(底边为平行四边形)如图所示。

该晶体的化学式为___________ 。
(1)B和Ni均为新材料的主角。
①按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成
 。杂化前,处于激发态的B原子的价电子轨道表示式为
。杂化前,处于激发态的B原子的价电子轨道表示式为A.
 B.
B.  C.
C.  D.
D.
②
 常温下呈液态,其分子空间构型为正四面体形。其易溶
常温下呈液态,其分子空间构型为正四面体形。其易溶 、苯等有机溶剂的原因是
、苯等有机溶剂的原因是(2)亚铁氰化钾具有防止食盐结块、保持食盐松散等作用,其化学式为
 ,所含元素电负性由大到小的顺序为
,所含元素电负性由大到小的顺序为 含有σ键的物质的量为
含有σ键的物质的量为(3)铀氮化合物是核燃料循环系统中的重要物质。已知
 。反应所得的气态产物中属于非极性分子的有
。反应所得的气态产物中属于非极性分子的有a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(4)某锂电池的负极材料是锂原子嵌入石墨烯层间,其晶胞结构(底边为平行四边形)如图所示。

该晶体的化学式为
更新时间:2023-10-04 22:57:19
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】W、R、X、Y、Z是原子序数依次增大的前四周期元素,其元素性质或原子结构如下表:
请按要求填空:
(1)Y的基态原子有_______ 种不同的运动状态的电子,Z的价电子排布图为______ 。
(2)W、R、X的简单氢化物中,键角由大到小排列的是___________ (用对应的分子式表示),原因是___________ 。
(3)已知:羧酸的酸性可用pKa(pKa=−lgKa)的大小来衡量,pKa越小,酸性越强。
由表可见,酸性:三氯乙酸___________ 三氟乙酸(填“大于”“小于”或“等于”),从键的极性角度解释原因:___________ 。
| 元素 | 元素性质或原子结构 |
| W | 基态原子L能层所有能级上电子数相同 |
| R | 第二周期元素基态原子中未成对电子最多 |
| X | 基态原子核外s能级上电子总数与p能级上电子总数相等,且第一电离能低于同周期相邻元素 |
| Y | 次外层电子数是最外层电子数的2倍 |
| Z | 最外层只有1个电子,其他内层各能级所有轨道电子均成对 |
(1)Y的基态原子有
(2)W、R、X的简单氢化物中,键角由大到小排列的是
(3)已知:羧酸的酸性可用pKa(pKa=−lgKa)的大小来衡量,pKa越小,酸性越强。
| 羧酸 | pKa |
| 三氯乙酸(CCl3COOH) | 0.65 |
| 三氟乙酸(CF3COOH) | 0.23 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有A、B、C、D、E、F、G七种前四周期元素,G的原子序数最大。已知:A、B、C三种元素的原子次外层电子排布都是(n-1)s2(n-1)p6;D、E、F三种元素的原子序数分别等于A、B、C的最外层电子数;G元素原子的最外层电子数和A相同,内层电子数均符合2n2;C的气态单质在标准状况下的密度为3.17g·L-1;A与C能形成离子化合物AC,A离子比C离子少一个能层;E原子的最外电子层中p能级的电子数等于前一能层的电子总数。回答下列问题:
(1)上述元素的基态原子中,含有2个未成对电子的元素是___________ (填元素符号);它们位于元素周期表的___________ 区。
(2)A与D能形成离子化合物AD,则AD的电子式是___________ 。
(3)F元素基态原子最外层电子的轨道表示式为___________ ;G元素基态原子的电子排布式为___________ 。
(1)上述元素的基态原子中,含有2个未成对电子的元素是
(2)A与D能形成离子化合物AD,则AD的电子式是
(3)F元素基态原子最外层电子的轨道表示式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F基态原子的核外电子排布式为______________________ 。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是___________ (用元素符号回答)。
(3)元素B的简单气态氢化物的沸点___________ (填“高于”或“低于”)元素A的简单气态氢化物的沸点,其主要原因是______________________ 。
(4)由A、B、C形成的离子CAB−与AC2互为等电子体,则CAB−的结构式为___________ 。
(5)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为___________ 。

(6)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因______________________ 。
(1)F基态原子的核外电子排布式为
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是
(3)元素B的简单气态氢化物的沸点
(4)由A、B、C形成的离子CAB−与AC2互为等电子体,则CAB−的结构式为
(5)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为

(6)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】高锰酸钾(KMnO4)被广泛用作氧化剂、消毒剂、水处理剂等。回答下列问题:
(1)基态锰原子的价电子排布式是_________ ,含有_________ 个未成对电子。
(2)高锰酸钾中各元素电负性的大小顺序为_________ 。
(3)已知元素Mn与Fe的第三电离能分别为:I3(Mn)=3248kJ/mol、I3(Fe)=2957kJ/mol,I3(Mn)>I3(Fe)的原因是_________ 。
(4)氧与硫位于相同主族,它们的最简单氢化物的沸点较高的是_________ ,其原因是_________ 。过氧化氢中氧原子的杂化方式为_________ 。
(5)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,如图所示。晶胞中K、I、O分别处于顶角、体心、面心位置,晶胞参数为a=0.446nm。

①距离K最近且距离相等的O有_________ 个;
②与I距离最近的O形成的空间构型为_________ 。
③已知A坐标(0,0,0),B坐标(1,1,1),则I的坐标为_________ ;
④与I距离最近的钾为_________ nm(已知 =1.732,计算结果保留小数点后三位有效数字)。
=1.732,计算结果保留小数点后三位有效数字)。
(1)基态锰原子的价电子排布式是
(2)高锰酸钾中各元素电负性的大小顺序为
(3)已知元素Mn与Fe的第三电离能分别为:I3(Mn)=3248kJ/mol、I3(Fe)=2957kJ/mol,I3(Mn)>I3(Fe)的原因是
(4)氧与硫位于相同主族,它们的最简单氢化物的沸点较高的是
(5)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,如图所示。晶胞中K、I、O分别处于顶角、体心、面心位置,晶胞参数为a=0.446nm。

①距离K最近且距离相等的O有
②与I距离最近的O形成的空间构型为
③已知A坐标(0,0,0),B坐标(1,1,1),则I的坐标为
④与I距离最近的钾为
 =1.732,计算结果保留小数点后三位有效数字)。
=1.732,计算结果保留小数点后三位有效数字)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】高氯酸三碳酰肼合镍{[Ni(CHZ)3](C104)2}是一种新型的起爆药。
(1)Ni2+核外电子排布式为___ 。
(2)ClO4-空间构型是___ ;与ClO4-互为等电子体的一种分子为___ (填化学式)。
(3)化学式中CHZ为碳酰肼,组成为CO(N2H3)2,碳酰肼中碳原子的杂化轨道类型为___ ;C、N、O三种元素的电负性由大到小的顺序为___ 。
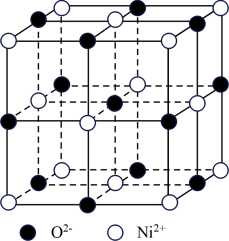
(4)高氯酸三碳酰肼合镍可由NiO、高氯酸及碳酰肼化合而成。NiO的晶胞结构如图所示,晶胞中含有的Ni2+数目为___ 。
(1)Ni2+核外电子排布式为
(2)ClO4-空间构型是
(3)化学式中CHZ为碳酰肼,组成为CO(N2H3)2,碳酰肼中碳原子的杂化轨道类型为
(4)高氯酸三碳酰肼合镍可由NiO、高氯酸及碳酰肼化合而成。NiO的晶胞结构如图所示,晶胞中含有的Ni2+数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钛、钒、铬、铁、镍、铜等过渡金属及其化合物在工业上有重要用途。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。
①基态 原子价层电子排布式为
原子价层电子排布式为___________ 。
②基态 原子核外电子的运动状态有
原子核外电子的运动状态有___________ 种。
(2)Ti的四卤化物熔点如下表所示,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是___________ 。
(3)制备 的反应为
的反应为 。
。
①上述化学方程式中非金属元素电负性由小到大的顺序为___________ (用元素符号表示)。
② 分子中所有原子均满足8电子稳定结构,
分子中所有原子均满足8电子稳定结构, 分子中π键和σ键的个数比为
分子中π键和σ键的个数比为___________ ,中心原子的杂化方式为___________ 。
(4)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如图所示:___________ 。
②该钒的硫化物的晶体中,与每V原子最近且等距S原子的个数是___________ 。
③能准确证明该钒的硫化物是晶体的最可靠的科学方法是___________ 。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。
①基态
 原子价层电子排布式为
原子价层电子排布式为②基态
 原子核外电子的运动状态有
原子核外电子的运动状态有(2)Ti的四卤化物熔点如下表所示,自
 至
至 熔点依次升高,原因是
熔点依次升高,原因是| 化合物 |  |  |  |
| 熔点/℃ | -24.12 | 38.3 | 155 |
(3)制备
 的反应为
的反应为 。
。①上述化学方程式中非金属元素电负性由小到大的顺序为
②
 分子中所有原子均满足8电子稳定结构,
分子中所有原子均满足8电子稳定结构, 分子中π键和σ键的个数比为
分子中π键和σ键的个数比为(4)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如图所示:
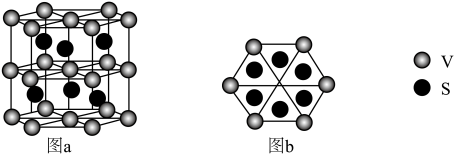
②该钒的硫化物的晶体中,与每V原子最近且等距S原子的个数是
③能准确证明该钒的硫化物是晶体的最可靠的科学方法是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】近年来我国科学家发明了Fe—Ni—P—C系非晶合金电催化剂(成分为:Fe80-xNixP20-yCy),是一种良好的析氢反应电催化剂,具有广泛的应用前景。回答下列问题:
(1)基态Ni原子的价电子排布图为_______ 。
(2)POCl3分子的VSEPR模型为_______ ,其中心原子的杂化方式为_______ 。
(3)二磷化四氢(P2H4),俗称“双磷”,沸点为51℃,C2H4的沸点为-103.9℃,P2H4的沸点高于C2H4的原因是_______ 。
(4)镍的一种化合物分子结构如图:

化合物中电负性最大的元素是_______ (填元素符号)。 分子中σ键和π键数目之比为_______ , 分子内还含有下列作用力中的_______ (填标号)。
A.氢键 B.离子键 C.配位键 D.金属键
(5)Ni、Fe均可形成多种氧化物晶体结构。
①NiO晶胞结构类型与氯化钠相同,Ni和O的配位数依次为_______ 。
②某种铁的氧化物晶胞如图所示,它由A、B方块组成,该氧化物中Fe2+、Fe3+、O2-的个数比为_______ 。 已知晶胞中相距最远的Fe2+之间距离为xnm,晶体的密度为_______ g·cm-3 (列出计算式,NA为阿伏加德罗常数的值)。

(1)基态Ni原子的价电子排布图为
(2)POCl3分子的VSEPR模型为
(3)二磷化四氢(P2H4),俗称“双磷”,沸点为51℃,C2H4的沸点为-103.9℃,P2H4的沸点高于C2H4的原因是
(4)镍的一种化合物分子结构如图:

化合物中电负性最大的元素是
A.氢键 B.离子键 C.配位键 D.金属键
(5)Ni、Fe均可形成多种氧化物晶体结构。
①NiO晶胞结构类型与氯化钠相同,Ni和O的配位数依次为
②某种铁的氧化物晶胞如图所示,它由A、B方块组成,该氧化物中Fe2+、Fe3+、O2-的个数比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁是一种重要的过渡元素,能形成多种物质,如做染料的普鲁士蓝(化学式为KFe[Fe(CN)6])。
Ⅰ.(1)Fe2+基态核外电子排布式为__ 。
(2)在普鲁士蓝中,中心离子是__ ,配体是__ 。
(3)一定条件下,CN-可氧化为OCN-。OCN-中三种元素的第一电离能由大到小的顺序为__ ;CN-中碳原子采取sp杂化,1 mol KFe[Fe(CN)6]中含有的π键数目为__ 。
Ⅱ.(1)某工厂为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程中,消耗的原料是__ 。有关反应的化学方程式为__ 。
(2)有一溶液中含有Ag+、Fe3+、Cu2+和Al3+四种阳离子,怎样把这些阳离子以沉淀的形式一一分离出来?___ 。
(3)制氧化亚铁常用:4FeC2O4 4FeO+CO↑+CO2↑,试说明为什么不采用FeCO3加热分解来制FeO而用此法。
4FeO+CO↑+CO2↑,试说明为什么不采用FeCO3加热分解来制FeO而用此法。___ 。
(4)在新生代的海水里有一种铁细菌,它们摄取海水中的亚铁离子,把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉淀下来形成铁矿;这个用酶作催化剂反应的另一个反应物是CO2,它在反应后转变成有机物,可用甲醛来表示。试写出配平的离子方程式__ 。
Ⅰ.(1)Fe2+基态核外电子排布式为
(2)在普鲁士蓝中,中心离子是
(3)一定条件下,CN-可氧化为OCN-。OCN-中三种元素的第一电离能由大到小的顺序为
Ⅱ.(1)某工厂为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程中,消耗的原料是
(2)有一溶液中含有Ag+、Fe3+、Cu2+和Al3+四种阳离子,怎样把这些阳离子以沉淀的形式一一分离出来?
(3)制氧化亚铁常用:4FeC2O4
 4FeO+CO↑+CO2↑,试说明为什么不采用FeCO3加热分解来制FeO而用此法。
4FeO+CO↑+CO2↑,试说明为什么不采用FeCO3加热分解来制FeO而用此法。(4)在新生代的海水里有一种铁细菌,它们摄取海水中的亚铁离子,把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉淀下来形成铁矿;这个用酶作催化剂反应的另一个反应物是CO2,它在反应后转变成有机物,可用甲醛来表示。试写出配平的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】根据所学内容回答下列问题:
(1)基态硼原子的轨道表示式为_______ 。
(2)根据VSEPR模型判断,下列微粒中所有原子都在同一平面上的一组是_______。
(3)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图1所示。1个铝原子周围有_______ 个镁原子最近且等距离。
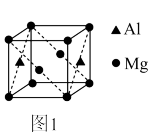
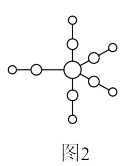
(4)配合物Fe(CO)5的熔点-20℃,沸点103℃,可用于制备纯铁。Fe(CO)5的结构如图2所示。下列关于Fe(CO)5说法不正确的是_______。
(5)独立的NH3分子中,H-N-H键角为107°。如图3所示是[Zn(NH3)6]2+的部分结构以及其中H-N-H键角。请解释[Zn(NH3)6]2+离子中H-N-H键角变为109.5°的原因是_______ 。
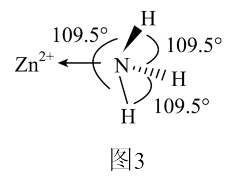
(1)基态硼原子的轨道表示式为
(2)根据VSEPR模型判断,下列微粒中所有原子都在同一平面上的一组是_______。
A. 和 和 | B. 和SO3 和SO3 | C.H3O+和 | D. 和 和 |

(4)配合物Fe(CO)5的熔点-20℃,沸点103℃,可用于制备纯铁。Fe(CO)5的结构如图2所示。下列关于Fe(CO)5说法不正确的是_______。

| A.Fe(CO)5是非极性分子,含有σ键和π键 |
B.Fe(CO)5中Fe原子的配体与 互为等电子体 互为等电子体 |
| C.1 mol Fe(CO)5含有5 mol σ键 |
| D.Fe(CO)5=Fe+5CO反应中没有新化学键生成 |
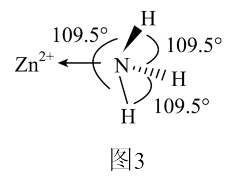
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】分铜液净化渣主要含铜、碲( )、锑(
)、锑( )、砷(
)、砷( )等元素的化合物,一种回收工艺流程如图所示:
)等元素的化合物,一种回收工艺流程如图所示:

已知:i.“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有 。
。
ii.“酸浸”时,锑元素反应生成难溶的 浸渣。
浸渣。
回答下列问题:
(1)As位于第四周期VA族,基态 的价层电子排布式为
的价层电子排布式为___________ 。
(2)“碱浸”时, 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(3)向碱浸液加入盐酸调节 ,有
,有 析出,分离出
析出,分离出 的操作是
的操作是___________ 。滤液中 元素最主要的存在形式为
元素最主要的存在形式为___________ (常温下, 的各级电离常数为:
的各级电离常数为: 、
、 、
、 )。
)。
A. B.
B.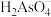 C.
C. D.
D.
(4)“氯盐酸浸”时,通入 的目的是
的目的是___________ 。
(5)“水解”时,生成 的化学方程式为
的化学方程式为___________ 。
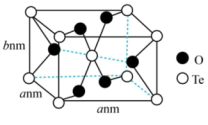
(6) 晶胞是长方体结构(如图所示),Te的配位数为
晶胞是长方体结构(如图所示),Te的配位数为___________ 。已知 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为___________  (列出计算表达式)
(列出计算表达式)
 )、锑(
)、锑( )、砷(
)、砷( )等元素的化合物,一种回收工艺流程如图所示:
)等元素的化合物,一种回收工艺流程如图所示:
已知:i.“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有
 。
。ii.“酸浸”时,锑元素反应生成难溶的
 浸渣。
浸渣。回答下列问题:
(1)As位于第四周期VA族,基态
 的价层电子排布式为
的价层电子排布式为(2)“碱浸”时,
 与
与 反应的离子方程式为
反应的离子方程式为(3)向碱浸液加入盐酸调节
 ,有
,有 析出,分离出
析出,分离出 的操作是
的操作是 元素最主要的存在形式为
元素最主要的存在形式为 的各级电离常数为:
的各级电离常数为: 、
、 、
、 )。
)。A.
 B.
B.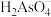 C.
C. D.
D.
(4)“氯盐酸浸”时,通入
 的目的是
的目的是(5)“水解”时,生成
 的化学方程式为
的化学方程式为(6)
 晶胞是长方体结构(如图所示),Te的配位数为
晶胞是长方体结构(如图所示),Te的配位数为 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 (列出计算表达式)
(列出计算表达式)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】氮族元素在化学领域具有重要的地位。请回答下列问题:
(1)基态氮原子的价电子轨道表示式为___________ ;第二周期的元素中,第一电离能介于B和N之间的元素有___________ 种。
(2)雌黄的分子式为As2S3,其分子结构如图所示: As原子的杂化类型为
As原子的杂化类型为___________ 。
(3)①向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。SO42-的空间构型为___________ ;[Cu(NH3)4]SO4·H2O固体中含有的化学键有___________ (填标号)。
A.离子键B.共价键C.氢键D.金属键E.配位键
若要确定[Cu(NH3)4]SO4·H2O是晶体还是非晶体,最科学的方法是进行___________ 实验。
②已知NF3与NH3分子的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,原因是___________ 。
(4)大π键可用 表示,其中n、m分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为
表示,其中n、m分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为 。N2O分子中的大π键表示为
。N2O分子中的大π键表示为_________________ 。
(5)立方氮化硼晶胞如图,其密度为ρg/cm3,氮化硼的摩尔质量为Mg/mol,阿伏伽德罗常数的值为NA,硼原子的半径为r cm,则硼原子的空间占有率为____________________ (用含有ρ、M、NA、r的代数式表示)。

(1)基态氮原子的价电子轨道表示式为
(2)雌黄的分子式为As2S3,其分子结构如图所示:
 As原子的杂化类型为
As原子的杂化类型为(3)①向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。SO42-的空间构型为
A.离子键B.共价键C.氢键D.金属键E.配位键
若要确定[Cu(NH3)4]SO4·H2O是晶体还是非晶体,最科学的方法是进行
②已知NF3与NH3分子的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,原因是
(4)大π键可用
 表示,其中n、m分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为
表示,其中n、m分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为 。N2O分子中的大π键表示为
。N2O分子中的大π键表示为(5)立方氮化硼晶胞如图,其密度为ρg/cm3,氮化硼的摩尔质量为Mg/mol,阿伏伽德罗常数的值为NA,硼原子的半径为r cm,则硼原子的空间占有率为

您最近一年使用:0次
【推荐3】铁、铜及其化合物在生产生活中有着广泛应用。回答下列问题:
(1)基态Fe原子核外电子的空间运动状态有_______ 种;试从结构角度解释 易被氧化为
易被氧化为 的原因
的原因_______ ; 是检验
是检验 的特征试剂,
的特征试剂,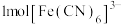 中含有
中含有_______ molσ键。
(2) 可形成
可形成 ,其中en代表
,其中en代表 。该化合物分子中,
。该化合物分子中, 的配位数为
的配位数为_______ ;VSEPR模型为四面体的非金属原子共有_______ 个;en中各元素的电负性由小到大的顺序为_______ 。
(3)一种由Cu、In,Te组成的晶体属四方晶系,晶胞参数和晶胞中各原子的投影位置如图所示,晶胞棱边夹角均为90°。
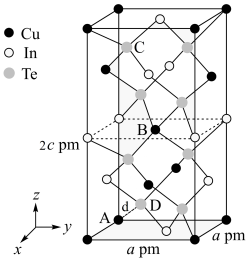
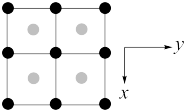
该晶体的化学式为_______ ;A点、B点原子的分数坐标分别为(0,0,0)、( ,
, ,
, ),则C点原子的分数坐标为
),则C点原子的分数坐标为_______ ;晶胞中A、D原子间距离d=_______ cm。
(1)基态Fe原子核外电子的空间运动状态有
 易被氧化为
易被氧化为 的原因
的原因 是检验
是检验 的特征试剂,
的特征试剂,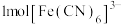 中含有
中含有(2)
 可形成
可形成 ,其中en代表
,其中en代表 。该化合物分子中,
。该化合物分子中, 的配位数为
的配位数为(3)一种由Cu、In,Te组成的晶体属四方晶系,晶胞参数和晶胞中各原子的投影位置如图所示,晶胞棱边夹角均为90°。


该晶体的化学式为
 ,
, ,
, ),则C点原子的分数坐标为
),则C点原子的分数坐标为
您最近一年使用:0次



