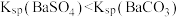下列图示与对应叙述相符的是
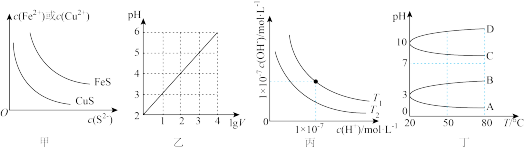

A.图甲表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则 |
B.图乙表示1L pH=2的 溶液加水稀释至V L,pH随 溶液加水稀释至V L,pH随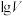 的变化 的变化 |
C.图丙表示在不同温度下水溶液中 和 和 浓度的变化曲线,图中温度 浓度的变化曲线,图中温度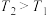 |
D.0.1mol/L  溶液的pH随温度变化的曲线如图丁中A所示 溶液的pH随温度变化的曲线如图丁中A所示 |
23-24高三上·北京·阶段练习 查看更多[2]
更新时间:2023-12-06 10:56:27
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】常温下,在等体积①pH=0的硫酸、②0.01mol/L NaOH溶液、③pH=10的纯碱溶液、④pH=5的NH4Cl溶液中,水电离程度的大小顺序是
| A.①>②>③>④ | B.②>①>④>③ | C.③>④>②>① | D.④>③>②>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温时,取0.1mol/LHCl和0.1mol/LHA(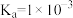 )混合溶液20mL,用0.1mol/LNaOH溶液滴定,滴定曲线如图所示,下列说法正确的是
)混合溶液20mL,用0.1mol/LNaOH溶液滴定,滴定曲线如图所示,下列说法正确的是
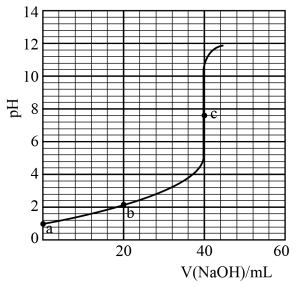
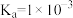 )混合溶液20mL,用0.1mol/LNaOH溶液滴定,滴定曲线如图所示,下列说法正确的是
)混合溶液20mL,用0.1mol/LNaOH溶液滴定,滴定曲线如图所示,下列说法正确的是
A.a点时,溶液中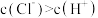 |
B.b点时,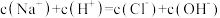 |
C.c点时, |
| D.a→c过程中,水的电离程度逐渐减弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下表是25℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
| 化学式 | CH3COOH | H2CO3 | AgCl | Ag2CrO4 |
| Ka或Ksp | Ka=1.8×10-5 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ksp=1.8×10-10 | Ksp=2.0×10-12 |
A.常温下,相同浓度①CH3COONH4②NH4HCO3③(NH4)2CO3溶液中,c(NH )由大到小的顺序是:①>②>③ )由大到小的顺序是:①>②>③ |
| B.AgCl易溶于氨水难溶于水,所以AgCl在氨水中的Ksp大于水中的Ksp |
C.向浓度均为1×10-3mol•L-1的KCl和K2CrO4混合液中滴加1×10-3mol•L-1的AgNO3溶液,CrO 先形成沉淀 先形成沉淀 |
| D.向饱和氯水中滴加NaOH溶液至溶液刚好为中性时,c(Na+)=2c(ClO-)+c(HClO) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述不正确的是
A.氨水中:c(OH-)-c(H+)=c(NH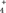 ) ) |
| B.饱和H2S溶液中:c(H2S)>c(H+)>c(HS-)>c(S2-) |
| C.0.1mol/LCH3COOH溶液中:c(CH3COOH)>c(CH3COO-)>c(H+) |
| D.Ca(OH)2溶液中:c(H+)+2c(Ca2+)=c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用pH试纸分别测量NaClO溶液、 溶液的pH 溶液的pH | 测得NaClO溶液的pH为11, 溶液的pH为8 溶液的pH为8 |  的酸性比HClO的强 的酸性比HClO的强 |
| B | 向试管中加入2 mL 10%  溶液,再滴加几滴2% NaOH溶液,振荡 溶液,再滴加几滴2% NaOH溶液,振荡 | 出现蓝色沉淀 | 该混合液可直接用于葡萄糖的检验 |
| C | 将盐酸滴入饱和碳酸氢钠溶液中 | 产生无色气体 | 非金属性:Cl>C |
| D | 向2 mL浓度均为0.1 mol·L 的NaCl和KI的混合液中滴加2滴0.1 mol•L 的NaCl和KI的混合液中滴加2滴0.1 mol•L  溶液 溶液 | 出现黄色沉淀 | 溶度积: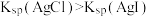 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下对于任一电池反应aA+bB=cC+dD,其电动势E=Eθ-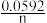 •lg
•lg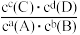 ,n为电池反应中转移的电子数。该小组同学设计装置(如图1),以Zn-Cu原电池探究离子浓度的改变对电极电势的影响。小组同学测得初始时Zn(s)+Cu2+(1mol•L-1)=Zn2+(1mol•L-1)+Cu(s) Eθ=1.1V(该反应n=2),随放电进行,观察电池电动势的变化趋势并绘制了电池电动势变化示意图(如图2)。下列说法正确的是
,n为电池反应中转移的电子数。该小组同学设计装置(如图1),以Zn-Cu原电池探究离子浓度的改变对电极电势的影响。小组同学测得初始时Zn(s)+Cu2+(1mol•L-1)=Zn2+(1mol•L-1)+Cu(s) Eθ=1.1V(该反应n=2),随放电进行,观察电池电动势的变化趋势并绘制了电池电动势变化示意图(如图2)。下列说法正确的是

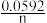 •lg
•lg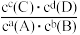 ,n为电池反应中转移的电子数。该小组同学设计装置(如图1),以Zn-Cu原电池探究离子浓度的改变对电极电势的影响。小组同学测得初始时Zn(s)+Cu2+(1mol•L-1)=Zn2+(1mol•L-1)+Cu(s) Eθ=1.1V(该反应n=2),随放电进行,观察电池电动势的变化趋势并绘制了电池电动势变化示意图(如图2)。下列说法正确的是
,n为电池反应中转移的电子数。该小组同学设计装置(如图1),以Zn-Cu原电池探究离子浓度的改变对电极电势的影响。小组同学测得初始时Zn(s)+Cu2+(1mol•L-1)=Zn2+(1mol•L-1)+Cu(s) Eθ=1.1V(该反应n=2),随放电进行,观察电池电动势的变化趋势并绘制了电池电动势变化示意图(如图2)。下列说法正确的是
| A.电压表读数为零后,则说明该原电池中Cu2+已经消耗完全 |
| B.小组同学向ZnSO4和CuSO4溶液中同时快速加入少量相同体积和浓度的Na2S溶液,发现电池电动势突然减小,则可知:Ksp(ZnS)<Ksp(CuS) |
| C.小组同学推测图2中直线与X轴的交点坐标大约为(37,0) |
| D.小组同学推测若将初始时左侧1mol•L-1的Zn-ZnSO4半电池,换为2mol•L-1的CuSO4-Cu半电池,右侧半电池保持不变,则仍能观察到相同的电压表偏转情况 |
您最近一年使用:0次

 的
的 溶液滴定
溶液滴定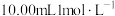 盐酸,该过程中
盐酸,该过程中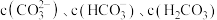 的变化曲线如图所示(忽略滴定过程中
的变化曲线如图所示(忽略滴定过程中 的逸出)。已知:
的逸出)。已知: 时,
时, 的
的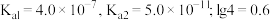 。下列说法正确的是
。下列说法正确的是
 的变化
的变化



 )大小:①>③>②
)大小:①>③>②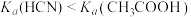 说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强
说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强