常温下,某三元有机中强酸H3A在一定pH范围内,存在以下平衡:H3A(s) H3A(aq);H3A(aq)
H3A(aq);H3A(aq)  H+(aq)+H2A-(aq);H2A-(aq)
H+(aq)+H2A-(aq);H2A-(aq) H+(aq)+HA2-(aq); HA2-(aq)
H+(aq)+HA2-(aq); HA2-(aq) H+(aq)+A3-(aq)。平衡常数依次为K0、K1、K2、K3。已知lgc(H2A-)、1gc(HA2-)、lgc(A3-)随 pH变化关系如图所示。下列说法正确的是
H+(aq)+A3-(aq)。平衡常数依次为K0、K1、K2、K3。已知lgc(H2A-)、1gc(HA2-)、lgc(A3-)随 pH变化关系如图所示。下列说法正确的是

 H3A(aq);H3A(aq)
H3A(aq);H3A(aq)  H+(aq)+H2A-(aq);H2A-(aq)
H+(aq)+H2A-(aq);H2A-(aq) H+(aq)+HA2-(aq); HA2-(aq)
H+(aq)+HA2-(aq); HA2-(aq) H+(aq)+A3-(aq)。平衡常数依次为K0、K1、K2、K3。已知lgc(H2A-)、1gc(HA2-)、lgc(A3-)随 pH变化关系如图所示。下列说法正确的是
H+(aq)+A3-(aq)。平衡常数依次为K0、K1、K2、K3。已知lgc(H2A-)、1gc(HA2-)、lgc(A3-)随 pH变化关系如图所示。下列说法正确的是
| A.随pH增大,H3A(aq)的浓度一定变小 |
| B.直线L表示lgc(H2A-)的变化情况 |
C.a= (pK2+ pK3) (已知: pK=-lgK) (pK2+ pK3) (已知: pK=-lgK) |
| D.pH=14时,则有c(A3-)>c(H2A-)>c(HA2-) |
更新时间:2023-11-11 12:16:04
|
相似题推荐
单选题
|
困难
(0.15)
名校
【推荐1】肼为二元弱碱,在水中的电离方式与氨相似。常温下,向一定浓度肼(N2H4)水溶液中通入HCl,保持溶液体积和温度不变,测得pOH与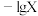 [X为
[X为 、
、 、
、 ]的变化关系如图所示。下列说法正确的是
]的变化关系如图所示。下列说法正确的是

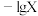 [X为
[X为 、
、 、
、 ]的变化关系如图所示。下列说法正确的是
]的变化关系如图所示。下列说法正确的是
A.曲线M表示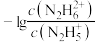 |
B.常温下, |
C.a点溶液中: |
D.b点溶液中: |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐2】常温下,用0.1 mol·L-1的HCl溶液分别滴定Vx mL 0.1 mol·L-1的NaX溶液和VY mL 0.1 mol·L-1 NaY溶液,二者的pH随着加入盐酸体积的变化曲线如图所示,已知:酸性HX>HY。下列判断正确的是


| A.Vx>VY |
| B.M点:c(X-)= c(Y-) |
| C.b表示盐酸滴定NaX溶液的曲线 |
| D.常温下,Ka (HX) = 9.0×10-12 |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐1】常温下,Ka(CH3COOH)=1.0×10-5, 向某含有ZnSO4酸性废液加入一定量CH3COONa后,再通入H2S生成ZnS沉淀,始终保持H2S饱和,即c(H2S)=0.1mol/L,体系中pX[pX=—1gX,X为 、
、 或c(Zn2+), 单位为 mol/L]与
或c(Zn2+), 单位为 mol/L]与 关系如图。下列说法错误的是
关系如图。下列说法错误的是
 、
、 或c(Zn2+), 单位为 mol/L]与
或c(Zn2+), 单位为 mol/L]与 关系如图。下列说法错误的是
关系如图。下列说法错误的是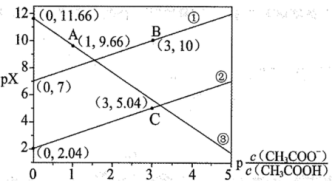
A.②中X为 | B.A 点溶液的pH为4 |
| C.Ka1(H₂S) 的数量级为10-7 | D.Ksp(ZnS)=10-21.7 |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐2】常温下,用0.1 mol·L-1的HCl溶液分别滴定Vx mL 0.1 mol·L-1的NaX溶液和VY mL 0.1 mol·L-1 NaY溶液,二者的pH随着加入盐酸体积的变化曲线如图所示,已知:酸性HX>HY。下列判断正确的是


| A.Vx>VY |
| B.M点:c(X-)= c(Y-) |
| C.b表示盐酸滴定NaX溶液的曲线 |
| D.常温下,Ka (HX) = 9.0×10-12 |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐3】常温下,向 饱和溶液[有足量
饱和溶液[有足量 固体]中滴加氨水,发生反应:
固体]中滴加氨水,发生反应: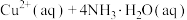

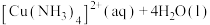 ,溶液中
,溶液中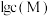 与
与 的关系如图所示,其中
的关系如图所示,其中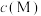 表示
表示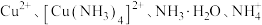 的浓度,单位为
的浓度,单位为 。下列说法正确的是
。下列说法正确的是
 饱和溶液[有足量
饱和溶液[有足量 固体]中滴加氨水,发生反应:
固体]中滴加氨水,发生反应: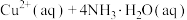

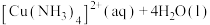 ,溶液中
,溶液中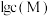 与
与 的关系如图所示,其中
的关系如图所示,其中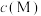 表示
表示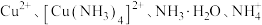 的浓度,单位为
的浓度,单位为 。下列说法正确的是
。下列说法正确的是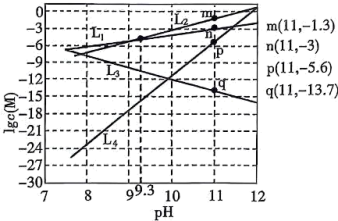
A. 表示溶液中 表示溶液中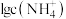 与 与 的关系 的关系 |
B. 的溶度积常数 的溶度积常数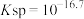 |
C. 时,溶液中: 时,溶液中: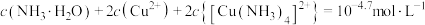 |
D.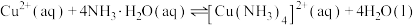 的平衡常数 的平衡常数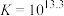 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐1】织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体。25 ℃时,各组分含量随pH变化情况如图所示(Cl-没有画出)。下列说法错误的是


| A.25 ℃时,HClO2的电离平衡常数的数值Ka=10-6 |
| B.使用该漂白剂的最佳pH为3.0 |
| C.25 ℃时,等浓度的HClO2溶液和NaClO2溶液等体积混合后,混合溶液中:c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-) |
D.该温度下的NaClO2溶液中c(Na+)>c(ClO )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
困难
(0.15)
解题方法
【推荐2】图(I)和图(II)分别为二元酸H2A和乙二胺(H2NCH2CH2NH2)溶液中各微粒的百分含量δ(即物质的量百分数)随溶液pH的变化曲线(25℃)。下列说法正确的是


| A.[H3NCH2CH2NH3]A溶液显碱性 |
| B.乙二胺(H2NCH2CH2NH2)的Kb2=10-7.15 |
| C.[H3NCH2CH2NH2][HA]溶液中各离子浓度大小关系为:c([H3NCH2CH2NH2]+>c(HA-)>c(H2NCH2CH2NH2)>c(A2-)>c(OH-)>c(H+) |
D.向[H3NCH2CH2NH2][HA]溶液中通入一定量的HCl气体,则 可能增大也可能减小 可能增大也可能减小 |
您最近一年使用:0次

 溶液中,溶液中含铁微粒
溶液中,溶液中含铁微粒 、
、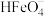 、
、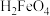 、
、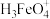 的物质的量分数
的物质的量分数 随pOH的变化如图,[
随pOH的变化如图,[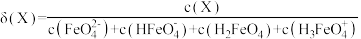 ,
, ]。下列说法正确的是
]。下列说法正确的是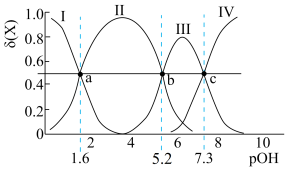

 的平衡常数
的平衡常数

 与pOH的变化关系
与pOH的变化关系


