SiCl4是生产多品硅的副产物。利用SiC14对废弃的锂电池正极材料LiCoO2进行氯化处理以回收Li、Co等金属,工艺路线如下:
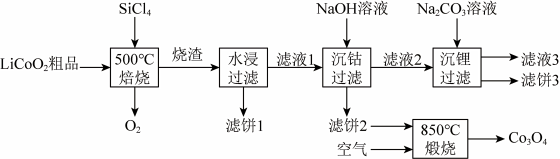
回答下列问题:
(1)Co位于元素周期表第__________ 周期第_________ 族。
(2)烧渣是LiC1、CoC12和SiO2的混合物,“500°C焙烧”后剩余的SiC14应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因___________ 。
(3)鉴别洗净的“滤饼3”和固体Na2CO3常用方法的名称是___________ 。
(4)已知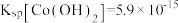 ,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为
,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为___________ mol·L-1。“850℃煅烧”时的化学方程式为___________ 。

回答下列问题:
(1)Co位于元素周期表第
(2)烧渣是LiC1、CoC12和SiO2的混合物,“500°C焙烧”后剩余的SiC14应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
(3)鉴别洗净的“滤饼3”和固体Na2CO3常用方法的名称是
(4)已知
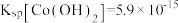 ,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为
,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为
更新时间:2023-12-02 19:15:28
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】 是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。
【 的制备】
的制备】
(1)用下图装置制备 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是___________ 。 ;
;___________ 。
【 的性质探究】
的性质探究】
资料:i. 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。
ii.单质硫可溶于 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。
某小组研究 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是___________ 。
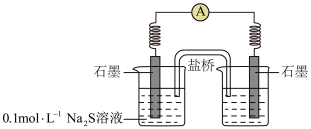
②同学讨论后,设计了如下实验,证实该条件下 的确可以将
的确可以将 氧化成
氧化成 。
。___________ 。
b.连通后电流计指针偏转,一段时间后,___________ (填操作和现象)。
(4)实验I的现象与资料i不相符,其原因是新生成的产物( )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是___________ 。
(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是___________ ,请设计验证此猜想的实验方案___________ 。
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与___________ 等因素有关。
 是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。【
 的制备】
的制备】(1)用下图装置制备
 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是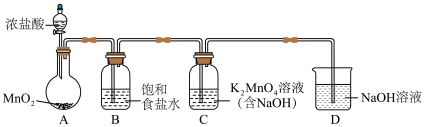
 ;
;【
 的性质探究】
的性质探究】资料:i.
 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。ii.单质硫可溶于
 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。某小组研究
 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。| 实验序号 | 实验过程 | 实验现象 |
| Ⅰ |
| 紫色变浅( ),生成棕褐色沉淀( ),生成棕褐色沉淀( ) ) |
| Ⅱ |
| 溶液呈淡黄色( ),生成浅粉色沉淀(MnS) ),生成浅粉色沉淀(MnS) |
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有
 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是②同学讨论后,设计了如下实验,证实该条件下
 的确可以将
的确可以将 氧化成
氧化成 。
。
b.连通后电流计指针偏转,一段时间后,
(4)实验I的现象与资料i不相符,其原因是新生成的产物(
 )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】合理利用工业烟尘,变废为宝,对保护环境具有重要意义。一种以铜冶炼烟尘(主要成分是CuO、Cu2O、ZnO、PbO、SiO2、As2O3)为原料制备Cu和ZnSO4•6H2O的流程如图所示:
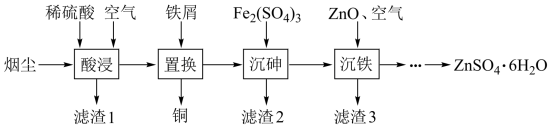
已知:酸浸时As2O3转化为H3AsO3。
回答下列问题:
(1)能提高“酸浸”浸出率的措施是________ (任写一条),“滤渣1”的主要成分是_______ 。
(2)“酸浸”.过程中Cu2O发生反应的化学方程式为________ 。
(3)“滤渣2”的成分为FeAsO4,则“沉砷”过程中发生反应的离子方程式为________ 。
(4)加入ZnO的目的________ ,滤渣3的成分是________ 。
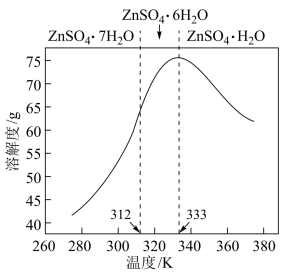
(5)ZnSO4的溶解度曲线如图所示,从溶液中回收ZnSO4•6H2O的实验操作为________ 。

已知:酸浸时As2O3转化为H3AsO3。
回答下列问题:
(1)能提高“酸浸”浸出率的措施是
(2)“酸浸”.过程中Cu2O发生反应的化学方程式为
(3)“滤渣2”的成分为FeAsO4,则“沉砷”过程中发生反应的离子方程式为
(4)加入ZnO的目的
(5)ZnSO4的溶解度曲线如图所示,从溶液中回收ZnSO4•6H2O的实验操作为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3、MgO、CaO等,生产工艺流程示意如图:

(1)将菱锌矿研磨成粉的目的是__ 。
(2)完成“氧化除铁”步骤中反应的离子方程式:□Fe(OH)2+□____+□_____=□Fe(OH)3+□Cl-____ 。
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是___ 。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为__ 。
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是___ (选填序号)。
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为_____ 、____ 、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于___ 。

(1)将菱锌矿研磨成粉的目的是
(2)完成“氧化除铁”步骤中反应的离子方程式:□Fe(OH)2+□____+□_____=□Fe(OH)3+□Cl-
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为
| Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
| 开始沉淀的pH | 10.4 | 6.4 | — | — |
| 沉淀完全的pH | 12.4 | 8.0 | — | — |
| 开始溶解的pH | — | 10.5 | — | — |
| Ksp | 5.6×10-12 | — | 6.8×10-6 | 2.8×10-9 |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】有关物质的转化关系如下图所示,部分物质与条件已略去。已知A由两种元素组成,且其式量为65,B是由两种元素组成的黑色粉末,C是空气中含量最多的气体,D是白色粉末,且其焰色反应呈黄色,E是一种紫红色金属,H是一种红棕色气体,I是最常见的液体,K是一种强碱。

(1)A的化学式为____________ 。
(2)C的结构式为____________ 。
(3)D的电子式为____________ 。
(4)K中含有的化学键类型有____________ ,属于____________ (填离子化合物或者共价化合物)。
(5)写出反应①的化学方程式:______________________ 。
(6)写出反应②的离子方程式:_________________________ 。

(1)A的化学式为
(2)C的结构式为
(3)D的电子式为
(4)K中含有的化学键类型有
(5)写出反应①的化学方程式:
(6)写出反应②的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】下图是由常见元素组成的一些单质及其化合物之间的转化关系图。常温常压下,B、E、F、H、I均为气体,F无色无味,且能使澄清石灰水变浑蚀;B、E、I均有刺激性气味,E能使湿润的红色石蕊试纸变蓝,B、E在空气中相遇会产生白烟,I为红棕色。A是一种常见的氮肥,F也能由人直接分解可得到。C、G、K的焰色反应呈黄色。(反应中部分生成物已略去)
请回答下列问题:
(1)物质D的化学式为____________ ,其水溶液中阳离子的检验方法为(文字表述)______ 。
(2)写出反应③的化学方程式:__________________ 。
(3)写出反应④的离子方程式:__________________ 。
(4)写出反应⑤的化学方程式:__________________ 。
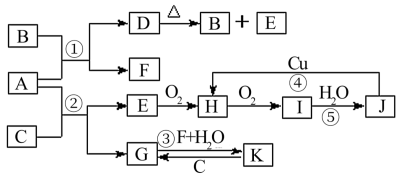
请回答下列问题:
(1)物质D的化学式为
(2)写出反应③的化学方程式:
(3)写出反应④的离子方程式:
(4)写出反应⑤的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】Na 、Fe 、Cl 、Al是中学化学常见的元素。回答下列问题:
(1)①只含上述某一种元素的常见化合物中,呈淡黄色的是________ (填化学式)。
②焰色反应的实验中,Na元素燃烧时的焰色为_______ 色,观察 K元素燃烧时的焰色需要透过________ 。
③实验室在制备 Fe(OH)2时必须隔绝空气,否则发生的现象是_________ 。 反应化学方程式为_________ 。
(2)饮用水质量是关系人类健康的重要问题。
①氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为:_________ 。
②写出工业上制取漂白粉的化学反应方程式:_________ 。
③ClO2是一种广谱型的消毒剂,将逐渐取代 Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加 H2SO4酸化后反应制得,反应中 NaClO3和Na2SO3的物质的量之比为________ 。
(1)①只含上述某一种元素的常见化合物中,呈淡黄色的是
②焰色反应的实验中,Na元素燃烧时的焰色为
③实验室在制备 Fe(OH)2时必须隔绝空气,否则发生的现象是
(2)饮用水质量是关系人类健康的重要问题。
①氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为:
②写出工业上制取漂白粉的化学反应方程式:
③ClO2是一种广谱型的消毒剂,将逐渐取代 Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加 H2SO4酸化后反应制得,反应中 NaClO3和Na2SO3的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】三氧化二镍(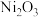 )是重要的电子元件材料和蓄电池材料,工业上利用含镍废料(主要成分为镍、铝、氧化铁、碳等)提取,工艺流程如下:
)是重要的电子元件材料和蓄电池材料,工业上利用含镍废料(主要成分为镍、铝、氧化铁、碳等)提取,工艺流程如下:

已知:①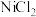 易溶于水,
易溶于水, 不能氧化
不能氧化 。
。
②实际生产温度时的溶解度: 。
。
(1)“预处理”操作选择用___________ (填标号)来除去废旧镍电池表面的矿物油污。
A.纯碱溶液清洗 B.NaOH溶液清洗 C.酒精清洗
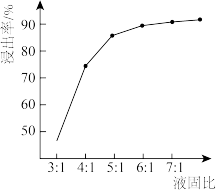
(2)常温下,盐酸的浓度为2.5mol/L,“液固比”与镍的浸出率的关系如图所示,实际生产采取的“液固比”为___________ ,主要的原因是___________ 。
(3)“酸浸”所得溶液中含有 ,通过实验证明
,通过实验证明 不能氧化
不能氧化 :
:___________ 。
(4)室温下,“酸浸”所得溶液中 的浓度为0.2mol/L,当溶液的pH调到2时,c(Fe3+)=
的浓度为0.2mol/L,当溶液的pH调到2时,c(Fe3+)=___________ 。(已知: )
)
(5)加入 溶液“沉镍”得到的沉淀为
溶液“沉镍”得到的沉淀为___________ 。
(6)电解过程中产生的氯气在碱性条件下生成 ,再把二价镍氧化为三价镍,写出“氧化”反应的离子反应方程式
,再把二价镍氧化为三价镍,写出“氧化”反应的离子反应方程式___________ 。
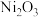 )是重要的电子元件材料和蓄电池材料,工业上利用含镍废料(主要成分为镍、铝、氧化铁、碳等)提取,工艺流程如下:
)是重要的电子元件材料和蓄电池材料,工业上利用含镍废料(主要成分为镍、铝、氧化铁、碳等)提取,工艺流程如下:
已知:①
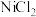 易溶于水,
易溶于水, 不能氧化
不能氧化 。
。②实际生产温度时的溶解度:
 。
。(1)“预处理”操作选择用
A.纯碱溶液清洗 B.NaOH溶液清洗 C.酒精清洗
(2)常温下,盐酸的浓度为2.5mol/L,“液固比”与镍的浸出率的关系如图所示,实际生产采取的“液固比”为

(3)“酸浸”所得溶液中含有
 ,通过实验证明
,通过实验证明 不能氧化
不能氧化 :
:(4)室温下,“酸浸”所得溶液中
 的浓度为0.2mol/L,当溶液的pH调到2时,c(Fe3+)=
的浓度为0.2mol/L,当溶液的pH调到2时,c(Fe3+)= )
)(5)加入
 溶液“沉镍”得到的沉淀为
溶液“沉镍”得到的沉淀为(6)电解过程中产生的氯气在碱性条件下生成
 ,再把二价镍氧化为三价镍,写出“氧化”反应的离子反应方程式
,再把二价镍氧化为三价镍,写出“氧化”反应的离子反应方程式
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】利用氢氧化钡沉淀-碘量法对锰酸钾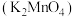 和高锰酸钾
和高锰酸钾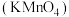 共存时的离子浓度进行分别测定,方法如下。
共存时的离子浓度进行分别测定,方法如下。
已知:① ,
, 易溶于水
易溶于水
②
③溶液中 较高时,
较高时, 易被空气氧化
易被空气氧化
④该条件下, 和
和 的还原产物都是
的还原产物都是
I.取 和
和 共存液
共存液 于烧杯中,加入过量
于烧杯中,加入过量 溶液,产生灰绿色沉淀,过滤。
溶液,产生灰绿色沉淀,过滤。
II.取I中的滤液于碘量瓶中,加入 溶液和浓硫酸,此时溶液颜色发生变化,盖上盖子后至黑暗处放置5分钟。
溶液和浓硫酸,此时溶液颜色发生变化,盖上盖子后至黑暗处放置5分钟。
III.用 溶液滴定,待溶液颜色变为淡黄色时,加入淀粉指示剂,达到滴定终点时,消耗
溶液滴定,待溶液颜色变为淡黄色时,加入淀粉指示剂,达到滴定终点时,消耗 溶液
溶液 。
。
IV.另取一份相同共存液 于碘量瓶中,重复II、III操作,记录消耗
于碘量瓶中,重复II、III操作,记录消耗 溶液
溶液 。
。
(1)I中灰绿色沉淀是_______ ,同时生成的另一种产物的化学式是_______ 。
(2)II中反应的离子方程式是_______ 。
(3)III中滴定终点时的现象是_______ 。
(4)II中加入浓硫酸要适量,防止溶液中 较高发生副反应:
较高发生副反应:_______ (写出反应的离子方程式)。
(5)该溶液中锰酸钾的物质的量浓度为_______  。
。
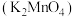 和高锰酸钾
和高锰酸钾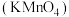 共存时的离子浓度进行分别测定,方法如下。
共存时的离子浓度进行分别测定,方法如下。已知:①
 ,
, 易溶于水
易溶于水②

③溶液中
 较高时,
较高时, 易被空气氧化
易被空气氧化④该条件下,
 和
和 的还原产物都是
的还原产物都是
I.取
 和
和 共存液
共存液 于烧杯中,加入过量
于烧杯中,加入过量 溶液,产生灰绿色沉淀,过滤。
溶液,产生灰绿色沉淀,过滤。II.取I中的滤液于碘量瓶中,加入
 溶液和浓硫酸,此时溶液颜色发生变化,盖上盖子后至黑暗处放置5分钟。
溶液和浓硫酸,此时溶液颜色发生变化,盖上盖子后至黑暗处放置5分钟。III.用
 溶液滴定,待溶液颜色变为淡黄色时,加入淀粉指示剂,达到滴定终点时,消耗
溶液滴定,待溶液颜色变为淡黄色时,加入淀粉指示剂,达到滴定终点时,消耗 溶液
溶液 。
。IV.另取一份相同共存液
 于碘量瓶中,重复II、III操作,记录消耗
于碘量瓶中,重复II、III操作,记录消耗 溶液
溶液 。
。(1)I中灰绿色沉淀是
(2)II中反应的离子方程式是
(3)III中滴定终点时的现象是
(4)II中加入浓硫酸要适量,防止溶液中
 较高发生副反应:
较高发生副反应:(5)该溶液中锰酸钾的物质的量浓度为
 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
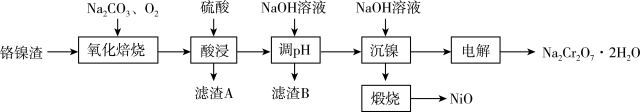
【推荐3】镍、铬等属于宝贵的金属资源。一种回收电化学废渣中铬镍的工艺流程如下:
已知:
①铬镍渣中含有 、
、 、
、 、
、 、
、 等;
等;
②25℃时,部分物质的溶度积表:
③
回答下列问题:
(1)“氧化焙烧”时, 发生的化学方程式
发生的化学方程式_______ 。
(2)“酸浸”使用强力搅拌器搅拌的目的是_______ ,滤渣A主要是_______ (填化学式)。
(3)“调 ”时,若
”时,若 至少为
至少为_______ 时, 沉淀完全。(
沉淀完全。( )
)
(4)“沉镍”后,“煅烧”的化学方程式为_______ 。
(5)已知“电解”操作中的装置如下图所示。
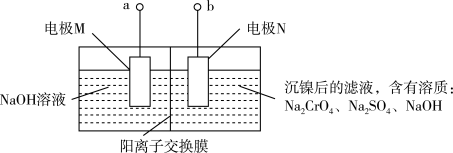
①a接电源的_______ (填“正”或“负”)极。
②电极N上的电极反应式为_______ 。

已知:
①铬镍渣中含有
 、
、 、
、 、
、 、
、 等;
等;②25℃时,部分物质的溶度积表:
| 物质 |  |  |  |  |
 | 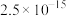 | 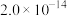 | 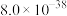 | 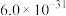 |

回答下列问题:
(1)“氧化焙烧”时,
 发生的化学方程式
发生的化学方程式(2)“酸浸”使用强力搅拌器搅拌的目的是
(3)“调
 ”时,若
”时,若 至少为
至少为 沉淀完全。(
沉淀完全。( )
)(4)“沉镍”后,“煅烧”的化学方程式为
(5)已知“电解”操作中的装置如下图所示。

①a接电源的
②电极N上的电极反应式为
您最近一年使用:0次
【推荐1】在石墨材料性能提升的帮助下,锂离子电池的性能也得到了大幅提升,华为公司曾开发出石墨烯锂离子电池,其工作原理如图1所示,该锂离子电池正极铝钴膜主要含有 、
、 等,处理该正极废料的一种流程如图2所示:
等,处理该正极废料的一种流程如图2所示:

请回答下列问题:
(1)“碱浸”时发生反应的离子方程式为_______ 。
(2)滤渣的主要成分的化学式为_______ 。
(3)“酸溶”时 的作用是
的作用是_______ ,“酸溶”时温度不宜过高的原因是_______ 。盐酸可以代替 和
和 的混合液,但工业上都不采用盐酸,其原因是
的混合液,但工业上都不采用盐酸,其原因是_______ 。
(4)用图1中锂离子电池作电源电解制备 的装置如图3所示,d与锂离子电池的
的装置如图3所示,d与锂离子电池的_______ 极相连(填“a”或“b”),电解池中发生的总反应离子方程式为_______ 。当锂离子电池中有 移向正极时,电解池中阴极区溶液质量的变化量为
移向正极时,电解池中阴极区溶液质量的变化量为_______ g。
 、
、 等,处理该正极废料的一种流程如图2所示:
等,处理该正极废料的一种流程如图2所示:
请回答下列问题:
(1)“碱浸”时发生反应的离子方程式为
(2)滤渣的主要成分的化学式为
(3)“酸溶”时
 的作用是
的作用是 和
和 的混合液,但工业上都不采用盐酸,其原因是
的混合液,但工业上都不采用盐酸,其原因是(4)用图1中锂离子电池作电源电解制备
 的装置如图3所示,d与锂离子电池的
的装置如图3所示,d与锂离子电池的 移向正极时,电解池中阴极区溶液质量的变化量为
移向正极时,电解池中阴极区溶液质量的变化量为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】过硫酸氢钾复盐(化学式表示为K2SO4·KHSO4·2KHSO5),—般用作漂白剂及NOx、SO2等废气脱除剂。制备过硫酸氢钾复盐流程如图:

(1)在“转化”操作前,需先用冰水冷却双氧水,可能的原因是________________ 。“转化”过程中,浓硫酸与H2O2发生可逆反应生成过硫酸(H2SO5),写出该变化的化学反应方程式____________________ 。
(2)已知H2SO5为一元强酸。结晶操作中,加入K2CO3即可获得过硫酸氢钾复盐晶体,该过程的离子反应方程式为________________________ ;操作中,选用50%K2CO3溶液且需分批缓慢加入目的是____________ 。过硫酸氢钾复盐产率(以产品含氧量表示)随溶液pH和温度的变化关系如图所示。则该过程适宜的条件是________________ 。

(3)过滤后,用无水乙醇取代蒸馏水洗涤沉淀,目的是__________________ 。

(1)在“转化”操作前,需先用冰水冷却双氧水,可能的原因是
(2)已知H2SO5为一元强酸。结晶操作中,加入K2CO3即可获得过硫酸氢钾复盐晶体,该过程的离子反应方程式为

(3)过滤后,用无水乙醇取代蒸馏水洗涤沉淀,目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】用软锰矿 主要成分为
主要成分为 生产高锰酸钾产生的锰泥中,还含有
生产高锰酸钾产生的锰泥中,还含有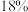 的
的 、
、 的
的 均为质量分数
均为质量分数 ,及少量Cu、Pb的化合物等,用锰泥可回收制取
,及少量Cu、Pb的化合物等,用锰泥可回收制取 ,过程如图:
,过程如图:

 高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强,通常用来酸化高锰酸钾的酸是
高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强,通常用来酸化高锰酸钾的酸是 ______ .
 除去滤液1中
除去滤液1中 的离子方程式是
的离子方程式是 ______ .
 经实验证明:
经实验证明: 稍过量时,起始
稍过量时,起始 、
、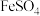 混合溶液中
混合溶液中 时,滤液1中能够检验出有
时,滤液1中能够检验出有 ;
; 时,滤液1中不能检验出有
时,滤液1中不能检验出有 根据上述信息回答①②③:
根据上述信息回答①②③:
①检验 是否氧化完全的实验操作是
是否氧化完全的实验操作是 ______ .
②生产时 、
、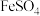 混合溶液中
混合溶液中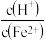 应控制在
应控制在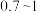 之间,不宜过大,请结合后续操作从节约药品的角度分析,原因是
之间,不宜过大,请结合后续操作从节约药品的角度分析,原因是 ______ .
③若 ,调节
,调节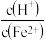 到
到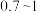 的最理想试剂是
的最理想试剂是 ______  填序号
填序号
 溶液
溶液  铁粉
铁粉 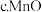
 写出滤液2中加入过量
写出滤液2中加入过量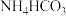 反应的离子方程式:
反应的离子方程式: ______ .
 上述过程锰回收率可达
上述过程锰回收率可达 ,若处理1740kg的锰泥,可生产
,若处理1740kg的锰泥,可生产
______ kg.
 主要成分为
主要成分为 生产高锰酸钾产生的锰泥中,还含有
生产高锰酸钾产生的锰泥中,还含有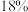 的
的 、
、 的
的 均为质量分数
均为质量分数 ,及少量Cu、Pb的化合物等,用锰泥可回收制取
,及少量Cu、Pb的化合物等,用锰泥可回收制取 ,过程如图:
,过程如图: 
 高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强,通常用来酸化高锰酸钾的酸是
高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强,通常用来酸化高锰酸钾的酸是  除去滤液1中
除去滤液1中 的离子方程式是
的离子方程式是  经实验证明:
经实验证明: 稍过量时,起始
稍过量时,起始 、
、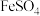 混合溶液中
混合溶液中 时,滤液1中能够检验出有
时,滤液1中能够检验出有 ;
; 时,滤液1中不能检验出有
时,滤液1中不能检验出有 根据上述信息回答①②③:
根据上述信息回答①②③:①检验
 是否氧化完全的实验操作是
是否氧化完全的实验操作是 ②生产时
 、
、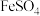 混合溶液中
混合溶液中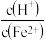 应控制在
应控制在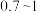 之间,不宜过大,请结合后续操作从节约药品的角度分析,原因是
之间,不宜过大,请结合后续操作从节约药品的角度分析,原因是 ③若
 ,调节
,调节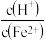 到
到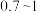 的最理想试剂是
的最理想试剂是  填序号
填序号
 溶液
溶液  铁粉
铁粉 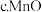
 写出滤液2中加入过量
写出滤液2中加入过量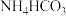 反应的离子方程式:
反应的离子方程式:  上述过程锰回收率可达
上述过程锰回收率可达 ,若处理1740kg的锰泥,可生产
,若处理1740kg的锰泥,可生产
您最近一年使用:0次





