在恒温下,向容积为2L的恒容容器中加入一定量的碳单质和2molH2O(g),初始压强为105Pa。发生反应: ∆H>0。经过2min后达到平衡,容器的压强增加了20%。
∆H>0。经过2min后达到平衡,容器的压强增加了20%。
(1)该反应自发进行的条件是__________ 。(填“高温”或“低温”或“任意条件”)
(2)2min内H2O的平均反应速率为__________ mol/(L·min)。
(3)2min平衡时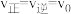 ,采取下列措施后,使
,采取下列措施后,使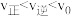 的是__________。
的是__________。
(4)平衡常数Kp=__________ Pa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)下列说法正确的是__________。
 ∆H>0。经过2min后达到平衡,容器的压强增加了20%。
∆H>0。经过2min后达到平衡,容器的压强增加了20%。(1)该反应自发进行的条件是
(2)2min内H2O的平均反应速率为
(3)2min平衡时
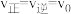 ,采取下列措施后,使
,采取下列措施后,使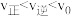 的是__________。
的是__________。| A.恒温恒容下,除去部分H2O | B.降低温度 |
| C.恒温恒容下,充入Ar | D.恒温恒压下,充入Ar |
(5)下列说法正确的是__________。
| A.增加碳单质,可以加快该反应速率 |
| B.2min时,H2O的转化率为20% |
| C.当混合气体的平均摩尔质量不再变化时,可以判断该反应达到了平衡 |
| D.平衡后向体系内补加0.4molH2O(g)和0.4molCO(g),反应向逆反应方向进行 |
更新时间:2023-12-11 17:42:46
|
相似题推荐
填空题
|
适中
(0.65)
真题
【推荐1】N2O5—是一种新型硝化剂,其性质和制备受到人们的关注.
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是_______________ 。
(2)2N2O5(g)→4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将___________ 填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
则500 s内N2O5的分解速率为____________ 。
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2_________ T1。
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的_________ 区生成,其电极反应式为______________________________ 。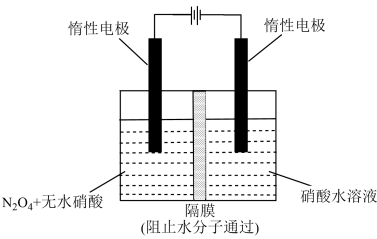
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是
(2)2N2O5(g)→4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| e(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500 s内N2O5的分解速率为
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的 NO 和 NH3,在 一定条件下发生反应:6NO(g) + 4NH3(g) 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。
①能说明该反应已达到平衡状态的标志是___________
a.反应速率 v( NH3) =v( N2)
b.容器内压强不再随时间而发生变化
c.容器内 N2的物质的量分数不再随时间而发生变化
d.容器内 n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
e.12molN-H 键断裂的同时生成 5mol N≡N 键
f.混合气体的总质量不随时间的变化而变化
②某次实验中测得容器内 NO 及 N2的物质的量随时间变化如图所示,图中 b 点 对应的速率关系是v(正)___________ v(逆)(填﹥、﹤或﹦),d 点对应的速率关系是v(正) ___________ v(逆)
(填﹥、﹤或﹦)。

(2)298 K 时,若已知生成标准状况下 2.24LNH3时放出热量为 4.62kJ。写出合成氨反应的热化学方程式___________ 。在该温度下,取 1molN2和 3mol H2 放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量总小于 92.4 kJ, 其原因是___________ 。
(3)一定条件下,在 2L密闭容器内,反应 2NO2(g) N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
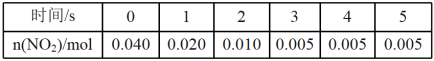
①用 N2O4 表示 0~2 s 内该反应的平均速率为__________ 。在第 5s 时,NO2的转化 率为____________ 。(转化率是指某一反应物转化的百分率。)
②根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是______________ 。
 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。①能说明该反应已达到平衡状态的标志是
a.反应速率 v( NH3) =v( N2)
b.容器内压强不再随时间而发生变化
c.容器内 N2的物质的量分数不再随时间而发生变化
d.容器内 n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
e.12molN-H 键断裂的同时生成 5mol N≡N 键
f.混合气体的总质量不随时间的变化而变化
②某次实验中测得容器内 NO 及 N2的物质的量随时间变化如图所示,图中 b 点 对应的速率关系是v(正)
(填﹥、﹤或﹦)。

(2)298 K 时,若已知生成标准状况下 2.24LNH3时放出热量为 4.62kJ。写出合成氨反应的热化学方程式
(3)一定条件下,在 2L密闭容器内,反应 2NO2(g)
 N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
①用 N2O4 表示 0~2 s 内该反应的平均速率为
②根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)可逆反应A(g)+B(g)⇌2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示.
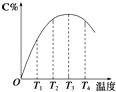
①由T1向T2变化时,正反应速率________ 逆反应速率(填“>”、“<”或“=”).
②由T3向T4变化时,正反应速率________ 逆反应速率(填“>”、“<”或“=”).
③反应在________ 温度下达到平衡.
④此反应的正反应为________ 热反应.
(2)800℃时,在2L密闭容器中发生反应2NO(g)+O2(g)⇌2NO2(g),在反应体系中,n(NO)随时间的变化如表所示:
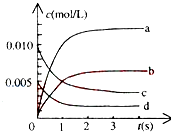
①图中表示NO2变化的曲线是________ ,用O2表示从0~2s内该反应的平均速率v=________ .
②能说明该反应已经达到平衡状态的是________
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变.

①由T1向T2变化时,正反应速率
②由T3向T4变化时,正反应速率
③反应在
④此反应的正反应为
(2)800℃时,在2L密闭容器中发生反应2NO(g)+O2(g)⇌2NO2(g),在反应体系中,n(NO)随时间的变化如表所示:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

①图中表示NO2变化的曲线是
②能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氨气是化工生产的主要原料之一,氨气的用途非常广泛。在一固定容积为2 L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,发生如下反应: N2(g)+3H2(g)⇌2NH3(g)△H=-Q kJ/mol(Q>0)。
(1)该反应所用的催化剂是_______ (填写名称);该反应450℃时的平衡常数______ 500℃时的平衡常数(填“>”、“<”或“=”)。
(2)下列描述中能说明上述反应已达平衡的是_______
A. 3v正(H2)=2v逆(NH3) B.容器中气体的平均分子量不随时间而变化
C.容器中气体的密度不随时间而变化 D.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2 mol计算从反应开始到平衡时,平均反应速率v(N2)为______________ 。
(4)在另一容积可变的容器内加入0.2 mol的N2和0.6 mol的H2,在相同条件下发生上述反应,则产生的NH3的物质的量比原平衡产生的NH3______ (填“多”或“少”或”“一样”)。
(5)工厂生产的氨水稀释后可作肥料。稀释氨水时,随着水的增加溶液中减少的是_______
a. b.
b.  c.
c.  d.
d. 
(6)液氨和水类似,也能电离:2NH3⇌NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K____ 2×10-30(填“<”、“>”或“=”);
②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为:____ 。
(1)该反应所用的催化剂是
(2)下列描述中能说明上述反应已达平衡的是
A. 3v正(H2)=2v逆(NH3) B.容器中气体的平均分子量不随时间而变化
C.容器中气体的密度不随时间而变化 D.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2 mol计算从反应开始到平衡时,平均反应速率v(N2)为
(4)在另一容积可变的容器内加入0.2 mol的N2和0.6 mol的H2,在相同条件下发生上述反应,则产生的NH3的物质的量比原平衡产生的NH3
(5)工厂生产的氨水稀释后可作肥料。稀释氨水时,随着水的增加溶液中减少的是
a.
 b.
b.  c.
c.  d.
d. 
(6)液氨和水类似,也能电离:2NH3⇌NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K
②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将CH4和CO2重整转化为合成气一直是减少温室气体排放的研究方向之一,涉及如下反应:
主反应:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)
积碳反应:CH4(g)⇌C(s)+2H2(g) =+75 kJ/mol
=+75 kJ/mol
(1)恒温恒容密闭容器中仅发生主反应,能说明反应达到平衡状态的是_______.(填标号)
(2)在体积为5L恒容密闭容器中充入2.0mol CH4和4.0molCO2,500℃下仅发生主反应,CH4、CO2的物质的量随时间变化如下表所示:
①CO2在 0~30 min 内的平均反应速率v(CO2)=___________ 。
②主反应的平衡常数表达式为______________________ 。
③若在60min 时再充入2.0 mol CH4,达到新平衡后CH4的转化率减小,此时平衡常数K_______ (填“增大”、“减小”或“不变”)
④ 若相同条件下改为充入4.0 mol CH4和 8.0 mol CO2反应,平衡后CH4的转化率______ 90%(填“<”、“=”或“>”)。
主反应:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)

积碳反应:CH4(g)⇌C(s)+2H2(g)
 =+75 kJ/mol
=+75 kJ/mol(1)恒温恒容密闭容器中仅发生主反应,能说明反应达到平衡状态的是_______.(填标号)
| A.容器内的压强不再变化 | B.c (CH4):c(CO2): c (CO): c (H2)=1:1:2:2 |
| C.混合气体的密度不再变化 | D.断开4molC-H键同时断开2molH-H键 |
| 时间/min 反应物 | 0 | 15 | 30 | 45 | 60 | 75 |
| n(CH4)/mol | 2.0 | 1.3 | 0.8 | 0.4 | 0.2 | 0.2 |
| n(CO2)/mol | 4.0 | 3.3 | 2.8 | 2.4 | 2.2 | 2.2 |
①CO2在 0~30 min 内的平均反应速率v(CO2)=
②主反应的平衡常数表达式为
③若在60min 时再充入2.0 mol CH4,达到新平衡后CH4的转化率减小,此时平衡常数K
④ 若相同条件下改为充入4.0 mol CH4和 8.0 mol CO2反应,平衡后CH4的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】300 ℃时,将2 mol SO2、1 mol O2混合于2 L的恒容密闭容器中,发生反应2SO2(g) + O2(g)  2SO3(g) ΔH,2 min末达到平衡,测得SO2的转化率为60%。请根据化学反应的有关原理回答下列问题:
2SO3(g) ΔH,2 min末达到平衡,测得SO2的转化率为60%。请根据化学反应的有关原理回答下列问题:
(1)能证明反应已经达到平衡状态的是________ 。
①c(SO2)∶c(O2)∶c(SO3) = 2∶1∶2
②单位时间内生成n mol SO3的同时消耗n mol SO2
③反应速率v(SO3) = 2v(O2)
④温度和体积一定时,容器内压强不再变化
⑤温度和压强一定时,混合气体的密度不再变化
(2)下图表示该反应的速率(v)随时间(t)变化的关系:
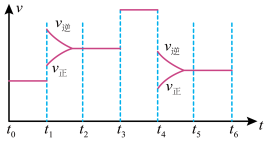
据图分析;t3时改变的外界条件可能是________ ;t6时保持体积不变向体系中充入少量He,平衡________ (填“向左”“向右”或“不”)移动。SO2含量最高的区间是______ (填“t0~t1”、“t2~t3”、“t3~t4”或“t5~t6”)。
(3)300 ℃时,该反应的平衡常数为________
 2SO3(g) ΔH,2 min末达到平衡,测得SO2的转化率为60%。请根据化学反应的有关原理回答下列问题:
2SO3(g) ΔH,2 min末达到平衡,测得SO2的转化率为60%。请根据化学反应的有关原理回答下列问题:(1)能证明反应已经达到平衡状态的是
①c(SO2)∶c(O2)∶c(SO3) = 2∶1∶2
②单位时间内生成n mol SO3的同时消耗n mol SO2
③反应速率v(SO3) = 2v(O2)
④温度和体积一定时,容器内压强不再变化
⑤温度和压强一定时,混合气体的密度不再变化
(2)下图表示该反应的速率(v)随时间(t)变化的关系:

据图分析;t3时改变的外界条件可能是
(3)300 ℃时,该反应的平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g) + 2N2(g)+ 6H2(g) Si3N4(s) + 12 HCl(g) ΔH<0
Si3N4(s) + 12 HCl(g) ΔH<0
(1)在一定温度下进行上述反应,若反应容器的容积为2 L, 3 min后达到平衡,测得固体的质量增加了2.80g,则H2的平均反应速率为___________ mol / (Lmin);该反应的平衡常数表达式K=___________
(2)上述反应达到平衡后,下列说法正确的是___________ 。
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4的物质的量,平衡向左移动
d.其他条件不变,增大HCl的物质的量,平衡向左移动
(3) 一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是___________
a. 3v逆(N2) = v 正(H2)
b. v正 (HCl) = 4v 正(SiCl4)
c.混合气体密度保持不变
d. c(N2): c(H2) :c(HCl)= 1:3:6
(4)若平衡时H2和HCl的物质的量之比为 ,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比
,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___________  (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
 Si3N4(s) + 12 HCl(g) ΔH<0
Si3N4(s) + 12 HCl(g) ΔH<0(1)在一定温度下进行上述反应,若反应容器的容积为2 L, 3 min后达到平衡,测得固体的质量增加了2.80g,则H2的平均反应速率为
(2)上述反应达到平衡后,下列说法正确的是
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4的物质的量,平衡向左移动
d.其他条件不变,增大HCl的物质的量,平衡向左移动
(3) 一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是
a. 3v逆(N2) = v 正(H2)
b. v正 (HCl) = 4v 正(SiCl4)
c.混合气体密度保持不变
d. c(N2): c(H2) :c(HCl)= 1:3:6
(4)若平衡时H2和HCl的物质的量之比为
 ,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比
,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】甲醇是重要的化工原料,利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇时,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1= -99kJ•mol-1
CH3OH(g) △H1= -99kJ•mol-1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2= 58kJ•mol-1
CH3OH(g)+H2O(g) △H2= 58kJ•mol-1
③CO2(g)+H2(g) CO(g)+H2O(g) △H3=+41kJ•mol-1
CO(g)+H2O(g) △H3=+41kJ•mol-1
(1)一定温度下,向体积为2L的密闭容器中加入CO和H2,假设只发生反应①,达平衡后测得各组分浓度如下:
①列式并计算平衡常数K=___ 。
②若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是___ 。
③若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正__ v逆(填“>”、“<”或“=”)。
(2)在实际生产中,当合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率α(CO)与温度和压强的关系如图所示。
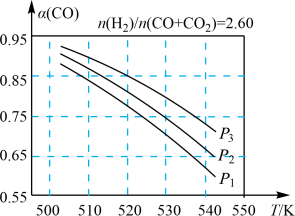
α(CO)值随温度升高而___ (填“增大”或“减小”),其原因是___ 。图中的压强由大到小为___ ,其判断理由是___ 。
①CO(g)+2H2(g)
 CH3OH(g) △H1= -99kJ•mol-1
CH3OH(g) △H1= -99kJ•mol-1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2= 58kJ•mol-1
CH3OH(g)+H2O(g) △H2= 58kJ•mol-1③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3=+41kJ•mol-1
CO(g)+H2O(g) △H3=+41kJ•mol-1(1)一定温度下,向体积为2L的密闭容器中加入CO和H2,假设只发生反应①,达平衡后测得各组分浓度如下:
| 物质 | CO | H2 | CH3OH |
| 浓度(mol•L-1) | 0.9 | 1.0 | 0.6 |
①列式并计算平衡常数K=
②若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是
③若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正
(2)在实际生产中,当合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率α(CO)与温度和压强的关系如图所示。

α(CO)值随温度升高而
您最近一年使用:0次
【推荐3】回答下列问题
(1)二氟卡宾(:CF2)作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注。硫单质与二氟卡宾可以形成S=CF2,反应历程如图所示:
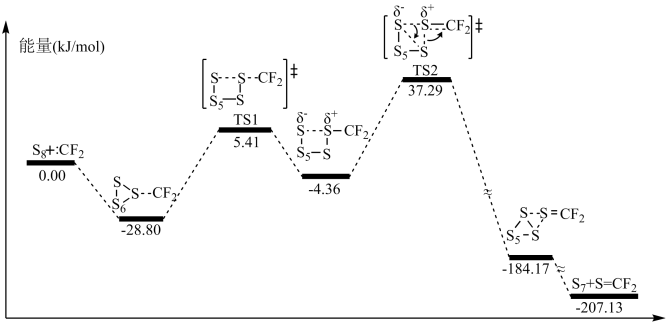
①由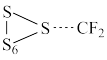 生成
生成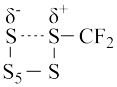 的活化能为
的活化能为__________________ ;
②决定反应速率的基元反应的活化能为______________________ 。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g) 2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量)
2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量)
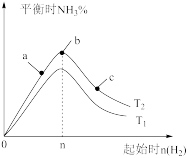
①图象中T2和T1的关系是:T2___________ T1(填“高于”、“低于”、 “等于”或“无法确定”)。
②比较在a、b、c三点所处的平衡状态中,反应物N 2的转化率最高的是_______________ (填字母)。
③在起始体系中n(N2):n(H2)= 1:3时,反应后氨的百分含量最大;若容器容积为1 L, n=3 mol反应达到平衡时H2的转化率为60%,则此条件下(T2),反应的平衡常数K=__________________ 。
(1)二氟卡宾(:CF2)作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注。硫单质与二氟卡宾可以形成S=CF2,反应历程如图所示:

①由
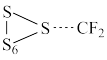 生成
生成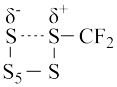 的活化能为
的活化能为②决定反应速率的基元反应的活化能为
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)
 2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量)
2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量) 
①图象中T2和T1的关系是:T2
②比较在a、b、c三点所处的平衡状态中,反应物N 2的转化率最高的是
③在起始体系中n(N2):n(H2)= 1:3时,反应后氨的百分含量最大;若容器容积为1 L, n=3 mol反应达到平衡时H2的转化率为60%,则此条件下(T2),反应的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题:
(1)用离子方程式表示碳酸钠溶液显碱性的原因:_______ 。
(2)汽油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),判断该设想能否实现,并简述原因:_______ 。
(3)25℃时,在1L0.1mol/L的HA溶液中,有0.001mol的HA电离成离子,则该温度下的电离平衡常数为_______ 。
(4)在25℃时,将pH=11 的Ba(OH)2溶液Va L与 pH=2 的HCl溶液Vb L混合,若所得溶液为中性,则Va :Vb=_______ 。
(5)常温下将10 mL 0.1 mol/L的NaOH溶液与10 mL 0.2 mol/L的醋酸溶液混合后溶液显酸性,则混合后溶液中各离子浓度的大小顺序为_______ 。
(6)已知常温下部分弱电解质的电离平衡常数如下表:
常温下,pH相同的三种溶液①NaF溶液;②NaClO溶液;③Na2CO3溶液,其物质的量浓度由大到小的顺序是_______ (填序号)。
(7)已知25℃时,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=1.0×10-32。则使Cr3+恰好完全沉淀,即溶液中c(Cr3+)=1.0×10-5mol/L时,应调节pH的最小值a为多少_______
(1)用离子方程式表示碳酸钠溶液显碱性的原因:
(2)汽油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),判断该设想能否实现,并简述原因:
(3)25℃时,在1L0.1mol/L的HA溶液中,有0.001mol的HA电离成离子,则该温度下的电离平衡常数为
(4)在25℃时,将pH=11 的Ba(OH)2溶液Va L与 pH=2 的HCl溶液Vb L混合,若所得溶液为中性,则Va :Vb=
(5)常温下将10 mL 0.1 mol/L的NaOH溶液与10 mL 0.2 mol/L的醋酸溶液混合后溶液显酸性,则混合后溶液中各离子浓度的大小顺序为
(6)已知常温下部分弱电解质的电离平衡常数如下表:
| 化学式 | HF | HClO | H2CO3 | NH3·H2O |
| 电离常数 | 6.8×10-4 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 | Kb=1.7×10-5 |
(7)已知25℃时,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=1.0×10-32。则使Cr3+恰好完全沉淀,即溶液中c(Cr3+)=1.0×10-5mol/L时,应调节pH的最小值a为多少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=__________ ,已知:K3000C>K3500C,则该反应是______ 热反应。
(2)图中表示NO2的变化的曲线是_____________ ;用O2表示从0~2 s内该反应的平均速率v=____________
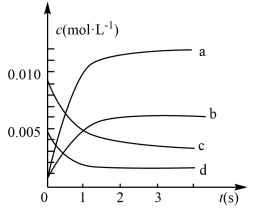
(3)能说明该反应已达到平衡状态的是____________ 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是____________
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(5)关于该反应的下列说法中,正确的是________ (填字母)。
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS>0 D.ΔH<0,ΔS<0
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=
(2)图中表示NO2的变化的曲线是

(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(5)关于该反应的下列说法中,正确的是
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS>0 D.ΔH<0,ΔS<0
您最近一年使用:0次

 CaO(s)+CO2(g),
CaO(s)+CO2(g), ,
,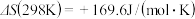 ,常温下该反应
,常温下该反应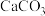 分解反应要自发进行,温度T应高于
分解反应要自发进行,温度T应高于 、
、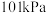 下,
下,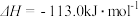 ,
,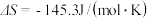 ,反应在常温下
,反应在常温下

