铼(Re)是一种熔点高、耐磨、耐腐蚀的金属,广泛用于航天航空等领域。
某实验室制备铼的原理如下:
Ⅰ.①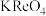 先与
先与 反应生成
反应生成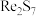 。
。
②滴入足量的含 的氨水溶液,生成
的氨水溶液,生成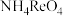 ,同时有
,同时有 生成,装置如图1所示。
生成,装置如图1所示。
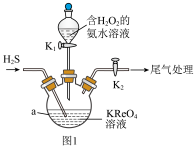
(1)仪器a的名称是___________ 。
(2)金属铼比同周期的Ba熔点高,从结构的角度解释原因是___________ 。
(3)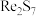 生成
生成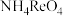 的化学方程式是
的化学方程式是___________ 。
Ⅱ.用氢气还原Ⅰ中生成的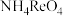 得到Re。实验装置如图2所示。
得到Re。实验装置如图2所示。
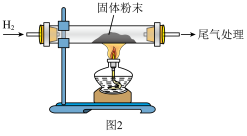
(4)在加热实验装置前,先通入一段时间的氢气,再___________ ,最后点燃酒精灯;停止实验时,先关闭酒精灯,再持续通一段时间 。制备Re反应的化学方程式为
。制备Re反应的化学方程式为___________ 。
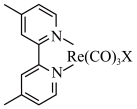
(5)铼可形成多种配位化合物,下图是它的一种配位化合物的结构(X表示卤素原子),其中碳原子的杂化方式为___________ ,Re的配位数为___________ 。
某实验室制备铼的原理如下:
Ⅰ.①
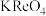 先与
先与 反应生成
反应生成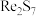 。
。②滴入足量的含
 的氨水溶液,生成
的氨水溶液,生成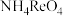 ,同时有
,同时有 生成,装置如图1所示。
生成,装置如图1所示。
(1)仪器a的名称是
(2)金属铼比同周期的Ba熔点高,从结构的角度解释原因是
(3)
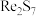 生成
生成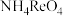 的化学方程式是
的化学方程式是Ⅱ.用氢气还原Ⅰ中生成的
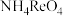 得到Re。实验装置如图2所示。
得到Re。实验装置如图2所示。
(4)在加热实验装置前,先通入一段时间的氢气,再
 。制备Re反应的化学方程式为
。制备Re反应的化学方程式为(5)铼可形成多种配位化合物,下图是它的一种配位化合物的结构(X表示卤素原子),其中碳原子的杂化方式为

更新时间:2024-01-15 19:45:23
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
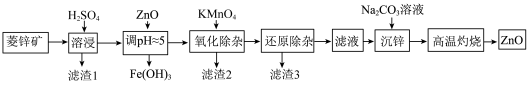
【推荐1】工业上可由菱锌矿(主要成分为ZnCO3,还含有Ni、Cd、Fe、Mn等元素)制备ZnO。工艺如图所示:
②弱酸性溶液中KMnO4氧化Mn2+时,产物中含Mn元素物质只有MnO2。
③氧化性强弱顺序:Ni2+>Cd2+>Zn2+。
④相关金属离子[c(Mn+)=0.1 mol/L]形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)基态Zn原子的价电子排布式为___________ ,ZnO溶于氨水生成[Zn(NH3)4]2+,1 mol [Zn(NH3)4]2+共有___________ mol的σ键。
(2)①“溶浸”过程中,为了提高浸出率,可采取的措施是___________ 。(写一条即可)
②“调pH”时,可替代ZnO的一种含锌化合物是___________ 。(用化学式表示)
③“调pH”时,若pH=5.5,此时溶液中Zn2+的最大浓度c=___________ mol/L。
(3)写出“氧化除杂”时KMnO4溶液与Mn2+反应的离子方程式___________ 。
(4)“还原除杂”除去的离子是___________ ,加入的还原剂是___________ 。
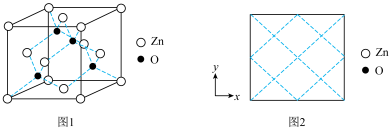
(5)“沉锌”时生成ZnCO3·2Zn(OH)2·2H2O (碱式碳酸锌)沉淀,该沉淀“高温灼烧”后获得ZnO。氧化锌的一种晶体的晶胞是立方晶胞(如图1所示),其中与锌原子距离最近的O原子数有___________ 个,请在图2中画出该晶胞沿z轴方向的平面投影图___________ 。
②弱酸性溶液中KMnO4氧化Mn2+时,产物中含Mn元素物质只有MnO2。
③氧化性强弱顺序:Ni2+>Cd2+>Zn2+。
④相关金属离子[c(Mn+)=0.1 mol/L]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ | Mn2+ | Ni2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.0 | 7.4 | 8.1 | 6.9 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.0 | 9.4 | 10.1 | 8.9 |
(1)基态Zn原子的价电子排布式为
(2)①“溶浸”过程中,为了提高浸出率,可采取的措施是
②“调pH”时,可替代ZnO的一种含锌化合物是
③“调pH”时,若pH=5.5,此时溶液中Zn2+的最大浓度c=
(3)写出“氧化除杂”时KMnO4溶液与Mn2+反应的离子方程式
(4)“还原除杂”除去的离子是
(5)“沉锌”时生成ZnCO3·2Zn(OH)2·2H2O (碱式碳酸锌)沉淀,该沉淀“高温灼烧”后获得ZnO。氧化锌的一种晶体的晶胞是立方晶胞(如图1所示),其中与锌原子距离最近的O原子数有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】LiMn2O4作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3,含有少量Si、Fe、Ni、Al等元素)制备LiMn2O4的流程如图:

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为________ 。为提高溶矿速率,可采取的措施________ (举1例)。
(2)加入少量MnO2的作用是________ 。不宜使用H2O2替代MnO2,原因是________ 。
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=________ mol•L-1;用石灰乳调节至pH≈7,除去的金属离子是________ 。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有________ 。
(5)煅烧窑中,生成LiMn2O4反应的化学方程式是________ 。

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为
(2)加入少量MnO2的作用是
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有
(5)煅烧窑中,生成LiMn2O4反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】含锰化合物在化学工业中有十分重要的用途。某含锰矿石的主要成分是 ,还含CaO、
,还含CaO、 、FeS等杂质,由此矿石生产
、FeS等杂质,由此矿石生产 的工艺流程如图所示:
的工艺流程如图所示:
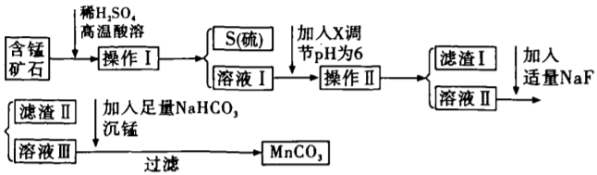
相关金属离子生成氢氧化物沉淀的pH如表所示:
回答下列问题:
(1)酸溶时,不能将稀硫酸换成浓盐酸,原因是___________ 。
(2)取溶液Ⅰ加入KSCN溶液,溶液呈血红色,试写出酸溶过程中FeS发生反应的离子方程式:___________ 。
(3)调节溶液Ⅰ的pH时所用的物质X最好是___________ 。
(4)滤渣Ⅱ为___________ (填化学式)。
(5)沉锰的化学方程式为___________ 。
(6)沉锰后过滤得到固体 ,设计实验方案验证
,设计实验方案验证 固体是否洗涤干净:
固体是否洗涤干净:___________ 。
(7) 可用于生产
可用于生产 等盐类。通过用草酸滴定
等盐类。通过用草酸滴定 溶液的方法可测定
溶液的方法可测定 粗品的纯度(质量分数)。若量取
粗品的纯度(质量分数)。若量取 溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将
溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将___________ (填“偏大”、“偏小”或“不变”)。
 ,还含CaO、
,还含CaO、 、FeS等杂质,由此矿石生产
、FeS等杂质,由此矿石生产 的工艺流程如图所示:
的工艺流程如图所示:
相关金属离子生成氢氧化物沉淀的pH如表所示:
| 物质 | 开始沉淀 | 沉淀完全 |
 | 2.7 | 3.7 |
 | 12 | ______ |
 | 3.8 | 4.7 |
回答下列问题:
(1)酸溶时,不能将稀硫酸换成浓盐酸,原因是
(2)取溶液Ⅰ加入KSCN溶液,溶液呈血红色,试写出酸溶过程中FeS发生反应的离子方程式:
(3)调节溶液Ⅰ的pH时所用的物质X最好是
(4)滤渣Ⅱ为
(5)沉锰的化学方程式为
(6)沉锰后过滤得到固体
 ,设计实验方案验证
,设计实验方案验证 固体是否洗涤干净:
固体是否洗涤干净:(7)
 可用于生产
可用于生产 等盐类。通过用草酸滴定
等盐类。通过用草酸滴定 溶液的方法可测定
溶液的方法可测定 粗品的纯度(质量分数)。若量取
粗品的纯度(质量分数)。若量取 溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将
溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】阅读资料,获取信息,回答问题。
(A) A、 B、C、D为四种元素,A原子的1S轨道为半充满;在元素周期表中,B的电负性最大;C的原子序数为24;D2+的电子排布式和Ar相同。
(B)两元素电负性差值大于1. 7,原子间一般形成离子键;小于1. 7,原子间一般形成共价键。
(C)下列是周期表中部分元素的电负性x和第一电离能I1 (KJ·mol-1):

(1).A原子的轨道表示式为_______ ,B原子的价电子排布式为________ ,C原子的电
子排布式为___________ ,D在周期表中的位置为________ 周期________ 族。
(2).电负性最小的元素位于______ 族,第一电离能最大的元素是(填元素符号)______ ;
锂元素的电负性取值范围为____ <x(Li)<_____ ;A12S3属______ 化合物
(3)标出化合物OF2、 LiAlH4中各元素的化合价(写在元素符号上)____ 、____ 。
(A) A、 B、C、D为四种元素,A原子的1S轨道为半充满;在元素周期表中,B的电负性最大;C的原子序数为24;D2+的电子排布式和Ar相同。
(B)两元素电负性差值大于1. 7,原子间一般形成离子键;小于1. 7,原子间一般形成共价键。
(C)下列是周期表中部分元素的电负性x和第一电离能I1 (KJ·mol-1):

(1).A原子的轨道表示式为
子排布式为
(2).电负性最小的元素位于
锂元素的电负性取值范围为
(3)标出化合物OF2、 LiAlH4中各元素的化合价(写在元素符号上)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】红砷镍矿(NiAs)是常见的镍矿之一,镍(28Ni)和砷(33As)都是第四周期元素。回答下列问题:
(1)对具有下列价电子排布的Ni或As进行光谱实验,用光谱仪一定能摄取到原子发射光谱的是_______ (填字母)。
A.Ni:3d10 B.As:4s24p 4p
4p 4p
4p
C.As: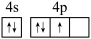 D.Ni:
D.Ni:
(2)镍及其化合物常用作有机合成的催化剂,如Ni(PPh3)2(Ph表示苯基),在该化合物中,配体 的空间构型为_______ ;Ni(PPh3)2晶体中存在的化学键类型有_______ (填字母)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(3)鉴定Ni2+的特征反应如下:
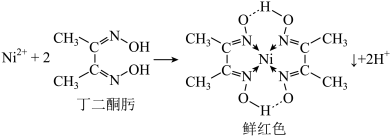
在1 mol鲜红色沉淀中,含有sp2杂化原子的数目为_______ 个。丁二酮肟中,各元素电负性由大到小的顺序为_______ (用元素符号表示)。
(4)红砷镍矿是一种六方晶体(底面为60°和120°的菱形),其晶胞如图所示,图中深色小球为Ni,浅色大球为As。

①晶胞中Ni周围距离最近且等距的As有_______ 个。
②已知NiAs的晶胞边长分别为a pm和c pm,阿伏加德罗常量的值为NA,则红砷镍矿晶体的理论密度为ρ=_______ g•cm-3。(写出表达式,需化简)
③画出以As为顶点的NiAs的晶胞图_______ 。
(1)对具有下列价电子排布的Ni或As进行光谱实验,用光谱仪一定能摄取到原子发射光谱的是
A.Ni:3d10 B.As:4s24p
 4p
4p 4p
4p
C.As:
 D.Ni:
D.Ni:
(2)镍及其化合物常用作有机合成的催化剂,如Ni(PPh3)2(Ph表示苯基),在该化合物中,
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(3)鉴定Ni2+的特征反应如下:

在1 mol鲜红色沉淀中,含有sp2杂化原子的数目为
(4)红砷镍矿是一种六方晶体(底面为60°和120°的菱形),其晶胞如图所示,图中深色小球为Ni,浅色大球为As。

①晶胞中Ni周围距离最近且等距的As有
②已知NiAs的晶胞边长分别为a pm和c pm,阿伏加德罗常量的值为NA,则红砷镍矿晶体的理论密度为ρ=
③画出以As为顶点的NiAs的晶胞图
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】A、B、C、D、E为原子序数依次增大的五种元素,A的一种同位素可用于考古中测定生物的死亡年代; B与A同周期,其s能级电子数比p能级电子数多;C原子的最外层电子数是次外层的3倍;D与B同主族;E的原子序数为29。回答下列问题:
(1)五种元素中第一电离能最大的是_____ ,其中D原子价电子排布图为______ 。
(2)元素B的简单气态氢化物的沸点______ 元素A的简单气态氢化物的沸点(填大于或小于),其主要原因是____ ; A的简单气态氢化物中心原子的杂化轨道类型为________ 。
(3)BC3-的立体构型为__________ ,与其互为等电子体的分子是__________ (写化学式)。
(4)EC在加热条件下容易转化为E2C,从原子结构的角度解释原因____________ ;E原子的外围电子排布式为_____________ 。
(5)硼与D可形成一种耐磨材料F,其结构与金刚石相似(如图)。F的晶胞边长为a cm,则该晶体密度的表达式为___________ g·cm-3。(用含a、NA的式子表示, 不必化简)。

(1)五种元素中第一电离能最大的是
(2)元素B的简单气态氢化物的沸点
(3)BC3-的立体构型为
(4)EC在加热条件下容易转化为E2C,从原子结构的角度解释原因
(5)硼与D可形成一种耐磨材料F,其结构与金刚石相似(如图)。F的晶胞边长为a cm,则该晶体密度的表达式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】臭氧(O3)在[Fe(H2O)6]2+催化下能将烟气中的SO2、NOx分别氧化为 和
和 ,NOx也可在其他条件下被还原为N2,回答下列问题:
,NOx也可在其他条件下被还原为N2,回答下列问题:
(1) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 ___________ ; 的空间构型为
的空间构型为 ___________ (用文字描述)。
(2)Fe2+基态核外电子排布式为___________ ;[Fe(H2O)6]2+中提供孤电子对的原子是 ___________ (用元素符号表示)。
(3)N的第一电离能___________ (填“大于”或“小于”)O的第一电离能;H2SO4酸性强于H2SO3的原因是 ___________ 。
(4)①离子晶体CaC2的晶胞结构如图所示。CaC2中包含的化学键为___________ 。从钙离子看该晶体属于 ___________ 堆积,一个晶胞中含有的π键有 ___________ 个。
②图中所示晶胞中,底面边长为anm,高为bnm2晶体密度为___________ g⋅cm﹣3(NA表示阿伏加德罗常数的值,用含NA、a、b的计算式表示)。
 和
和 ,NOx也可在其他条件下被还原为N2,回答下列问题:
,NOx也可在其他条件下被还原为N2,回答下列问题:(1)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为  的空间构型为
的空间构型为 (2)Fe2+基态核外电子排布式为
(3)N的第一电离能
(4)①离子晶体CaC2的晶胞结构如图所示。CaC2中包含的化学键为
②图中所示晶胞中,底面边长为anm,高为bnm2晶体密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ氢、碳、氮都是重要的非金属元素,它们的单质及其化合物在科学研究和工业生产中有重要的应用。
(1)下列微粒基态的电子排布中未成对电子数最多的是__ (填序号)
a.N3- b.Fe3+ c.Cu d.Cr e.C
(2)第一电离能介于B、N之间的第二周期元素有_____ 种。
(3)已知HCO3-在水溶液中可通过氢键成为二聚体(八元环结构),试画出该二聚体的结构式:____________________________ 。
(4)[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2-+4H++4H2O [Zn(H2O)4]2++4HOCH2CN
[Zn(H2O)4]2++4HOCH2CN
①Zn2+基态核外电子排布式为____ 。1 mol HCHO分子中含有σ键的物质的量为____ mol。
②HOCH2CN分子中碳原子轨道的杂化类型是__ 。与H2O分子互为等电子体的阴离子为__ 。
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为______ 。
Ⅱ.由原子序数由小到大的A、B、C、D、E五种元素构成某配位化合物X,其原子个数比为14∶4∶5∶1∶1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6ns1,回答下列问题。
(1)该配位化合物X的化学式为________ 。
(2)元素B、C、D的第一电离能由小到大排列顺序为________ 。(用元素符号表示)
(3)D元素原子的最外层电子轨道表示式为________ 。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可任意比互溶,解释其主要原因为_______________________ 。
(5)A元素与E元素可形成一种红色离子化合物Y,其原子个数比为1∶1,该化合物Y可与稀硝酸反应,生成一种蓝色溶液和两种无色气体(其中一种为A元素的单质),写出该反应的化学方程式_____________________________ 。
(1)下列微粒基态的电子排布中未成对电子数最多的是
a.N3- b.Fe3+ c.Cu d.Cr e.C
(2)第一电离能介于B、N之间的第二周期元素有
(3)已知HCO3-在水溶液中可通过氢键成为二聚体(八元环结构),试画出该二聚体的结构式:
(4)[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2-+4H++4H2O
 [Zn(H2O)4]2++4HOCH2CN
[Zn(H2O)4]2++4HOCH2CN①Zn2+基态核外电子排布式为
②HOCH2CN分子中碳原子轨道的杂化类型是
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
Ⅱ.由原子序数由小到大的A、B、C、D、E五种元素构成某配位化合物X,其原子个数比为14∶4∶5∶1∶1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6ns1,回答下列问题。
(1)该配位化合物X的化学式为
(2)元素B、C、D的第一电离能由小到大排列顺序为
(3)D元素原子的最外层电子轨道表示式为
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可任意比互溶,解释其主要原因为
(5)A元素与E元素可形成一种红色离子化合物Y,其原子个数比为1∶1,该化合物Y可与稀硝酸反应,生成一种蓝色溶液和两种无色气体(其中一种为A元素的单质),写出该反应的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铬云母是一些玉石、彩石的重要组成和着色矿物。理想的组分是含Al的八面体片,化学式为KAl2[Si3AlO10](OH,F)2,其中的Al也可少量地被Fe、Mg、Mn、Cr、V等替换。
(1)基态Cr原子的核外电子排布式为__ 。
(2)基态锰原子核外电子排布中能量最高的能级符号为___ 。
(3)O、F、Si三种元素的第一电离能由大到小的顺序为___ 。
(4)O、F、Si与H形成的氢化物有H2O2、H2O、HF、SiH4、Si2H6等。
①SiH4中Si原子的杂化方式为__ 。
②H2O、HF、SiH4三种物质中沸点最高的是__ 。
③等物质的量的H2O2与Si2H6所含σ键数目之比为__ 。
(1)基态Cr原子的核外电子排布式为
(2)基态锰原子核外电子排布中能量最高的能级符号为
(3)O、F、Si三种元素的第一电离能由大到小的顺序为
(4)O、F、Si与H形成的氢化物有H2O2、H2O、HF、SiH4、Si2H6等。
①SiH4中Si原子的杂化方式为
②H2O、HF、SiH4三种物质中沸点最高的是
③等物质的量的H2O2与Si2H6所含σ键数目之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】工业废水中常含有一定量的 ,利用滴定原理测定
,利用滴定原理测定 含量的方法如下:
含量的方法如下:
步骤Ⅰ:量取30.00 mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液并放于暗处充分反应,其中 转化为
转化为 。
。
步骤Ⅲ:向锥形瓶中滴加几滴淀粉溶液。用滴定管量取0.1 000 mol·L-1 溶液进行滴定,数据记录如下:(
溶液进行滴定,数据记录如下:( )
)
(1)步骤Ⅰ量取30.00 mL废水,选择的仪器是_______ 。
(2)滴定达到终点时的实验现象是_______ 。
(3)以下操作会造成废水中 含量测定值偏小的是
含量测定值偏小的是_______ (填字母)。
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.量取 溶液的滴定管用蒸馏水洗后未用标准液润洗
溶液的滴定管用蒸馏水洗后未用标准液润洗
E.步骤Ⅱ中“放于暗处反应”,若未放于暗处
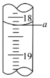
(4)步骤Ⅲ中a的读数如下图所示,则 的含量为
的含量为_______ g·L (写出计算过程)。
(写出计算过程)。
 ,利用滴定原理测定
,利用滴定原理测定 含量的方法如下:
含量的方法如下:步骤Ⅰ:量取30.00 mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液并放于暗处充分反应,其中
 转化为
转化为 。
。步骤Ⅲ:向锥形瓶中滴加几滴淀粉溶液。用滴定管量取0.1 000 mol·L-1
 溶液进行滴定,数据记录如下:(
溶液进行滴定,数据记录如下:( )
)| 实验次数 | 第一次(mL) | 第二次(mL) | 第三次(mL) |
 溶液原始读数 溶液原始读数 | 1.02 | 2.00 | 0.20 |
 溶液终点读数 溶液终点读数 | 19.03 | 19.99 | a |
(1)步骤Ⅰ量取30.00 mL废水,选择的仪器是
(2)滴定达到终点时的实验现象是
(3)以下操作会造成废水中
 含量测定值偏小的是
含量测定值偏小的是A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.量取
 溶液的滴定管用蒸馏水洗后未用标准液润洗
溶液的滴定管用蒸馏水洗后未用标准液润洗E.步骤Ⅱ中“放于暗处反应”,若未放于暗处
(4)步骤Ⅲ中a的读数如下图所示,则
 的含量为
的含量为 (写出计算过程)。
(写出计算过程)。
您最近一年使用:0次
【推荐2】某班同学用氢氧化钠溶液和稀硫酸进行中和反应实验:
(1)甲同学在烧杯中加入约5mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈____ 色,接着用滴管滴入一定量的稀硫酸,再用玻璃棒搅拌,发现溶液变为无色,该反应的化学方程式为____ 。
(2)甲、乙、丙同学对反应后溶液中的溶质成分进行探究。
【猜想与假设】反应后溶液中的溶质是什么?
猜想一:只有Na2SO4;
猜想二:_______ 。
猜想三:可能是Na2SO4和NaOH
以上猜想中,可以直接排除的是_______ ,理由_______ 。
【实验探究】
为了验证另外两种猜想,甲、乙、丙同学设计如下实验方案:
老师认为甲同学方案不合理,你认为理由是_______ 。
【反思交流】实验结束后,废液处理方法正确的是_______ (填序号)。
A.倒入下水道 B.倒入废液缸
(1)甲同学在烧杯中加入约5mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈
(2)甲、乙、丙同学对反应后溶液中的溶质成分进行探究。
【猜想与假设】反应后溶液中的溶质是什么?
猜想一:只有Na2SO4;
猜想二:
猜想三:可能是Na2SO4和NaOH
以上猜想中,可以直接排除的是
【实验探究】
为了验证另外两种猜想,甲、乙、丙同学设计如下实验方案:
| 实验操作 | 实验现象 | 实验结论 | |
| 甲同学方案 | 取少量反应后的溶液于试管中,向试管中滴加BaCl2溶液, | 有白色沉淀产生。 | 猜想二成立 |
| 乙同学方案 | 取少量反应后的溶液于试管中,向试管中加入 | 有气泡产生。 | 猜想二成立 |
| 丙同学方案 | 取少量反应后的溶液于试管中,向试管中加入生锈的铁钉。 | 猜想二成立 |
【反思交流】实验结束后,废液处理方法正确的是
A.倒入下水道 B.倒入废液缸
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】甲酸钙广泛用于食品、工、石油等工业生产上,300~400℃左右分解.
Ⅰ、实验室制取的方法之一是:Ca(OH)2+2HCHO+H2O2=Ca(HCOO)2+2H2O+H2↑.
实验室制取时,将工业用氢氧化钙和甲醛依次加入到质量分数为30-70%的过氧化氢溶液中(投料物质的量之比依次为1:2:1.2),最终可得到质量分数98%以上且重金属含量极低的优质产品.
(1)过氧化氢比理论用量稍多,其目的是____________ 。
(2)反应温度最好控制在30-70℃之间,温度不易过高,其主要原因是____________ 。
(3)制备时在混合溶液中要加入微量硼酸钠抑制甲醛发生副反应外,还要加入少量的Na2S溶液,加硫化钠的目的是____________ 。
(4)实验时需强力搅拌45min,其目的是____________ ;结束后需调节溶液的pH 7~8,其目的是____________ ,最后经结晶分离、干燥得产品.
Ⅱ、某研究性学习小组用工业碳酸钙(主要成分为CaCO3;杂质为:Al2O3、FeCO3) 为原料,先制备无机钙盐,再与甲酸钠溶液混合制取甲酸钙.结合右图几种物质的溶解度曲线及表中相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算)。

请补充完整由碳酸钙制备甲酸钙的实验方案:称取13.6g甲酸钠溶于约20mL水,配成溶液待用,并称取研细的碳酸钙样品10g待用;____________ 。
提供的试剂有:a.甲酸钠,B.5mol•L-1硝酸,C.5mol•L-1盐酸,D.5mol•L-1硫酸,e.3%H2O2溶液,f.澄清石灰水。
Ⅰ、实验室制取的方法之一是:Ca(OH)2+2HCHO+H2O2=Ca(HCOO)2+2H2O+H2↑.
实验室制取时,将工业用氢氧化钙和甲醛依次加入到质量分数为30-70%的过氧化氢溶液中(投料物质的量之比依次为1:2:1.2),最终可得到质量分数98%以上且重金属含量极低的优质产品.
(1)过氧化氢比理论用量稍多,其目的是
(2)反应温度最好控制在30-70℃之间,温度不易过高,其主要原因是
(3)制备时在混合溶液中要加入微量硼酸钠抑制甲醛发生副反应外,还要加入少量的Na2S溶液,加硫化钠的目的是
(4)实验时需强力搅拌45min,其目的是
Ⅱ、某研究性学习小组用工业碳酸钙(主要成分为CaCO3;杂质为:Al2O3、FeCO3) 为原料,先制备无机钙盐,再与甲酸钠溶液混合制取甲酸钙.结合右图几种物质的溶解度曲线及表中相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算)。

| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
提供的试剂有:a.甲酸钠,B.5mol•L-1硝酸,C.5mol•L-1盐酸,D.5mol•L-1硫酸,e.3%H2O2溶液,f.澄清石灰水。
您最近一年使用:0次



