已知分解1 mol H2O2放出热量98 kJ。在含少量I-的溶液中,H2O2分解的机理为:
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是
| A.是自发反应 | B.IO-也是该反应的催化剂 |
| C.整个反应的快慢由第一步决定 | D.反应活化能等于98 kJ·mol-1 |
更新时间:2024-01-10 12:13:51
|
相似题推荐
【推荐1】反应N2(g)+O2(g)=2NO(g)的能量变化如图所示。已知:断开1 mol N2(g)中化学键需吸收946 kJ能量,断开1 molO2(g)中化学键需吸收498 kJ 能量。下列说法正确的是


| A.1mol N2(g)所具有的能量为946 kJ,1 mol O2(g)所具有的能量为498kJ |
| B.该反应是化合反应,放热反应 |
| C.断开l mol NO(g)中化学键需要吸收632 kJ能量 |
| D.形成l mol NO(g)中化学键可释放90 kJ能量 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是N2与H2反应生成NH3的过程中能量变化的曲线图:下列叙述正确的是。


| A.b曲线是加入催化剂时的能量变化曲线 |
| B.加入催化剂,该化学反应的反应热减小 |
| C.该反应的热化学方程式为N2(g)+3H2(g)=2NH3(g) ΔH=-92 kJ |
| D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2kJ,则184>Q2>2Q1 |
您最近一年使用:0次
【推荐1】Burns和Dainton研究发现Cl2与CO合成COCl2的反应机理如下: ①Cl2(g)  2Cl•(g)快;②CO(g)+Cl•(g)
2Cl•(g)快;②CO(g)+Cl•(g) COCl•(g)快;③COCl•(g)+Cl2(g)
COCl•(g)快;③COCl•(g)+Cl2(g) COCl2(g)+Cl•(g)慢。其中反应②存在v正=k正c(CO) c(C1•)、v逆=k逆c(COCl•)。下列说法正确的是
COCl2(g)+Cl•(g)慢。其中反应②存在v正=k正c(CO) c(C1•)、v逆=k逆c(COCl•)。下列说法正确的是
| A.反应①的活化能大于反应③的活化能 |
B.反应②的平衡常数K=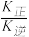 |
| C.要提高合成COCl2的速率,关键是提高反应③的速率 |
| D.选择合适的催化剂能加快该反应的速率,并提高COCl2的平衡产率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】甲醇通过催化氧化制取甲醛时,在无催化剂(图中实线)和加入特定催化剂(图中虚线)时均会产生甲醛,其反应中相关物质的相对能量如图所示。下列说法错误的是


| A.无催化剂时,温度升高,生成甲醛的正反应速率增大的程度比逆反应速率增大程度大 |
| B.无催化剂时,生成CO比生成甲醛的活化能小 |
| C.该条件下CO2比CO的稳定性强 |
| D.加入该催化剂可提高图中各反应的速率,但不能改变反应的焓变 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】根据下列图示所得出的结论不正确的是
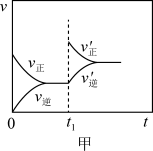
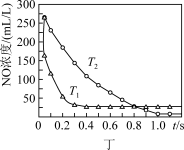




A.图甲表示2SO2(g)+O2(g) 2SO3(g) △H<0,t1时改变的条件是增大体系的压强 2SO3(g) △H<0,t1时改变的条件是增大体系的压强 |
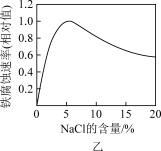
| B.图乙NaCl溶液浓度过高铁腐蚀速率降低,说明NaCl浓度越大溶液中O2的浓度越小 |
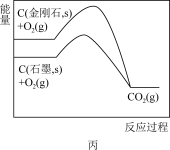
| C.图丙说明石墨转化为金刚石的反应的△H<0 |
D.图丁是一定条件下发生反应:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g)此过程△H<0 4N2(g)+6H2O(g)此过程△H<0 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】已知分解 ,放出热量98kJ,在含少量I-的溶液中,
,放出热量98kJ,在含少量I-的溶液中, 分解的机理为
分解的机理为
 (慢)、
(慢)、 (快)。下列有关该反应的说法错误的是
(快)。下列有关该反应的说法错误的是
 ,放出热量98kJ,在含少量I-的溶液中,
,放出热量98kJ,在含少量I-的溶液中, 分解的机理为
分解的机理为
 (慢)、
(慢)、 (快)。下列有关该反应的说法错误的是
(快)。下列有关该反应的说法错误的是A.化学反应速率与 浓度无关 浓度无关 |
B.化学反应速率 |
C.反应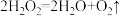 的反应热 的反应热 |
| D. I-是该反应的催化剂 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】CO2/HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。下列说法不正确的是
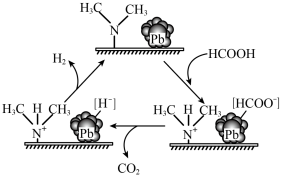

| A.如HCOOD催化释氢反应除生成CO2外,还生成HD |
| B.其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳 |
C.在密闭容器中,向含有催化剂的KHCO3溶液中通H2可生成HCOO-,其离子方程式为:2 +H2 +H2 HCOO-+H2O+CO2+OH- HCOO-+H2O+CO2+OH- |
| D.该过程有气体产生,温度越高越有利HCOOH分解 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】已知 ,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,
,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注, 为过渡态)。
为过渡态)。
 ,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,
,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注, 为过渡态)。
为过渡态)。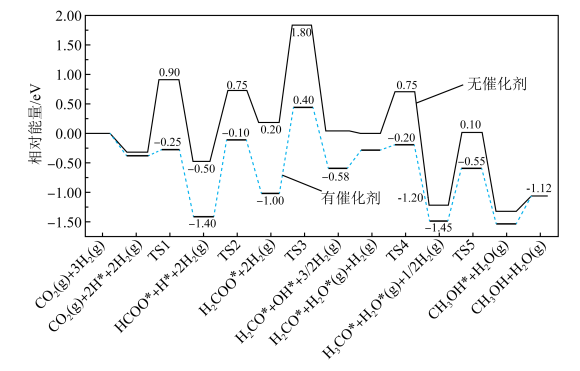
A.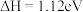 |
B.无催化剂时,决速步骤的方程式为 |
| C.使用催化剂,降低了反应的活化能和焓变 |
| D.该反应在低温下易自发进行 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
A.某浓度的氨水加水稀释后 pH 变小,则其中的c(NH3·H2O)/c(NH )的值也减小 )的值也减小 |
| B.向 AgCl 悬浊液中加入少量 KI 溶液,沉淀转化为黄色,说明 Ksp(AgI)>Ksp(AgCl) |
| C.常温下,MgO(s)+C(s)=Mg(s)+CO(g)不能自发进行,则其△H>0 |
| D.室温下,pH=3 的 CH3COOH 溶液与pH=11 的 NaOH 溶液等体积混合,溶液 pH>7 |
您最近一年使用:0次

 、4mol
、4mol  的混合气体,发生反应:
的混合气体,发生反应: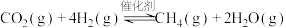
 ,8min时反应刚好达到平衡,测得此时容器内
,8min时反应刚好达到平衡,测得此时容器内 为0.4mol。下列说法正确的是
为0.4mol。下列说法正确的是

 2NOBr(g)
2NOBr(g)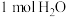 在不同状态时的熵值:
在不同状态时的熵值: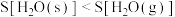
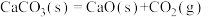
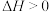 能否自发进行与温度有关
能否自发进行与温度有关 不能自发进行,则该反应的
不能自发进行,则该反应的


