中国科学家在淀粉人工光合成方面取得重大突破性进展,该实验方法首先将CO2催化还原为CH3OH。已知CO2催化加氢的主要反应有:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=﹣49.4kJ/mol
CH3OH(g)+H2O(g) ΔH1=﹣49.4kJ/mol
②CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41.2kJ/mol
CO(g)+H2O(g) ΔH2=+41.2kJ/mol
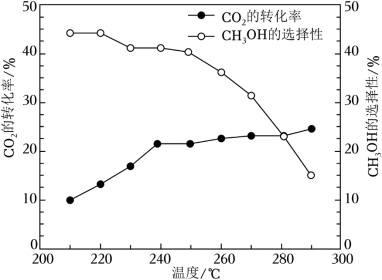
其他条件不变时,在相同时间内温度对CO2催化加氢的影响如图。下列说法不正确的是
【注】CH3OH的选择性= ×100%
×100%
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=﹣49.4kJ/mol
CH3OH(g)+H2O(g) ΔH1=﹣49.4kJ/mol②CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41.2kJ/mol
CO(g)+H2O(g) ΔH2=+41.2kJ/mol其他条件不变时,在相同时间内温度对CO2催化加氢的影响如图。下列说法不正确的是
【注】CH3OH的选择性=
 ×100%
×100%
A.CO(g)+2H2(g) CH3OH(g) ΔH=﹣90.6kJ/mol CH3OH(g) ΔH=﹣90.6kJ/mol |
| B.使用催化剂,能降低反应的活化能,增大活化分子百分数 |
| C.其他条件不变,增大压强,有利于反应向生成CH3OH的方向进行 |
| D.0~240℃,升高温度,对反应②速率的影响比对反应①的小 |
更新时间:2024-01-11 09:27:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法或表示方法中正确的是
| A.HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=-2×57.3kJ·mol-1 |
B.101kPa时,H2的热值为142.75kJ·g-1,则表示氢气标准燃烧热的热化学方程式为:H2(g)+ O2(g)=H2O(l) ΔH=-142.75kJ·mol-1 O2(g)=H2O(l) ΔH=-142.75kJ·mol-1 |
| C.由C(金刚石)=C(石墨) ΔH=-1.9kJ·mol-1可知,金刚石比石墨稳定 |
| D.若CO(g)的燃烧热ΔH=-283.0kJ·mol-1,则反应2CO2(g)=2CO(g)+O2(g)的ΔH=2×283.0kJ·mol-1 |
您最近一年使用:0次
【推荐2】已知反应:
①丙烷与溴原子能发生以下两种反应:
CH3CH2CH3(g) + Br·(g)→CH3CH2CH2·(g) + HBr(g) ΔH= +376kJ·mol-1
CH3CH2CH3(g) + Br·(g)→CH3CH·CH3 (g) + HBr(g) ΔH +254 kJ·mol-1
②稀溶液中,H +(aq) +OH-(aq) =H2O(1) ΔH = -57.3 kJ·mol-1
下列结论正确的是
①丙烷与溴原子能发生以下两种反应:
CH3CH2CH3(g) + Br·(g)→CH3CH2CH2·(g) + HBr(g) ΔH= +376kJ·mol-1
CH3CH2CH3(g) + Br·(g)→CH3CH·CH3 (g) + HBr(g) ΔH +254 kJ·mol-1
②稀溶液中,H +(aq) +OH-(aq) =H2O(1) ΔH = -57.3 kJ·mol-1
下列结论正确的是
| A.CH3CH2CH2·(g)转变为CH3CH·CH3 (g)时需要吸热 |
| B.反应②可以代表所有稀酸和稀碱生成lmol水的中和反应 |
| C.对于CH3CH2CH3(g) + Br·(g)→CH3CH2CH2·(g) + HBr(l) ΔH <376 kJ·mol-1 |
| D.pH=3 的醋酸与pH=11的NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关平衡常数的说法中,正确的是
| A.改变条件,反应物的转化率增大,平衡常数也一定增大 |
B.反应2NO2(g) N2O4(g) △H <0,升高温度该反应平衡常数增大 N2O4(g) △H <0,升高温度该反应平衡常数增大 |
| C.对于给定可逆反应,温度一定时,其正、逆反应的平衡常数相等 |
D.CO2+H2  CO+H2O的平衡常数表达式为K== CO+H2O的平衡常数表达式为K==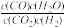 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知下列反应的反应热:
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ⋅mol-1
(2)C(s)+O2(g)=CO2(g) △H2=-393.5kJ⋅mol-1
(3)H2(g)+ O2(g)=H2O(l) △H3=-285.8kJ⋅mol-1
O2(g)=H2O(l) △H3=-285.8kJ⋅mol-1
则下列反应的反应热为
2C(s)+2H2(g)+O2(g)=CH3COOH(l)
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ⋅mol-1
(2)C(s)+O2(g)=CO2(g) △H2=-393.5kJ⋅mol-1
(3)H2(g)+
 O2(g)=H2O(l) △H3=-285.8kJ⋅mol-1
O2(g)=H2O(l) △H3=-285.8kJ⋅mol-1则下列反应的反应热为
2C(s)+2H2(g)+O2(g)=CH3COOH(l)
| A.△H=+488.3kJ⋅mol-1 | B.△H=-244.15kJ⋅mol-1 |
| C.△H=-977.6kJ⋅mol-1 | D.△H=-488.3kJ⋅mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知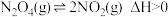 在瞬间即可达成化学平衡。NO2和N2O4混合气体体积由V压缩至
在瞬间即可达成化学平衡。NO2和N2O4混合气体体积由V压缩至 时,相关数据变化如下表。根据表中数据得出若干结论,下列结论
时,相关数据变化如下表。根据表中数据得出若干结论,下列结论不正确 的是
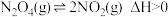 在瞬间即可达成化学平衡。NO2和N2O4混合气体体积由V压缩至
在瞬间即可达成化学平衡。NO2和N2O4混合气体体积由V压缩至 时,相关数据变化如下表。根据表中数据得出若干结论,下列结论
时,相关数据变化如下表。根据表中数据得出若干结论,下列结论| 温度/L | 气体的总压强/Pa | NO2的物质的量浓度/mol·L-1 | |
 | 298 | 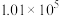 | 1.28×10-2 |
 | 311 | 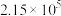 | 2.80×10-2 |
A.体积由V压缩至 时,NO2的物质的量增大 时,NO2的物质的量增大 |
| B.正反应和逆反应的活化能均较低 |
| C.体积缩小后混合气体的颜色加深 |
| D.其它条件不变,温度升高,该反应逆向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】向某恒温恒压的密闭容器中加入等物质的量的 和
和 ,发生反应:
,发生反应: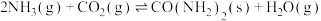 。下列说法错误的是
。下列说法错误的是
 和
和 ,发生反应:
,发生反应: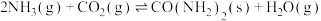 。下列说法错误的是
。下列说法错误的是A.体系中 的体积分数始终是50% 的体积分数始终是50% |
B.体系达到平衡时,断裂2mol 键的同时断裂2mol 键的同时断裂2mol 键 键 |
C.通过及时分离出 ,可促进平衡右移,提高反应限度 ,可促进平衡右移,提高反应限度 |
| D.体系达平衡后,恒温下恢复至初始体积并恒容,达新平衡时反应速率比原平衡慢 |
您最近一年使用:0次

 O2(g)=2CO2(g)+H2O(g) △H=-1256kJ·mol-1,下列说法正确的是
O2(g)=2CO2(g)+H2O(g) △H=-1256kJ·mol-1,下列说法正确的是
 nB(g)ΔH==Q kJ·mol-1。反应达到平衡时,B的物质的量浓度与温度、容器容积的关系如表所示。下列说法正确的是
nB(g)ΔH==Q kJ·mol-1。反应达到平衡时,B的物质的量浓度与温度、容器容积的关系如表所示。下列说法正确的是


