随着新能源汽车销量的猛增,动力电池退役高峰将至,磷酸铁锂(LFP)是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片( 、导电石墨、铝箔)中回收锂的工艺流程如下:
、导电石墨、铝箔)中回收锂的工艺流程如下:
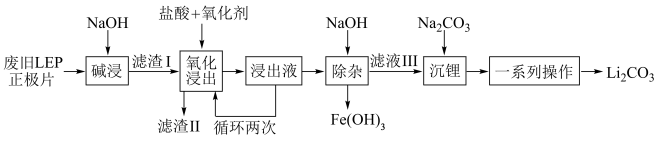
已知: 在水中的溶解度随温度升高而降低。
在水中的溶解度随温度升高而降低。
回答下列问题:
(1)旧电池拆解前进行放电处理有利于锂在正极的回收,其原因是___________ 。
(2)“碱浸”时,为加快浸出速率,可采取的措施是___________ (答出一点即可)。
(3)“氧化浸出”时,实际生产中氧化剂选用 ,不选用
,不选用 的原因是
的原因是___________ 。“氧化浸出”时生成了难溶的 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(4)“沉锂”过程中使用水浴加热保持温度在95℃,“一系列操作”具体包括___________ 、___________ 、干燥。
(5)滤液Ⅲ中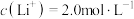 ,“沉锂”结束时溶液中
,“沉锂”结束时溶液中 为
为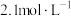 ,则“沉锂”过程中,锂的沉降率为
,则“沉锂”过程中,锂的沉降率为___________ %[已知:浸出液在沉锂过程中溶液体积不变,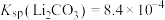 ]。
]。
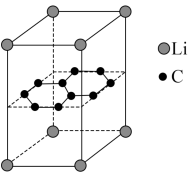
(6)某锂电池的负极材料晶体是锂原子嵌入石墨烯层间形成的,晶胞结构(底面为平行四边形)如图所示。该晶体的化学式为___________ ,该晶体中最近的两个碳原子核间距离为apm,石墨烯层间距离为bpm,则该晶体的密度为___________  (列出计算式,用
(列出计算式,用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
 、导电石墨、铝箔)中回收锂的工艺流程如下:
、导电石墨、铝箔)中回收锂的工艺流程如下:
已知:
 在水中的溶解度随温度升高而降低。
在水中的溶解度随温度升高而降低。回答下列问题:
(1)旧电池拆解前进行放电处理有利于锂在正极的回收,其原因是
(2)“碱浸”时,为加快浸出速率,可采取的措施是
(3)“氧化浸出”时,实际生产中氧化剂选用
 ,不选用
,不选用 的原因是
的原因是 ,该反应的离子方程式为
,该反应的离子方程式为(4)“沉锂”过程中使用水浴加热保持温度在95℃,“一系列操作”具体包括
(5)滤液Ⅲ中
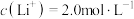 ,“沉锂”结束时溶液中
,“沉锂”结束时溶液中 为
为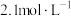 ,则“沉锂”过程中,锂的沉降率为
,则“沉锂”过程中,锂的沉降率为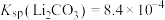 ]。
]。(6)某锂电池的负极材料晶体是锂原子嵌入石墨烯层间形成的,晶胞结构(底面为平行四边形)如图所示。该晶体的化学式为
 (列出计算式,用
(列出计算式,用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
23-24高三上·湖南长沙·阶段练习 查看更多[2]
更新时间:2024-01-23 22:10:33
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】对废旧干电池拆解后的碳包滤渣(含 、C、
、C、 等)再加工,既可制取高纯
等)再加工,既可制取高纯 又可消除废弃物对环境的污染。实验流程如下:
又可消除废弃物对环境的污染。实验流程如下:
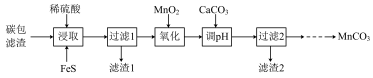
已知: ,MnS都是不溶于水的沉淀。
,MnS都是不溶于水的沉淀。
(1)“浸取”时,为了提高碳包滤渣的浸取率,除了控制温度70℃左右外,还可以采取的措施有___________ (写出一种即可),浸取后生成 和
和 ,则浸取过程中发生的主要反应的化学方程式为
,则浸取过程中发生的主要反应的化学方程式为___________ 。
(2)实验流程中,“氧化”步骤的目的是___________ ;滤渣2的主要成分为___________ (填化学式)。
(3)为了提高 的纯度,滤液
的纯度,滤液 溶液与
溶液与 溶液的混合方式为
溶液的混合方式为___________ 。
(4) 产率与“浸取”时
产率与“浸取”时 的投料比关系如图所示,FeS用量超过最佳值时,
的投料比关系如图所示,FeS用量超过最佳值时, 产率反而变小的原因是
产率反而变小的原因是___________ 。

 、C、
、C、 等)再加工,既可制取高纯
等)再加工,既可制取高纯 又可消除废弃物对环境的污染。实验流程如下:
又可消除废弃物对环境的污染。实验流程如下:
已知:
 ,MnS都是不溶于水的沉淀。
,MnS都是不溶于水的沉淀。(1)“浸取”时,为了提高碳包滤渣的浸取率,除了控制温度70℃左右外,还可以采取的措施有
 和
和 ,则浸取过程中发生的主要反应的化学方程式为
,则浸取过程中发生的主要反应的化学方程式为(2)实验流程中,“氧化”步骤的目的是
(3)为了提高
 的纯度,滤液
的纯度,滤液 溶液与
溶液与 溶液的混合方式为
溶液的混合方式为(4)
 产率与“浸取”时
产率与“浸取”时 的投料比关系如图所示,FeS用量超过最佳值时,
的投料比关系如图所示,FeS用量超过最佳值时, 产率反而变小的原因是
产率反而变小的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】K2FeO4具有强氧化性,易溶于水,可迅速杀灭水体中的细菌。某化学小组通过如图装置以Cl2、Fe(OH)3和KOH为 原料制备K2FeO4。

回答下列问题:
(1)K2FeO4属于___________ (填选项字母),其电离方程式为___________ 。
A.酸 B.碱 C.有机物 D.盐
(2)实验前,检查装置 A 气密性的操作为关闭止水夹K1,通过分液漏斗向圆底烧瓶中加水,若观察到___________ ,则证明装置A气密性良好。
(3)写出装置A中发生反应的离子方程式:___________ 。
(4)若装置 A 中生成5.6 L Cl2(标准状况),则转移电子的物质的量为___________ mol,作还原剂的 HCl的质量为 ___________ g。
(5)装置B中的试剂a为___________ 。
(6)装置 C 中发生的反应为 (未配平),该反应中氧化剂和还原剂的物质的量之比为
(未配平),该反应中氧化剂和还原剂的物质的量之比为___________ 。
(7)装置D中发生反应的离子方程式为___________ 。

回答下列问题:
(1)K2FeO4属于
A.酸 B.碱 C.有机物 D.盐
(2)实验前,检查装置 A 气密性的操作为关闭止水夹K1,通过分液漏斗向圆底烧瓶中加水,若观察到
(3)写出装置A中发生反应的离子方程式:
(4)若装置 A 中生成5.6 L Cl2(标准状况),则转移电子的物质的量为
(5)装置B中的试剂a为
(6)装置 C 中发生的反应为
 (未配平),该反应中氧化剂和还原剂的物质的量之比为
(未配平),该反应中氧化剂和还原剂的物质的量之比为(7)装置D中发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】中学化学中几种常见物质的转化关系如下:

将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)写出A、B、H的化学式:A___________ 、B___________ 、H___________ 。
(2)写出C的酸性溶液与双氧水反应的离子方程式:___________ 。
(3)写出鉴定E中阳离子的实验方法和现象:___________ 。
(4)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:___________ 。

将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)写出A、B、H的化学式:A
(2)写出C的酸性溶液与双氧水反应的离子方程式:
(3)写出鉴定E中阳离子的实验方法和现象:
(4)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(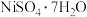 ):
):
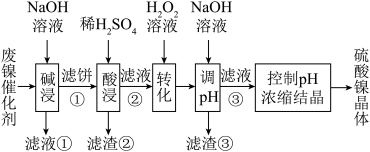
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中 的两个作用分别是除去油脂和
的两个作用分别是除去油脂和___________ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式___________ 。
(2)“转化”中可替代 的最佳物质是___________。
的最佳物质是___________。
(3)利用上述表格数据,计算 的
的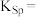
___________ 。如果“转化”后的溶液中 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是___________ 。
(4)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是___________ 。
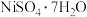 ):
):
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |  |
开始沉淀时(c=0.01mol/L)的 | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时(c=1.0×10-5mol/L)的 | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中
 的两个作用分别是除去油脂和
的两个作用分别是除去油脂和(2)“转化”中可替代
 的最佳物质是___________。
的最佳物质是___________。A.酸性 溶液 溶液 | B. | C.硝酸 | D.新制氯水 |
(3)利用上述表格数据,计算
 的
的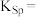
 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是(4)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】活性氧化锌(ZnO)广泛用于橡胶、涂料、陶瓷、电子等行业,以粗氧化锌(主要成分为ZnO,还含有少量MnO、CuO、FeO、Fe2O3等)为原料经深度净化可制备高纯活性氧化锌,其流程如图所示:
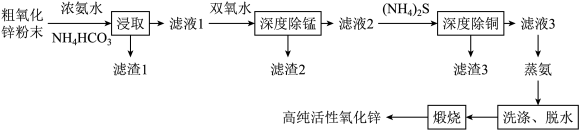
几种难溶物的Ksp:
(1)将大小为66nm的高纯活性氧化锌粉末分散到水中,所得分散系为______ 。
(2)“浸取”过程中ZnO与NH3·H2O、NH4HCO3反应生成可溶性的Zn[(NH3)n]CO3和H2O。若有1mol ZnO溶解,则在该转化反应中参加反应的NH3·H2O和NH4HCO3物质的量之比的最大值为___________ (已知:1≤n≤4)。
(3)“深度除锰”过程中双氧水可将“滤液1”中的Mn(OH)2转化为更难溶的MnO2·H2O,写出反应的化学方程式______________ ,“滤渣2”中存在的物质除了MnO2·H2O还可能含有_________ (用化学式表示)。
(4)“深度除铜”过程中当溶液中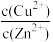 ≤2.0×10-6时,才能满足“深度除铜”的要求,若溶液中Zn2+浓度为1mol/L时,则最终溶液中S2-的浓度理论上的最小值为
≤2.0×10-6时,才能满足“深度除铜”的要求,若溶液中Zn2+浓度为1mol/L时,则最终溶液中S2-的浓度理论上的最小值为____ mol/L。
(5)“蒸氨”过程中Zn[(NH3)n]CO3分解为ZnCO3·2Zn(OH)2·H2O、NH3和CO2。为了提高经济效益,请设计循环利用NH3和CO2方案_____________ 。
(6)“煅烧”时ZnCO3·2Zn(OH)2转变为高纯活性氧化锌,写出反应的化学方程式______

几种难溶物的Ksp:
| 物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | ZnS | CuS |
| Ksp | 1.9×10-13 | 8.0×10-16 | 4.0×10-38 | 2.5×10-22 | 6.4×10-36 |
(2)“浸取”过程中ZnO与NH3·H2O、NH4HCO3反应生成可溶性的Zn[(NH3)n]CO3和H2O。若有1mol ZnO溶解,则在该转化反应中参加反应的NH3·H2O和NH4HCO3物质的量之比的最大值为
(3)“深度除锰”过程中双氧水可将“滤液1”中的Mn(OH)2转化为更难溶的MnO2·H2O,写出反应的化学方程式
(4)“深度除铜”过程中当溶液中
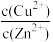 ≤2.0×10-6时,才能满足“深度除铜”的要求,若溶液中Zn2+浓度为1mol/L时,则最终溶液中S2-的浓度理论上的最小值为
≤2.0×10-6时,才能满足“深度除铜”的要求,若溶液中Zn2+浓度为1mol/L时,则最终溶液中S2-的浓度理论上的最小值为(5)“蒸氨”过程中Zn[(NH3)n]CO3分解为ZnCO3·2Zn(OH)2·H2O、NH3和CO2。为了提高经济效益,请设计循环利用NH3和CO2方案
(6)“煅烧”时ZnCO3·2Zn(OH)2转变为高纯活性氧化锌,写出反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】利用“铁脱络-化学沉淀法”回收电镀废水中镍的流程如图。

已知:①废水中镍主要以NiR2络合物形式存在,其在水溶液中存在平衡:NiR2(aq)⇌Ni2+(aq)+2R-(aq,有机配体)K=1.6×10-14。
②常温下,Ksp[Fe(OH)3]=1×10-39,Ksp[Ni(OH)2]=1.6×10-15。
③“脱络”(指NiR2转化成Ni2+)过程中,反应历程如下:
i.Fe2++H2O2=Fe3++OH-+·OH
ii.R-+·OH=OH-+·R
iii.H2O2+2·OH=O2↑+2H2O
(1)·OH的电子式为_______ ,其中氧元素的化合价为_______ 价。
(2)①根据·OH与H2O2的反应历程,分析“脱络”时加入的Fe2+的作用机制:_______ 。
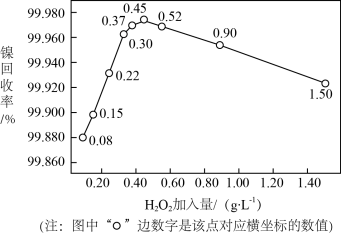
②实验测得H2O2加入量对溶液中镍回收率的影响如图所示。由图可知,当加入H2O2的量为_______ g·L-1时,镍回收效果最好;当加入H2O2的量较大时,镍回收回率下降,可能的原因是_______ 。
(3)常温下,若“脱络”后的废水中c(Ni2+)=0.01mol·L-1,“沉淀”时先加入NaOH至溶液的pH=_______ ,使Fe3+恰好沉淀完全(Fe3+浓度为10-6mol·L-1,忽略溶液体积变化),此时_______ (填“有”或“无”)Ni(OH)2沉淀生成。
(4)取100mL某电镀废水利用上述流程回收镍,得到2.325gNi(OH)2沉淀,经计算该步骤中Ni2+的回收率为99.97%;Ni(OH)2沉淀再经稀硫酸溶解、_______ 、过滤,得到NiSO4·7H2O固体的质量为6.744g。试计算100mL该电镀废水中镍转化成NiSO4·7H2O的总回收率:_______ (保留四位有效数字)。

已知:①废水中镍主要以NiR2络合物形式存在,其在水溶液中存在平衡:NiR2(aq)⇌Ni2+(aq)+2R-(aq,有机配体)K=1.6×10-14。
②常温下,Ksp[Fe(OH)3]=1×10-39,Ksp[Ni(OH)2]=1.6×10-15。
③“脱络”(指NiR2转化成Ni2+)过程中,反应历程如下:
i.Fe2++H2O2=Fe3++OH-+·OH
ii.R-+·OH=OH-+·R
iii.H2O2+2·OH=O2↑+2H2O
(1)·OH的电子式为
(2)①根据·OH与H2O2的反应历程,分析“脱络”时加入的Fe2+的作用机制:
②实验测得H2O2加入量对溶液中镍回收率的影响如图所示。由图可知,当加入H2O2的量为

(3)常温下,若“脱络”后的废水中c(Ni2+)=0.01mol·L-1,“沉淀”时先加入NaOH至溶液的pH=
(4)取100mL某电镀废水利用上述流程回收镍,得到2.325gNi(OH)2沉淀,经计算该步骤中Ni2+的回收率为99.97%;Ni(OH)2沉淀再经稀硫酸溶解、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
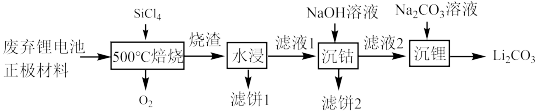
【推荐1】近几年新能源汽车呈现爆发式增长,对于锂电池的需求量越来越大,而碳酸锂是锂电池的重要原料之一,对废旧锂离子电池进行资源化和无害化处理具有重要的经济和环境效益,利用SiCl4对废弃的锂电池正极材料LiCoO2)进行氧化处理以回收Li等金属的工艺流程如下:
(1)Co在元素周期表的位置是___________ ,Co2+与Co3+的未成对电子数之比为___________ 。
(2)“烧渣”是LiCl、CoCl2和SiO2的混合物。“ 焙烧”反应生成的氧化产物与还原产物的物质的量之比为
焙烧”反应生成的氧化产物与还原产物的物质的量之比为___________ 。
(3)“滤饼2”的主要成分为___________ (填化学式)。利用Li2CO3与CoCO3按n(Li):n(Co)=1:1的比例配合,然后在空气中于 烧结可合成锂电池正极材料LiCoO2,反应的化学方程式为
烧结可合成锂电池正极材料LiCoO2,反应的化学方程式为___________ 。
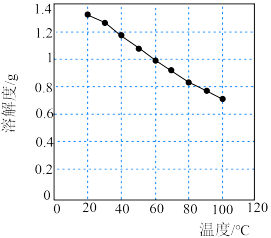
(4)碳酸锂的溶解度随温度变化如图所示。向滤液2中加入Na2CO3溶液,将温度升至90℃是为了提高沉淀反应速率和___________ 。得到碳酸锂沉淀的操作为___________ (填标号)。
(5)常温下,取 “滤液2”,其中
“滤液2”,其中 ,为使锂元素的回收率不低于
,为使锂元素的回收率不低于 ,则至少应加入
,则至少应加入 固体的质量为
固体的质量为___________ g[已知常温下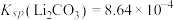 。计算结果保留3位小数。
。计算结果保留3位小数。
(6)由 进一步制得的
进一步制得的 具有反萤石结构,晶胞如图所示。
具有反萤石结构,晶胞如图所示。 在晶胞中的位置为
在晶胞中的位置为___________ 。
② 晶体的密度为
晶体的密度为 ,则晶胞参数(棱长)为
,则晶胞参数(棱长)为___________ nm(列出计算式,阿伏加德罗常数的值为 )。
)。
(1)Co在元素周期表的位置是
(2)“烧渣”是LiCl、CoCl2和SiO2的混合物。“
 焙烧”反应生成的氧化产物与还原产物的物质的量之比为
焙烧”反应生成的氧化产物与还原产物的物质的量之比为(3)“滤饼2”的主要成分为
 烧结可合成锂电池正极材料LiCoO2,反应的化学方程式为
烧结可合成锂电池正极材料LiCoO2,反应的化学方程式为(4)碳酸锂的溶解度随温度变化如图所示。向滤液2中加入Na2CO3溶液,将温度升至90℃是为了提高沉淀反应速率和
(5)常温下,取
 “滤液2”,其中
“滤液2”,其中 ,为使锂元素的回收率不低于
,为使锂元素的回收率不低于 ,则至少应加入
,则至少应加入 固体的质量为
固体的质量为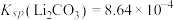 。计算结果保留3位小数。
。计算结果保留3位小数。(6)由
 进一步制得的
进一步制得的 具有反萤石结构,晶胞如图所示。
具有反萤石结构,晶胞如图所示。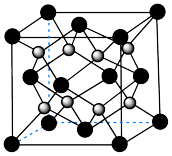
 在晶胞中的位置为
在晶胞中的位置为②
 晶体的密度为
晶体的密度为 ,则晶胞参数(棱长)为
,则晶胞参数(棱长)为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】过渡金属不但能够与非金属元素形成化合物,还能与其他金属元素形成金属互化物。回答下列问题:
(1)Mn在元素周期表中的位置___________ ,属于___________ 区的元素,基态锰原子的价电子轨道表示式为___________ 。
(2)二茂铁化学式为 ,由
,由 与两个
与两个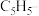 构成(如图),熔点为172℃。
构成(如图),熔点为172℃。___________ 。
②大 键通常用符号
键通常用符号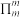 表示(m代表参与形大
表示(m代表参与形大 键的原子数,n代表大
键的原子数,n代表大 键的电子数),则
键的电子数),则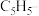 中的大
中的大 键表示为
键表示为___________ 。
③ 与两个
与两个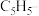 离子形成配位键后,使
离子形成配位键后,使 的3d、4s、4p能级中共具有18电子的稳定结构。则
的3d、4s、4p能级中共具有18电子的稳定结构。则 与两个
与两个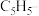 离子形成配位键的数目为
离子形成配位键的数目为___________ 。
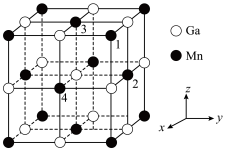
(3)锰和镓形成的金属互化物立方晶胞如图所示。
___________ (填标号)。
A.面心B.体心C.顶点D.棱心
②晶胞中,相邻Mn原子构成的正四面体空隙完全由镍原子填充,可用于制备碳基金属催化剂。1号Mn原子坐标参数为 ,则填充在1、2、3、4号Mn构成的四面体空隙中心的镍原子的坐标参数为
,则填充在1、2、3、4号Mn构成的四面体空隙中心的镍原子的坐标参数为___________ ;晶胞参数为a nm,则填充镍后的晶胞的密度
___________  (用含
(用含 、a的代数式表示)。
、a的代数式表示)。
(1)Mn在元素周期表中的位置
(2)二茂铁化学式为
 ,由
,由 与两个
与两个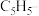 构成(如图),熔点为172℃。
构成(如图),熔点为172℃。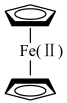
②大
 键通常用符号
键通常用符号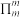 表示(m代表参与形大
表示(m代表参与形大 键的原子数,n代表大
键的原子数,n代表大 键的电子数),则
键的电子数),则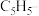 中的大
中的大 键表示为
键表示为③
 与两个
与两个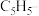 离子形成配位键后,使
离子形成配位键后,使 的3d、4s、4p能级中共具有18电子的稳定结构。则
的3d、4s、4p能级中共具有18电子的稳定结构。则 与两个
与两个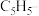 离子形成配位键的数目为
离子形成配位键的数目为(3)锰和镓形成的金属互化物立方晶胞如图所示。
A.面心B.体心C.顶点D.棱心
②晶胞中,相邻Mn原子构成的正四面体空隙完全由镍原子填充,可用于制备碳基金属催化剂。1号Mn原子坐标参数为
 ,则填充在1、2、3、4号Mn构成的四面体空隙中心的镍原子的坐标参数为
,则填充在1、2、3、4号Mn构成的四面体空隙中心的镍原子的坐标参数为
 (用含
(用含 、a的代数式表示)。
、a的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】以 、
、 和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下:
和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下: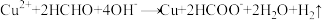
(1)基态Cu原子有___________ 种运动状态不相同的电子;铜—镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。Ni位于___________ 区。
(2)选择HCHO进行化学镀铜的原因之一是它易溶于水。下列分析正确的是___________ (填字母序号)。
a.HCHO、H2O均属于极性分子
b.HCHO与H2O之间能形成氢键
c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的 、HCHO、H2O三种微粒,空间结构为三角形的是
、HCHO、H2O三种微粒,空间结构为三角形的是___________ 。
(4)将过量的氨气通入盛有硫酸铜溶液的试管里,产生的现象为___________ ,写出该过程中沉淀溶解的离子方程式___________ 。
(5)在硅酸盐中,SiO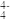 四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根(其中硅原子数为n):其中Si原子的杂化形式为
四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根(其中硅原子数为n):其中Si原子的杂化形式为___________ ,化学式为___________ 。
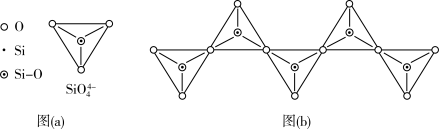
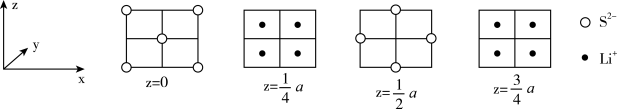
(6)Li2S属立方晶体,晶胞边长为ɑpm,晶胞截面图如下图所示。晶胞中 的配位数是
的配位数是___________ 。阿伏加德罗常数的值用NA表示,则Li2S晶体的密度为___________  (列出计算表达式)。
(列出计算表达式)。
 、
、 和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下:
和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下: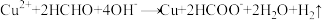
(1)基态Cu原子有
(2)选择HCHO进行化学镀铜的原因之一是它易溶于水。下列分析正确的是
a.HCHO、H2O均属于极性分子
b.HCHO与H2O之间能形成氢键
c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的
 、HCHO、H2O三种微粒,空间结构为三角形的是
、HCHO、H2O三种微粒,空间结构为三角形的是(4)将过量的氨气通入盛有硫酸铜溶液的试管里,产生的现象为
(5)在硅酸盐中,SiO
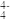 四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根(其中硅原子数为n):其中Si原子的杂化形式为
四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根(其中硅原子数为n):其中Si原子的杂化形式为
(6)Li2S属立方晶体,晶胞边长为ɑpm,晶胞截面图如下图所示。晶胞中
 的配位数是
的配位数是 (列出计算表达式)。
(列出计算表达式)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】镍有广泛的用途,不仅可以用于不锈钢的制造,目前也是三元锂电池中的重要元素。由红土镍矿(主要成分为NiO,还含有少量MgO、SiO2以及铁的氧化物等)可以制取黄钠铁矾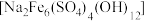 和
和 。
。

(1)黄钠铁矾中Fe的化合价为______ 。
(2)为加快红土镍矿的溶解,在“酸浸”步骤中可以采取的措施是______________________________ (任写2条);滤渣的主要成分是____________ 。
(3)“预处理”中,反应的离子方程式可能为__________________ 。
(4)“沉铁”中若采用Na2CO3作为除铁所需钠源,Na2CO3的用量对体系pH和镍的损失影响如图1所示。当Na2CO3的用量超过6g/L时,镍的损失率会增大,其可能的原因是____________________ (已知Fe3+、Ni2+社开始沉淀的pH分别为2.2、7.5)
(5)若溶液中c(Mg2+)为0.l mol/L,溶液的体积为1L,则要使溶液中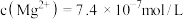 ,则应加入固体NaF为
,则应加入固体NaF为______ mol[忽略体积的变化,已知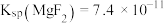 ]。“沉镁”时应保证MgO已将溶液的pH调节至5.5~6.0的原因是
]。“沉镁”时应保证MgO已将溶液的pH调节至5.5~6.0的原因是____________________ 。

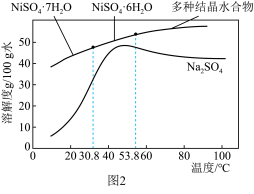
(6)硫酸钠与硫酸镍晶体的溶解度曲线图如图2所示,由滤液Y制备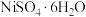 的步骤为:Ⅰ.边搅拌边向滤液Y中滴加NaOH溶液至沉淀完全,过滤﹔Ⅱ.用蒸馏水洗涤固体﹔Ⅲ.将所得固体分批加入足量稀硫酸,搅拌使其完全溶解﹔Ⅳ.稍低于______℃减压蒸发浓缩,降温至稍高于______℃,趁热过滤。
的步骤为:Ⅰ.边搅拌边向滤液Y中滴加NaOH溶液至沉淀完全,过滤﹔Ⅱ.用蒸馏水洗涤固体﹔Ⅲ.将所得固体分批加入足量稀硫酸,搅拌使其完全溶解﹔Ⅳ.稍低于______℃减压蒸发浓缩,降温至稍高于______℃,趁热过滤。
①步骤Ⅱ中确定固体洗涤干净的方法是____________ ;
②步骤Ⅳ中横线上的数字分别是______ 、______ 。
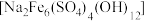 和
和 。
。
(1)黄钠铁矾中Fe的化合价为
(2)为加快红土镍矿的溶解,在“酸浸”步骤中可以采取的措施是
(3)“预处理”中,反应的离子方程式可能为
(4)“沉铁”中若采用Na2CO3作为除铁所需钠源,Na2CO3的用量对体系pH和镍的损失影响如图1所示。当Na2CO3的用量超过6g/L时,镍的损失率会增大,其可能的原因是
(5)若溶液中c(Mg2+)为0.l mol/L,溶液的体积为1L,则要使溶液中
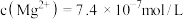 ,则应加入固体NaF为
,则应加入固体NaF为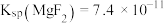 ]。“沉镁”时应保证MgO已将溶液的pH调节至5.5~6.0的原因是
]。“沉镁”时应保证MgO已将溶液的pH调节至5.5~6.0的原因是

(6)硫酸钠与硫酸镍晶体的溶解度曲线图如图2所示,由滤液Y制备
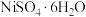 的步骤为:Ⅰ.边搅拌边向滤液Y中滴加NaOH溶液至沉淀完全,过滤﹔Ⅱ.用蒸馏水洗涤固体﹔Ⅲ.将所得固体分批加入足量稀硫酸,搅拌使其完全溶解﹔Ⅳ.稍低于______℃减压蒸发浓缩,降温至稍高于______℃,趁热过滤。
的步骤为:Ⅰ.边搅拌边向滤液Y中滴加NaOH溶液至沉淀完全,过滤﹔Ⅱ.用蒸馏水洗涤固体﹔Ⅲ.将所得固体分批加入足量稀硫酸,搅拌使其完全溶解﹔Ⅳ.稍低于______℃减压蒸发浓缩,降温至稍高于______℃,趁热过滤。①步骤Ⅱ中确定固体洗涤干净的方法是
②步骤Ⅳ中横线上的数字分别是
您最近一年使用:0次
【推荐2】废旧无汞碱性锌锰电池可用于制造隐形战机的机身涂料MnxZn(1-x)Fe2O4,该电池工作反应原理为Zn+2MnO2+2H2O 2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:
2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:
A.浸取:将去除表面塑料的旧电池加入水中浸取并过滤,滤液经操作a得KOH固体;
B.溶液:滤渣中加入过量稀硫酸和足量双氧水,至不再出现气泡时,过滤;
C.测成分:测步骤B中滤液成分,然后加入铁粉;
D.氧化:加入双氧水氧化;
E.调pH:滴加氨水调pH,经结晶处理得MnxZn(1-x)Fe2O4。
(1)浸取时的操作有______ 。
A.拆解、粉碎旧电池 B.降低温度 C.搅拌 D.加压
(2)操作a为________ 。
(3)溶渣时生成Mn2+的主要离子方程式为______________________________ 。
(4)若步骤C测得滤液中金属离子组成为:c(Mn2+) +c(Zn2+) =0.8mol/L, c(Fe2+ ) = 0. 1 mol/L。若滤液体积为lm3,要合成MnxZn(1-x)Fe2O4,需加入Fe粉质量为___________ kg(忽略体积变化)。
(5)氧化时,因为分解所需双氧水的量比理论值大得多。其原因可能是①温度过高;②______ 。
(6)最后一步结晶时,处理不当易生成MnFe2O4和ZnFe2O4。要制得MnxZn(1-x)Fe2O4,最后一步结晶时需注意______________________ 。
(7)某小组构想用ZnSO4、MnSO4溶液为原料,以Fe作电极用电解法经过一系列步骤制得MnxZn(1-x)Fe2O4,则开始电解时阳极反应式为___________________________________ 。
 2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:
2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:A.浸取:将去除表面塑料的旧电池加入水中浸取并过滤,滤液经操作a得KOH固体;
B.溶液:滤渣中加入过量稀硫酸和足量双氧水,至不再出现气泡时,过滤;
C.测成分:测步骤B中滤液成分,然后加入铁粉;
D.氧化:加入双氧水氧化;
E.调pH:滴加氨水调pH,经结晶处理得MnxZn(1-x)Fe2O4。
(1)浸取时的操作有
A.拆解、粉碎旧电池 B.降低温度 C.搅拌 D.加压
(2)操作a为
(3)溶渣时生成Mn2+的主要离子方程式为
(4)若步骤C测得滤液中金属离子组成为:c(Mn2+) +c(Zn2+) =0.8mol/L, c(Fe2+ ) = 0. 1 mol/L。若滤液体积为lm3,要合成MnxZn(1-x)Fe2O4,需加入Fe粉质量为
(5)氧化时,因为分解所需双氧水的量比理论值大得多。其原因可能是①温度过高;②
(6)最后一步结晶时,处理不当易生成MnFe2O4和ZnFe2O4。要制得MnxZn(1-x)Fe2O4,最后一步结晶时需注意
(7)某小组构想用ZnSO4、MnSO4溶液为原料,以Fe作电极用电解法经过一系列步骤制得MnxZn(1-x)Fe2O4,则开始电解时阳极反应式为
您最近一年使用:0次
【推荐3】海洋是资源的宝库,海水中所含食盐高达4×1016t。用海水可生产食盐和金属镁或镁的化合物,其过程如下图所示。

请回答
(1)贝壳主要成分的化学式_________________ ;
(2)步骤④反应的离子方程式____________________________________________ ;
(3)实验室由粗盐结晶制精盐的操作包括溶解、过滤、蒸发等步骤,
A.粗盐提纯过程中过滤的目的是____________ (填序号)
①获得NaCl晶体 ②除去难溶性物质 ③除去易挥发物质 ④除去可溶性物质
B.过滤需要用到的玻璃仪器有玻璃棒______________ 、______________ 。
(4)电解MgCl2制金属Mg的反应方程式为MgCl2 Mg+Cl2↑。电解0.2molMgCl2可生成金属Mg
Mg+Cl2↑。电解0.2molMgCl2可生成金属Mg_______ g,同时可得到氯气__________ L(标准状况)。

请回答
(1)贝壳主要成分的化学式
(2)步骤④反应的离子方程式
(3)实验室由粗盐结晶制精盐的操作包括溶解、过滤、蒸发等步骤,
A.粗盐提纯过程中过滤的目的是
①获得NaCl晶体 ②除去难溶性物质 ③除去易挥发物质 ④除去可溶性物质
B.过滤需要用到的玻璃仪器有玻璃棒
(4)电解MgCl2制金属Mg的反应方程式为MgCl2
 Mg+Cl2↑。电解0.2molMgCl2可生成金属Mg
Mg+Cl2↑。电解0.2molMgCl2可生成金属Mg
您最近一年使用:0次



