二氧化氯( )消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氯常温下为黄绿色或枯黄色气体,以下是二氧化氯的几种工业制备方法。
)消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氯常温下为黄绿色或枯黄色气体,以下是二氧化氯的几种工业制备方法。
(1) 还原法:
还原法: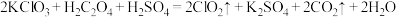 ,请用双线桥表示该反应电子转移的方向和数目
,请用双线桥表示该反应电子转移的方向和数目_______ 。
(2) 还原法:(
还原法:( 和
和 以物质的量之比
以物质的量之比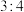 进行反应)
进行反应)
①配平该反应的离子方程式:_______ 。
_______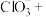 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
②还原产物为_______ 。
(3)盐酸法: ;当
;当 参加反应时,做酸性介质的HCl的物质的量为
参加反应时,做酸性介质的HCl的物质的量为_______ mol。
(4) 自氧化法:
自氧化法: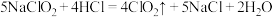 ;该反应中,氧化剂与还原剂的物质的量之比为
;该反应中,氧化剂与还原剂的物质的量之比为_______ ,若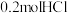 参加反应,则转移的电子数为
参加反应,则转移的电子数为_______ 。
 )消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氯常温下为黄绿色或枯黄色气体,以下是二氧化氯的几种工业制备方法。
)消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氯常温下为黄绿色或枯黄色气体,以下是二氧化氯的几种工业制备方法。(1)
 还原法:
还原法: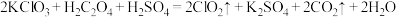 ,请用双线桥表示该反应电子转移的方向和数目
,请用双线桥表示该反应电子转移的方向和数目(2)
 还原法:(
还原法:( 和
和 以物质的量之比
以物质的量之比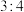 进行反应)
进行反应)①配平该反应的离子方程式:
_______
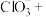 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
②还原产物为
(3)盐酸法:
 ;当
;当 参加反应时,做酸性介质的HCl的物质的量为
参加反应时,做酸性介质的HCl的物质的量为(4)
 自氧化法:
自氧化法: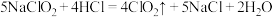 ;该反应中,氧化剂与还原剂的物质的量之比为
;该反应中,氧化剂与还原剂的物质的量之比为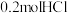 参加反应,则转移的电子数为
参加反应,则转移的电子数为
更新时间:2024-01-21 11:56:10
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】请根据钠及其化合物性质按要求完成各题。
(1)金属钠的密度比水小,在钠与水反应的实验中,能得出“该反应是放热反应”这一结论的实验现象是_______ ,反应的离子方程式是_______ 。
(2)钠的焰色反应的焰色为_______ 色,金属焰色反应是_______ 变化(填“物理”或“化学”)。
(3)写出过氧化钠和二氧化碳反应的化学方程式,并用双线桥表示电子转移方向和数目_______ 。
(1)金属钠的密度比水小,在钠与水反应的实验中,能得出“该反应是放热反应”这一结论的实验现象是
(2)钠的焰色反应的焰色为
(3)写出过氧化钠和二氧化碳反应的化学方程式,并用双线桥表示电子转移方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】I.现有下列物质:
①铁、②硫酸溶液、③ 、④熔融的
、④熔融的 、⑤
、⑤ 固体、⑥蔗糖、⑦
固体、⑥蔗糖、⑦ 晶体、⑧氧气、⑨氨水、⑩稀硝酸。
晶体、⑧氧气、⑨氨水、⑩稀硝酸。
(1)上述物质中属于电解质的有___________ (填编号,下同),属于非电解质的有___________ ,能导电的有___________ 。
(2) 电离方程式为
电离方程式为___________ 。
II.利用氧化还原反应原理可处理污水。
(3)高铁酸钠 是一种新型的净水剂,其中一种制备方法如下:
是一种新型的净水剂,其中一种制备方法如下:
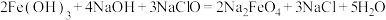 。
。
用单线桥标出该反应电子转移的方向和数目___________ 。
(4)电镀废水中含有剧毒的 (C为
(C为 价),加入
价),加入 溶液处理该碱性废水时生成
溶液处理该碱性废水时生成 、
、 和
和 。该反应的离子方程式为
。该反应的离子方程式为___________ 。
①铁、②硫酸溶液、③
 、④熔融的
、④熔融的 、⑤
、⑤ 固体、⑥蔗糖、⑦
固体、⑥蔗糖、⑦ 晶体、⑧氧气、⑨氨水、⑩稀硝酸。
晶体、⑧氧气、⑨氨水、⑩稀硝酸。(1)上述物质中属于电解质的有
(2)
 电离方程式为
电离方程式为II.利用氧化还原反应原理可处理污水。
(3)高铁酸钠
 是一种新型的净水剂,其中一种制备方法如下:
是一种新型的净水剂,其中一种制备方法如下: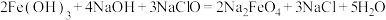 。
。用单线桥标出该反应电子转移的方向和数目
(4)电镀废水中含有剧毒的
 (C为
(C为 价),加入
价),加入 溶液处理该碱性废水时生成
溶液处理该碱性废水时生成 、
、 和
和 。该反应的离子方程式为
。该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。
试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________ (填序号)。
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________ (填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,请写出反应的离子方程式:____
(4)Fe与过量稀硫酸反应可以制取FeSO4。若将反应所得的酸性溶液中Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________ (填序号)。
A.Cl2 B.Fe
C.H2O2 D.HNO2
试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,请写出反应的离子方程式:
(4)Fe与过量稀硫酸反应可以制取FeSO4。若将反应所得的酸性溶液中Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
A.Cl2 B.Fe
C.H2O2 D.HNO2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个发生还原过程的反应式:NO3-+4H++3e-→NO↑+2H2O和发生氧化过程KI→I2(未配平),向KI 溶液中滴加少量稀硝酸能使上述氧化还原过程发生。
①写出并配平该氧化还原反应的方程式:_________________________ 。
②上述反应中被还原的元素是________________ ,还原剂是 ___________ 。
③反应生成0.3molH2O,则转移电子的物质的量为______________ mol。
(2)请配平下面化学方程式。
____ CH3CH2OH+____KMnO4—____CH3CHO+____MnO2+____KOH+____H2O。
(3)用酸性KMnO4溶液处理Cu2S 和CuS 的混合物时,发生的反应如下:
① MnO4-+Cu2S+H+→Cu2++SO2↑+Mn2++ H2O(未配平)
② MnO4-+CuS+H+→Cu2++SO2↑+Mn2++ H2O(未配平)
下列关于反应①的说法中错误的是___________ (填序号)。
A.被氧化的元素是Cu和S
B.氧化剂与还原剂的物质的量之比为8∶5
C.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
D.还原性的强弱关系是:Mn2+>Cu2S
(4)已知:2KMnO4+5H2O2+ 3H2SO4===K2SO4+2MnSO4+5O2↑+8H2O,则被1mol KMnO4 氧化的H2O2 是____ mol。
①写出并配平该氧化还原反应的方程式:
②上述反应中被还原的元素是
③反应生成0.3molH2O,则转移电子的物质的量为
(2)请配平下面化学方程式。
(3)用酸性KMnO4溶液处理Cu2S 和CuS 的混合物时,发生的反应如下:
① MnO4-+Cu2S+H+→Cu2++SO2↑+Mn2++ H2O(未配平)
② MnO4-+CuS+H+→Cu2++SO2↑+Mn2++ H2O(未配平)
下列关于反应①的说法中错误的是
A.被氧化的元素是Cu和S
B.氧化剂与还原剂的物质的量之比为8∶5
C.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
D.还原性的强弱关系是:Mn2+>Cu2S
(4)已知:2KMnO4+5H2O2+ 3H2SO4===K2SO4+2MnSO4+5O2↑+8H2O,则被1mol KMnO4 氧化的H2O2 是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求完成下列方程式
(1)用一种碱性氧化物和一种酸制备MgCl2,写出该制备反应的化学方程式___________ 。
(2)常温下以Fe、CuO、H2SO4三种物质为原料制备Cu的离子方程式___________ ,___________ 。
(3)用稀硫酸清洗青铜器表面的铜绿[Cu2(OH)2CO3],写出涉及的离子方程式___________ 。
(4)高温下铝粉与氧化铁的反应可用来焊接钢轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。该反应的化学方程式为___________ 。
(5)工业废水中含有的Cr2O 有毒,必须处理达标后才能排放。工业上常用FeSO4·7H2O做处理剂将Cr2O
有毒,必须处理达标后才能排放。工业上常用FeSO4·7H2O做处理剂将Cr2O 还原为Cr3+,反应的离子方程式为
还原为Cr3+,反应的离子方程式为___________ 。
(6)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上通过碱性环境中次氯酸钠氧化三氯化铁制备高铁酸钠,制备过程的离子方程式为___________ 。
(1)用一种碱性氧化物和一种酸制备MgCl2,写出该制备反应的化学方程式
(2)常温下以Fe、CuO、H2SO4三种物质为原料制备Cu的离子方程式
(3)用稀硫酸清洗青铜器表面的铜绿[Cu2(OH)2CO3],写出涉及的离子方程式
(4)高温下铝粉与氧化铁的反应可用来焊接钢轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。该反应的化学方程式为
(5)工业废水中含有的Cr2O
 有毒,必须处理达标后才能排放。工业上常用FeSO4·7H2O做处理剂将Cr2O
有毒,必须处理达标后才能排放。工业上常用FeSO4·7H2O做处理剂将Cr2O 还原为Cr3+,反应的离子方程式为
还原为Cr3+,反应的离子方程式为(6)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上通过碱性环境中次氯酸钠氧化三氯化铁制备高铁酸钠,制备过程的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氯酸钾和浓盐酸之间有下列反应:2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2+2H2O
(1)该反应中发生还原反应的物质是___________ 。氧化产物是___________ 。
(2)用双线桥标出方程式中的电子得失。2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2+2H2O,___________
(3)当有0.2mol电子发生转移时,生成的氯气的体积为___________ L(标准状况)。被氧化的HCl的物质的量为___________ mol。
(4)若分别用①KMnO4(还原产物是Mn2+);②MnO2(还原产物是Mn2+);③Ca(ClO)2(还原产物是Cl2)氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是___________ (填编号)。
(5)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个配平 的化学方程式:___________+___________+H2SO4→___________+___________+___________(填化学式),___________
(1)该反应中发生还原反应的物质是
(2)用双线桥标出方程式中的电子得失。2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2+2H2O,
(3)当有0.2mol电子发生转移时,生成的氯气的体积为
(4)若分别用①KMnO4(还原产物是Mn2+);②MnO2(还原产物是Mn2+);③Ca(ClO)2(还原产物是Cl2)氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是
(5)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个
您最近一年使用:0次
【推荐2】我国城市为了减少燃煤造成的大气污染,对于作民用燃料的煤进行了多方面的改进。
(1)为了除去煤中的含硫化合物,采用FeCl3脱硫,即用FeCl3溶液浸洗煤粉,发生如下反应:FeS2+14FeCl3+8H2O=2FeSO4+13FeCl2+16HCl。
①该反应中的氧化剂是________ ,若有1 mol FeS2被除去,则发生转移的电子的物质的量是________ 。
②为了充分利用Fe2+并减少酸(HCl)污染,本方法中可利用工业废铁屑和氯气让废液重新利用生成FeCl3。请写出这一过程中有关的离子方程式:_____________ 。
(2)另一种方法是采用“固硫法”,即在燃料中加入生石灰,使含硫煤在燃烧时生成的SO2不能逸出而进入炉渣中,试用化学方程式表示这一“固硫”过程:_______ 、________ 。
(3)某城市采用了以油制气代替煤作民用燃料的做法。油制气的主要成分是丙烷,请写出其燃烧的化学方程式:_____________ 。
(4)绿色能源是人类的理想能源,不会造成环境污染,下列能源属于绿色能源的是________ 。
A 氢能源 B 太阳能 C 风能 D 石油
(1)为了除去煤中的含硫化合物,采用FeCl3脱硫,即用FeCl3溶液浸洗煤粉,发生如下反应:FeS2+14FeCl3+8H2O=2FeSO4+13FeCl2+16HCl。
①该反应中的氧化剂是
②为了充分利用Fe2+并减少酸(HCl)污染,本方法中可利用工业废铁屑和氯气让废液重新利用生成FeCl3。请写出这一过程中有关的离子方程式:
(2)另一种方法是采用“固硫法”,即在燃料中加入生石灰,使含硫煤在燃烧时生成的SO2不能逸出而进入炉渣中,试用化学方程式表示这一“固硫”过程:
(3)某城市采用了以油制气代替煤作民用燃料的做法。油制气的主要成分是丙烷,请写出其燃烧的化学方程式:
(4)绿色能源是人类的理想能源,不会造成环境污染,下列能源属于绿色能源的是
A 氢能源 B 太阳能 C 风能 D 石油
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式: NO3-+4H++3e- →NO↑+2H2O
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:________________________________ 。
(2)反应中氧化剂和还原剂的物质的量之比是___________ 。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是_________ mol。
(4)若该反应生成一种化合价更高的还原产物,其他物质保持不变,则反应物中氧化剂与还原剂的物质的量之比将_______ (填增大、减小、不变或者不能确定)。
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中氧化剂和还原剂的物质的量之比是
(3)反应中若产生0.2mol气体,则转移电子的物质的量是
(4)若该反应生成一种化合价更高的还原产物,其他物质保持不变,则反应物中氧化剂与还原剂的物质的量之比将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按照要求回答问题。
(1) 的电子式为
的电子式为_______ ,写出其用于呼吸面具做供氧剂的化学方程式:_______ 。
(2)实验室用NaOH浓溶液配制0.1 mol·L NaOH溶液500 mL,需量取密度为1.4 g·cm
NaOH溶液500 mL,需量取密度为1.4 g·cm 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液_______ mL(保留一位小数),该实验所需的玻璃仪器除玻璃棒、量筒、胶头滴管、烧杯之外,还有_______ 。
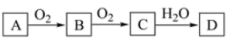
(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的 ,则C→D的化学方程式:
,则C→D的化学方程式:_______ 。
(4)盛放NaOH溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示):_______ 。
(5)高铁酸钠( )是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用
)是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用 的反应原理来制备高铁酸钠,若制备1 mol
的反应原理来制备高铁酸钠,若制备1 mol  ,则该反应转移的电子为
,则该反应转移的电子为_______ mol。
(1)
 的电子式为
的电子式为(2)实验室用NaOH浓溶液配制0.1 mol·L
 NaOH溶液500 mL,需量取密度为1.4 g·cm
NaOH溶液500 mL,需量取密度为1.4 g·cm 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的
 ,则C→D的化学方程式:
,则C→D的化学方程式:
(4)盛放NaOH溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示):
(5)高铁酸钠(
 )是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用
)是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用 的反应原理来制备高铁酸钠,若制备1 mol
的反应原理来制备高铁酸钠,若制备1 mol  ,则该反应转移的电子为
,则该反应转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: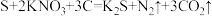 。该反应中,被还原的元素是
。该反应中,被还原的元素是_______ (元素符号)。
(2)饮用水中的NO 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,其化学方程式为:10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2 H2O。请回答下列问题:
还原为N2,其化学方程式为:10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2 H2O。请回答下列问题:
①上述反应中,被氧化的元素_______ ,还原产物是_______ 。
②用双线桥法表示上述反应中电子转移的方向和数目:_______ 。
(3) 是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:
是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:

①高铁酸钾( )属于
)属于_______ (“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为_______ 价。
②过程a中 体现
体现_______ (填“氧化“或“还原”)性,反应过程中消耗1个 转移电子数
转移电子数_______ 。
(4)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体Cl2。请将方程式补充完整:_______ 。
_______NaClO+_______HCl(浓) =_______NaCl+_______Cl2↑+_______H2O
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
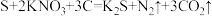 。该反应中,被还原的元素是
。该反应中,被还原的元素是(2)饮用水中的NO
 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,其化学方程式为:10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2 H2O。请回答下列问题:
还原为N2,其化学方程式为:10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2 H2O。请回答下列问题:①上述反应中,被氧化的元素
②用双线桥法表示上述反应中电子转移的方向和数目:
(3)
 是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:
是高效、绿色的水处理剂,其原理如图所示。请回答下列问题:
①高铁酸钾(
 )属于
)属于②过程a中
 体现
体现 转移电子数
转移电子数(4)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体Cl2。请将方程式补充完整:
_______NaClO+_______HCl(浓) =_______NaCl+_______Cl2↑+_______H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)147 g H2SO4的物质的量是________ ;0.5 mol H2SO4的质量是________ g;
(2)氧化铜在高温下发生分解反应:4CuO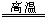 2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为
2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为____________ mol。
(3)反应:2FeCl3+2KI=2FeCl2+2KCl+I2,其中_____ 元素化合价升高,则该元素被_______ ,_____ 元素化合价降低;__________ 做还原剂,_______ 发生还原反应。
(4)钠在空气中燃烧的化学方程式:________________________________ ,1mol钠完全燃烧转移电子的个数为____________ 。
(2)氧化铜在高温下发生分解反应:4CuO
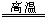 2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为
2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为(3)反应:2FeCl3+2KI=2FeCl2+2KCl+I2,其中
(4)钠在空气中燃烧的化学方程式:
您最近一年使用:0次



