常温下,下列有关电解质溶液的叙述正确的是
A.0.1mol·L-1CuSO4·(NH4)2SO4·6H2O的溶液中: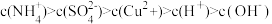 |
B.在 溶液中 溶液中 |
C.0.1mol/LNa2CO3溶液中: |
D.0.1mol·L-1的NaHA溶液,其pH=4: |
更新时间:2024-01-22 15:35:23
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确 的是
A.钢铁发生电化学腐蚀的负极反应: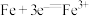 |
B.常温下 通入 通入 溶液,当溶液中约 溶液,当溶液中约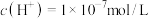 ,一定存在 ,一定存在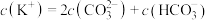 |
C.向 稀溶液中加入 稀溶液中加入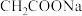 固体,则 固体,则 的值变小 的值变小 |
D.向 溶液中滴加少量 溶液中滴加少量 溶液,产生黑色沉淀, 溶液,产生黑色沉淀, 水解程度增大 水解程度增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】室温下,通过实验探究亚硫酸盐的性质。已知: 、
、 。下列说法正确的是
。下列说法正确的是
 、
、 。下列说法正确的是
。下列说法正确的是| 实验 | 实验操作和现象 |
| 1 | 向10mL1.0mol/LNaOH溶液通入 至溶液pH=7 至溶液pH=7 |
| 2 | 将等体积、等物质的量浓度的 和 和 溶液混合,无明显现象 溶液混合,无明显现象 |
| 3 | 向10mL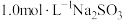 溶液中,逐滴加入等体积等浓度盐酸最终溶液pH<7 溶液中,逐滴加入等体积等浓度盐酸最终溶液pH<7 |
| 4 | 向10mL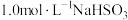 溶液中逐滴滴加15mL1.0mol/LNaOH溶液后测得pH>7 溶液中逐滴滴加15mL1.0mol/LNaOH溶液后测得pH>7 |
A.实验1得到的溶液中: |
B.实验2混合后的溶液中存在: |
C.实验3所得溶液中: |
| D.实验4反应过程中水的电离程度逐渐减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】室温下,Ka1(H2SO3)=10-1.81,Ka1(H2SO3)=10-6.99。室温下通过下列实验探究Na2SO3、NaHSO3溶液的性质。
实验1:测定某浓度的NaHSO3溶液的pH,测得pH为5.2。
实验2:向0.10mol·L-1NaHSO3溶液中加氨水至pH=7。
实验3:向0.10mol·L-1Na2SO3溶液中滴几滴0.10mol·L-1FeCl3溶液,再滴加KSCN溶液,溶液不变红。
实验4:向0.10mol·L-1Na2SO3溶液中加入BaO2固体,有气体产生,同时有白色沉淀。
下列说法错误的是
实验1:测定某浓度的NaHSO3溶液的pH,测得pH为5.2。
实验2:向0.10mol·L-1NaHSO3溶液中加氨水至pH=7。
实验3:向0.10mol·L-1Na2SO3溶液中滴几滴0.10mol·L-1FeCl3溶液,再滴加KSCN溶液,溶液不变红。
实验4:向0.10mol·L-1Na2SO3溶液中加入BaO2固体,有气体产生,同时有白色沉淀。
下列说法错误的是
A.实验1的溶液中: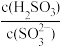 =10-1.6 =10-1.6 |
B.实验2得到的溶液中有 |
C.实验3中加FeCl3溶液的离子方程式为: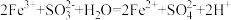 |
D.实验4的上层清液中有c(SO )•c(Ba2+)=Ksp(BaSO3),产生的气体中一定有SO2 )•c(Ba2+)=Ksp(BaSO3),产生的气体中一定有SO2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,在25mL0.1mol/LNaOH 溶液中逐滴加入0.2mol/LCH3COOH 溶液,下图曲线所示的有关粒子浓度关系错误的是


| A.任一点一定都有c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| B.B点:a=12.5,c(Na+ ) =c(CH3COO-)>c(OH-)= c(H+) |
| C.C点:c(CH3COO-)+ c(CH3COOH)=2 c(Na+ )=0.1mol/L |
| D.C点:c(CH3COO-):c(CH3COOH))=3:2,则CH3COOH的Ka=1.5×10-5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列说法中正确的是
①NaHCO3溶液加水稀释时,c(Na+)/c(HCO3-)将增大;
②浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混溶液:2c(Na+)=3[c(CO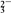 )+c(HCO
)+c(HCO )];
)];
③在0.1 mol·L—1氨水中滴加0.1 mol·L-1盐酸,恰好完全中和时pH=a,则由水电离产生的c(OH-)=10-amol·L-1;
④已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2Cr2O4的溶解度小于AgCl
①NaHCO3溶液加水稀释时,c(Na+)/c(HCO3-)将增大;
②浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混溶液:2c(Na+)=3[c(CO
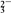 )+c(HCO
)+c(HCO )];
)];③在0.1 mol·L—1氨水中滴加0.1 mol·L-1盐酸,恰好完全中和时pH=a,则由水电离产生的c(OH-)=10-amol·L-1;
④已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2Cr2O4的溶解度小于AgCl
| A.①② | B.②④ | C.①③ | D.③④ |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】室温下,Ka1(H2SO3)=10-1.81,Ka1(H2SO3)=10-6.99。室温下通过下列实验探究Na2SO3、NaHSO3溶液的性质。
实验1:测定某浓度的NaHSO3溶液的pH,测得pH为5.2。
实验2:向0.10mol·L-1NaHSO3溶液中加氨水至pH=7。
实验3:向0.10mol·L-1Na2SO3溶液中滴几滴0.10mol·L-1FeCl3溶液,再滴加KSCN溶液,溶液不变红。
实验4:向0.10mol·L-1Na2SO3溶液中加入BaO2固体,有气体产生,同时有白色沉淀。
下列说法错误的是
实验1:测定某浓度的NaHSO3溶液的pH,测得pH为5.2。
实验2:向0.10mol·L-1NaHSO3溶液中加氨水至pH=7。
实验3:向0.10mol·L-1Na2SO3溶液中滴几滴0.10mol·L-1FeCl3溶液,再滴加KSCN溶液,溶液不变红。
实验4:向0.10mol·L-1Na2SO3溶液中加入BaO2固体,有气体产生,同时有白色沉淀。
下列说法错误的是
A.实验1的溶液中: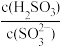 =10-1.6 =10-1.6 |
B.实验2得到的溶液中有 |
C.实验3中加FeCl3溶液的离子方程式为: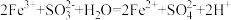 |
D.实验4的上层清液中有c(SO )•c(Ba2+)=Ksp(BaSO3),产生的气体中一定有SO2 )•c(Ba2+)=Ksp(BaSO3),产生的气体中一定有SO2 |
您最近一年使用:0次



