亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO和Cl2反应得到,化学方程式为2NO(g)+Cl2(g)⇌2NOCl(g)。
(1)在1L恒容密闭容器中充入2molNO(g)和1molCl2(g),在不同温度下测得c(NOCl)与时间t的关系如图A所示:___________ mol·L-1·min-1。
②T2时该反应的平衡常数K=___________ 。
③T2时Cl2的平衡转化率为___________ 。
(2)若按投料比n(NO)∶n(Cl2)=2∶1把NO和Cl2加入一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图B所示:___________ (填“>”“<”或“=”)0。
②在p压强条件下,M点时容器内NO的体积分数为___________ 。
③若反应一直保持在p压强条件下进行,则M点的压强平衡常数Kp=___________ (用含p的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
(1)在1L恒容密闭容器中充入2molNO(g)和1molCl2(g),在不同温度下测得c(NOCl)与时间t的关系如图A所示:
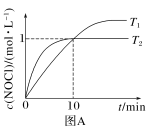
②T2时该反应的平衡常数K=
③T2时Cl2的平衡转化率为
(2)若按投料比n(NO)∶n(Cl2)=2∶1把NO和Cl2加入一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图B所示:
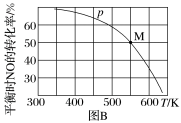
②在p压强条件下,M点时容器内NO的体积分数为
③若反应一直保持在p压强条件下进行,则M点的压强平衡常数Kp=
23-24高三上·河南周口·阶段练习 查看更多[2]
更新时间:2024-01-22 13:33:36
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】工业生产硫酸时,利用催化氧化反应将 转化为
转化为 是一个关键步骤。压强及温度对
是一个关键步骤。压强及温度对 转化率的影响如下表(原料气各成分的体积分数为:
转化率的影响如下表(原料气各成分的体积分数为: 7%,
7%, 11%,
11%, 82%):
82%):
(1)已知 的氧化是放热反应,如何利用表中数据推断此结论?
的氧化是放热反应,如何利用表中数据推断此结论?___________ ;
(2)在400℃~500℃时, 的催化氧化采用常压而不是高压,主要原因是:
的催化氧化采用常压而不是高压,主要原因是:___________ ;
(3)选择适宜的催化剂,是否可以提高 的平衡转化率?
的平衡转化率?___________ (填“是”或“否”),是否可以增大该反应所放出的热量?___________ (填“是”或“否”);
(4)在 催化氧化设备中设置热交器的目的是
催化氧化设备中设置热交器的目的是___________ 、___________ ,从而充分利用能源。
(5)为提高 吸收率,实际生产中用
吸收率,实际生产中用___________ 吸收 ;尾气中
;尾气中 必须回收,主要是为了
必须回收,主要是为了___________ 。
(6)研究表明, 催化氧化的反应速率方程为:
催化氧化的反应速率方程为: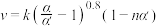 式中:k为反应速率常数,随温度t升高而增大;
式中:k为反应速率常数,随温度t升高而增大; 为
为 平衡转化率,
平衡转化率,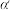 为某时刻
为某时刻 转化率,n为常数。在
转化率,n为常数。在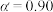 时,将一系列温度下的k、
时,将一系列温度下的k、 值代入上述速率方程,得到
值代入上述速率方程,得到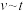 曲线,如下图所示。
曲线,如下图所示。
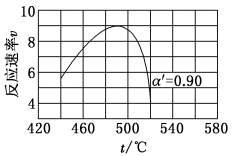
线上v最大值所对应温度称为该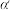 下反应的最适宜温度
下反应的最适宜温度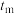 。
。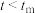 时,v逐渐提高:
时,v逐渐提高: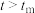 后,v逐渐下降。原因是
后,v逐渐下降。原因是___________ 。
 转化为
转化为 是一个关键步骤。压强及温度对
是一个关键步骤。压强及温度对 转化率的影响如下表(原料气各成分的体积分数为:
转化率的影响如下表(原料气各成分的体积分数为: 7%,
7%, 11%,
11%, 82%):
82%):| 压强/Mpa 转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
 的氧化是放热反应,如何利用表中数据推断此结论?
的氧化是放热反应,如何利用表中数据推断此结论?(2)在400℃~500℃时,
 的催化氧化采用常压而不是高压,主要原因是:
的催化氧化采用常压而不是高压,主要原因是:(3)选择适宜的催化剂,是否可以提高
 的平衡转化率?
的平衡转化率?(4)在
 催化氧化设备中设置热交器的目的是
催化氧化设备中设置热交器的目的是(5)为提高
 吸收率,实际生产中用
吸收率,实际生产中用 ;尾气中
;尾气中 必须回收,主要是为了
必须回收,主要是为了(6)研究表明,
 催化氧化的反应速率方程为:
催化氧化的反应速率方程为: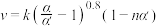 式中:k为反应速率常数,随温度t升高而增大;
式中:k为反应速率常数,随温度t升高而增大; 为
为 平衡转化率,
平衡转化率,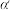 为某时刻
为某时刻 转化率,n为常数。在
转化率,n为常数。在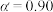 时,将一系列温度下的k、
时,将一系列温度下的k、 值代入上述速率方程,得到
值代入上述速率方程,得到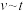 曲线,如下图所示。
曲线,如下图所示。
线上v最大值所对应温度称为该
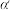 下反应的最适宜温度
下反应的最适宜温度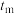 。
。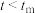 时,v逐渐提高:
时,v逐渐提高: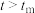 后,v逐渐下降。原因是
后,v逐渐下降。原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】盖斯定律是人们研究热化学的重要工具和方法。
(1)已知1molSi固体中有2molSi-Si键,1molO2中有1molO=O键,1molSiO2固体中有4molSi-O键。某些化学键键能(1mol化学键断裂需要吸收的能量)数据如下:
根据化学键数据写出Si(s)在O2中完全燃烧生成SiO2的热化学方式:___________ 。
(2)N2H4和H2O2混合可作火箭推进剂,已知:16g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出267kJ的热量;2H2O2(l)=O2(g)+2H2O(l) ΔH=-196.4kJ·mol-1。液态N2H4和液态H2O2反应生成N2(g)和H2O(l)的热化学方程式为___________ 。
(3)煤加工的重要手段是煤的气化,如用煤合成水煤气的原理为C(s)+H2O(g) CO(g)+H2(g) ΔH。
CO(g)+H2(g) ΔH。
已知:C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
H2(g)+ O2(g)=H2O(g) ΔH=-242.0kJ/mol
O2(g)=H2O(g) ΔH=-242.0kJ/mol
CO(g)+ O2(g)=CO2(g) ΔH=-283.0kJ/mol
O2(g)=CO2(g) ΔH=-283.0kJ/mol
求:①6gC(s)完全燃烧放出的热量为___________ kJ。
②C(s)+H2O(g)=CO(g)+H2(g)ΔH=___________ 。
(4)工业上可用CO2来生产燃料甲醇。在容积为2L的密闭容器中充入0.8molCO2和2.4molH2。在500℃下发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如图所示:
CH3OH(g)+H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如图所示:

从反应开始到平衡,用氢气表示的平均反应速率v(H2)=___________ 。
(1)已知1molSi固体中有2molSi-Si键,1molO2中有1molO=O键,1molSiO2固体中有4molSi-O键。某些化学键键能(1mol化学键断裂需要吸收的能量)数据如下:
| 化学键 | Si-O | Si-Si | O=O |
| 键能(kJ·mol-1) | 460 | 176 | 498 |
(2)N2H4和H2O2混合可作火箭推进剂,已知:16g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出267kJ的热量;2H2O2(l)=O2(g)+2H2O(l) ΔH=-196.4kJ·mol-1。液态N2H4和液态H2O2反应生成N2(g)和H2O(l)的热化学方程式为
(3)煤加工的重要手段是煤的气化,如用煤合成水煤气的原理为C(s)+H2O(g)
 CO(g)+H2(g) ΔH。
CO(g)+H2(g) ΔH。已知:C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
H2(g)+
 O2(g)=H2O(g) ΔH=-242.0kJ/mol
O2(g)=H2O(g) ΔH=-242.0kJ/molCO(g)+
 O2(g)=CO2(g) ΔH=-283.0kJ/mol
O2(g)=CO2(g) ΔH=-283.0kJ/mol求:①6gC(s)完全燃烧放出的热量为
②C(s)+H2O(g)=CO(g)+H2(g)ΔH=
(4)工业上可用CO2来生产燃料甲醇。在容积为2L的密闭容器中充入0.8molCO2和2.4molH2。在500℃下发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如图所示:
CH3OH(g)+H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如图所示:
从反应开始到平衡,用氢气表示的平均反应速率v(H2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为2L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)前10min, (CO2)=
(CO2)=____ mol·L-1·min-1。
(2)能说明上述反应达到平衡状态的是____ (填字母)。
a.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
b.混合气体的压强不随时间的变化而变化
c.单位时间内生成1molH2O,同时生成1molCH3OH
d.混合气体的平均相对分子质量不随时间的变化而变化
e.混合气体的密度不随时间的变化而变化
f.CO2和CH3OH的反应速率之比为1∶1
(3)反应前与平衡时的压强比为____ 。
(4)平衡混合气体中CO2(g)和H2(g)的质量之比是____ 。
(5)平衡时H2的转化率为____ 。

(1)前10min,
 (CO2)=
(CO2)=(2)能说明上述反应达到平衡状态的是
a.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
b.混合气体的压强不随时间的变化而变化
c.单位时间内生成1molH2O,同时生成1molCH3OH
d.混合气体的平均相对分子质量不随时间的变化而变化
e.混合气体的密度不随时间的变化而变化
f.CO2和CH3OH的反应速率之比为1∶1
(3)反应前与平衡时的压强比为
(4)平衡混合气体中CO2(g)和H2(g)的质量之比是
(5)平衡时H2的转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
I.CO(g)+H2O(g) CO2(g)+H2(g)△H1=−41.0kJ/mol
CO2(g)+H2(g)△H1=−41.0kJ/mol
II.CO(g)+2H2(g) CH3OH(g)△H2=−90.0kJ/mol
CH3OH(g)△H2=−90.0kJ/mol
III.CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3
回答下列问题:
(1)则△H3=___ ,在以上制备甲醇的两个反应中,反应Ⅱ优于反应Ⅲ,其原因是___ 。
(2)一定比例的合成气在装有催化剂的反应器中反应12小时,体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。

当温度为470K时,图中P点___ (填“是“或“不是”)处于平衡状态。490K之后。甲醇产率下降的原因是___ 。
(3)图2为一定比例的CO2和H2,CO和H2,CO2、CO和H2三组混合气体在一定条件下反应时甲醇生成速率与温度的关系。
①490K时,根据曲线a、c判断合成甲醇的反应机理是___ (填“A“或“B“)。
A. CO2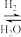 CO
CO CH3OH
CH3OH
B. CO CO2
CO2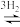 CH3OH+H2O
CH3OH+H2O
②490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,结合反应Ⅰ、Ⅲ分析原因___ 。
③某温度时,在体积为2L的恒容容器中充入1molCO和2molH2,发生反应Ⅱ,若平衡时CO的转化率为50%,其平衡常数为___ ( mol∙L−1) −2。
(4)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的电极反应式为:___ 。
I.CO(g)+H2O(g)
 CO2(g)+H2(g)△H1=−41.0kJ/mol
CO2(g)+H2(g)△H1=−41.0kJ/molII.CO(g)+2H2(g)
 CH3OH(g)△H2=−90.0kJ/mol
CH3OH(g)△H2=−90.0kJ/molIII.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3回答下列问题:
(1)则△H3=
(2)一定比例的合成气在装有催化剂的反应器中反应12小时,体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。

当温度为470K时,图中P点
(3)图2为一定比例的CO2和H2,CO和H2,CO2、CO和H2三组混合气体在一定条件下反应时甲醇生成速率与温度的关系。
①490K时,根据曲线a、c判断合成甲醇的反应机理是
A. CO2
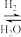 CO
CO CH3OH
CH3OH B. CO
 CO2
CO2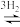 CH3OH+H2O
CH3OH+H2O②490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,结合反应Ⅰ、Ⅲ分析原因
③某温度时,在体积为2L的恒容容器中充入1molCO和2molH2,发生反应Ⅱ,若平衡时CO的转化率为50%,其平衡常数为
(4)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的电极反应式为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】“碳达峰·碳中和”是我国社会发展重大战略之一,以 、
、 为原料合成甲醇是实现“双碳”经济的有效途径之一、回答下列问题:
为原料合成甲醇是实现“双碳”经济的有效途径之一、回答下列问题:
已知:①
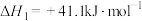
②
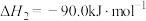
(1)以 、
、 为原料合成甲醇:
为原料合成甲醇: 。
。
①该反应的
___________  。
。
②该反应的活化能 (正)
(正)___________  (逆)(填“>”“<”或“=”)。
(逆)(填“>”“<”或“=”)。
(2)T℃时,向容积为2L的密闭容器中充入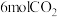 和
和 ,并加入催化剂合成甲醇:
,并加入催化剂合成甲醇: ,容器中
,容器中 的物质的量随时间变化如图中实线所示,图中虚线表示仅改变某一反应条件时,
的物质的量随时间变化如图中实线所示,图中虚线表示仅改变某一反应条件时, 的物质的量随时间的变化。
的物质的量随时间的变化。
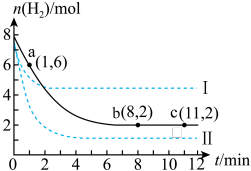
①该反应在0~8min内, 的平均反应速率是
的平均反应速率是___________ 。
②T℃时,该反应的化学平衡常数
___________ 。
③曲线I、Ⅱ改变的条件分别可能是___________ 、___________ 。
(3)在一定温度下的恒容密闭容器中,能说明 达到平衡状态的是
达到平衡状态的是___________ (填字母)。
a.容器中混合气体的密度不再改变
b.容器中的压强不再改变
c. 和
和 的浓度之比为3:1
的浓度之比为3:1
 、
、 为原料合成甲醇是实现“双碳”经济的有效途径之一、回答下列问题:
为原料合成甲醇是实现“双碳”经济的有效途径之一、回答下列问题:已知:①

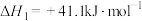
②

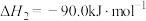
(1)以
 、
、 为原料合成甲醇:
为原料合成甲醇: 。
。①该反应的

 。
。②该反应的活化能
 (正)
(正) (逆)(填“>”“<”或“=”)。
(逆)(填“>”“<”或“=”)。(2)T℃时,向容积为2L的密闭容器中充入
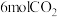 和
和 ,并加入催化剂合成甲醇:
,并加入催化剂合成甲醇: ,容器中
,容器中 的物质的量随时间变化如图中实线所示,图中虚线表示仅改变某一反应条件时,
的物质的量随时间变化如图中实线所示,图中虚线表示仅改变某一反应条件时, 的物质的量随时间的变化。
的物质的量随时间的变化。
①该反应在0~8min内,
 的平均反应速率是
的平均反应速率是②T℃时,该反应的化学平衡常数

③曲线I、Ⅱ改变的条件分别可能是
(3)在一定温度下的恒容密闭容器中,能说明
 达到平衡状态的是
达到平衡状态的是a.容器中混合气体的密度不再改变
b.容器中的压强不再改变
c.
 和
和 的浓度之比为3:1
的浓度之比为3:1
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)⇌CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2 L的密闭容器中加入 4 mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
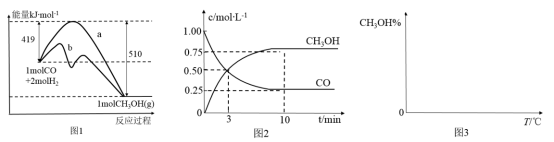
请回答下列问题:
(1)在“图1”中,曲线________ (填“a”或“b”)表示使用了催化剂;该反应属于________ (填“吸热”或“放热”)反应。
(2)下列说法正确的是________ 。
A.起始充入的CO为2 mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1 mol CO和2 mol H2,再次达到平衡n(CH3OH)/n(CO)会减小
(3)从反应开始到建立平衡,v(H2)=________________ ;该温度下CO(g)+2H2(g) CH3OH(g)的化学平衡常数为
CH3OH(g)的化学平衡常数为________ 。若保持其他条件不变,将反应体系升温,则该反应化学平衡常数________ (填“增大”“减小”或“不变”)。
(4)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出p1、p2,且p1<p2)。_____________________
(5)已知CH3OH(g)+3/2O2(g)⇌CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol,又知H2O(l)=H2O(g) ΔH=+44 kJ/mol,请写出32 g的CH3OH(g)完全燃烧生成CO2和液态水的热化学方程式________ 。

请回答下列问题:
(1)在“图1”中,曲线
(2)下列说法正确的是
A.起始充入的CO为2 mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1 mol CO和2 mol H2,再次达到平衡n(CH3OH)/n(CO)会减小
(3)从反应开始到建立平衡,v(H2)=
 CH3OH(g)的化学平衡常数为
CH3OH(g)的化学平衡常数为(4)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出p1、p2,且p1<p2)。
(5)已知CH3OH(g)+3/2O2(g)⇌CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol,又知H2O(l)=H2O(g) ΔH=+44 kJ/mol,请写出32 g的CH3OH(g)完全燃烧生成CO2和液态水的热化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】NH3经一系列反应可以得到HNO3和NH4NO3,如图所示。

(1)Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是______ 。
(2)Ⅱ中,2NO(g)+O2(g) 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线(如图)。

①比较p1、p2的大小关系:_______ 。
②随温度升高,该反应平衡常数变化的趋势是______ 。
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。已知:2NO2(g) N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g) N2O4(l) ΔH2,下列能量变化示意图中,正确的是
N2O4(l) ΔH2,下列能量变化示意图中,正确的是____ (选填字母)。

(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示。

①写出阳极的电极反应式______
②为使电解产物全部转化为NH4NO3,需补充A。A是_____ ,说明理由:____ 。

(1)Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是
(2)Ⅱ中,2NO(g)+O2(g)
 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线(如图)。
①比较p1、p2的大小关系:
②随温度升高,该反应平衡常数变化的趋势是
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。已知:2NO2(g)
 N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g) N2O4(l) ΔH2,下列能量变化示意图中,正确的是
N2O4(l) ΔH2,下列能量变化示意图中,正确的是
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示。

①写出阳极的电极反应式
②为使电解产物全部转化为NH4NO3,需补充A。A是
您最近一年使用:0次
【推荐2】二氧化硫的污染治理是化学家关注的热点问题之一,回答下列问题。
I.二氧化硫的治理。已知25℃时,Kb(NH3·H2O)=1.8×10-5 Ksp(CaSO4)=7.1×10-5 Ka1(H2SO3)=1.5×10-2 Ka2(H2SO3)=1.0×10-7。
(1)亚硫酸盐法。将含二氧化硫的烟气通入1.0mol·L-1的Na2SO3溶液,写出该反应的化学方程式_______ 。若此过程中溶液体积不变,则溶液的pH将_______ (填“减小”“不变”或“增大)。
(2)双碱脱硫法。
第1步:用过量的浓氨水吸收SO2,并在空气中氧化;
第2步:加入石灰水,发生反应Ca2++2OH-+2NH +SO
+SO ⇌CaSO4↓+2NH3·H2O
⇌CaSO4↓+2NH3·H2O
计算第2步反应的K=_______ (填数值,保留2位有效数字)。
(3)电解法。先用Na2SO4溶液吸收烟气中的SO2,再用离子膜电解法电解吸收液得到单质硫,同时在阳极得到副产物氧气,装置如图所示。

①b为电源的_______ (填“正极”或“负极”)。
②用Na2SO4溶液代替水吸收烟气中的SO2,目的是_______ 。
③若电解一段时间后通过质子交换膜的离子数为1.204×1024个,则通过处理烟气理论上能得到硫_______ kg。
II.二氧化硫的转化。
(4)适当调控硫酸工业的反应条件可提高二氧化硫的转化率,减少其排放。已知,对于放热的可逆反应,某一给定转化率下,最大反应速率对应的温度称为最适宜温度。在图中画出反应2SO2(g)+O2(g)⇌2SO3(g)的转化率与最适宜温度(曲线a)、平衡转化率与温度(曲线b)的关系曲线示意图(标明曲线 a 、 b )_______ 。

I.二氧化硫的治理。已知25℃时,Kb(NH3·H2O)=1.8×10-5 Ksp(CaSO4)=7.1×10-5 Ka1(H2SO3)=1.5×10-2 Ka2(H2SO3)=1.0×10-7。
(1)亚硫酸盐法。将含二氧化硫的烟气通入1.0mol·L-1的Na2SO3溶液,写出该反应的化学方程式
(2)双碱脱硫法。
第1步:用过量的浓氨水吸收SO2,并在空气中氧化;
第2步:加入石灰水,发生反应Ca2++2OH-+2NH
 +SO
+SO ⇌CaSO4↓+2NH3·H2O
⇌CaSO4↓+2NH3·H2O计算第2步反应的K=
(3)电解法。先用Na2SO4溶液吸收烟气中的SO2,再用离子膜电解法电解吸收液得到单质硫,同时在阳极得到副产物氧气,装置如图所示。

①b为电源的
②用Na2SO4溶液代替水吸收烟气中的SO2,目的是
③若电解一段时间后通过质子交换膜的离子数为1.204×1024个,则通过处理烟气理论上能得到硫
II.二氧化硫的转化。
(4)适当调控硫酸工业的反应条件可提高二氧化硫的转化率,减少其排放。已知,对于放热的可逆反应,某一给定转化率下,最大反应速率对应的温度称为最适宜温度。在图中画出反应2SO2(g)+O2(g)⇌2SO3(g)的转化率与最适宜温度(曲线a)、平衡转化率与温度(曲线b)的关系曲线示意图(

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
真题
【推荐3】硼酸(H3BO3)在食品、医药领域应用广泛。
(1)请完成B2H6气体与水反应的化学方程式:B2H6+ 6H2O=2H3BO3+__________ 。
(2)在其他条件相同时,反应H3BO3+3CH3OH B(OCH3)3+3H2O中,H3BO3的转化率(
B(OCH3)3+3H2O中,H3BO3的转化率( )在不同温度下随反应时间(t)的变化见图12,由此图可得出:
)在不同温度下随反应时间(t)的变化见图12,由此图可得出:
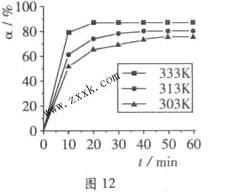
①温度对应该反应的反应速率和平衡移动的影响是_______________________ 。
②该反应的
_____ 0(填“<”、“=”或“>”)。
(3)H3BO3溶液中存在如下反应:H3BO3(aq)+H2O(l) [B(OH)4]-( aq)+H+(aq),已知0.70 mol·L-1H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0 × 10-5mol·L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
[B(OH)4]-( aq)+H+(aq),已知0.70 mol·L-1H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0 × 10-5mol·L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)__________
(1)请完成B2H6气体与水反应的化学方程式:B2H6+ 6H2O=2H3BO3+
(2)在其他条件相同时,反应H3BO3+3CH3OH
 B(OCH3)3+3H2O中,H3BO3的转化率(
B(OCH3)3+3H2O中,H3BO3的转化率( )在不同温度下随反应时间(t)的变化见图12,由此图可得出:
)在不同温度下随反应时间(t)的变化见图12,由此图可得出:
①温度对应该反应的反应速率和平衡移动的影响是
②该反应的

(3)H3BO3溶液中存在如下反应:H3BO3(aq)+H2O(l)
 [B(OH)4]-( aq)+H+(aq),已知0.70 mol·L-1H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0 × 10-5mol·L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
[B(OH)4]-( aq)+H+(aq),已知0.70 mol·L-1H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0 × 10-5mol·L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)在恒温条件下,1 mol NO2和足量C发生反应:2NO2(g)+2C(s) N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
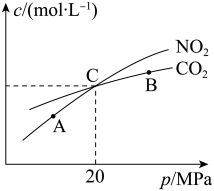
①A B两点的浓度平衡常数关系:Kc(A)___________ Kc(B)(填“<”或“>”或“=”)。
②A B C三点中NO2的转化率最高的是___________ (填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp=___________ (写出计算结果,Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10 mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。
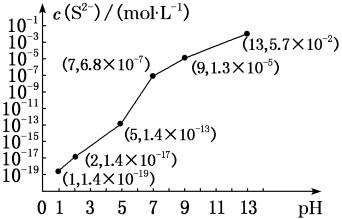
①pH=13时,溶液中的c(H2S)+c(HS-)=___________ mol·L-1;
②某溶液含0.010 mol·L-1Fe2+和0.10 mol·L-1H2S,当溶液pH=___________ 时,Fe2+开始沉淀。【已知:KSP(FeS)=1.4×10-19】
(3)常温下,将pH=a的醋酸溶液与pH=b的NaOH溶液等体积混合后,两者恰好完全反应,则该温度下醋酸的电离平衡常数约为___________ 。
(1)在恒温条件下,1 mol NO2和足量C发生反应:2NO2(g)+2C(s)
 N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
①A B两点的浓度平衡常数关系:Kc(A)
②A B C三点中NO2的转化率最高的是
③计算C点时该反应的压强平衡常数Kp=
(2)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10 mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。

①pH=13时,溶液中的c(H2S)+c(HS-)=
②某溶液含0.010 mol·L-1Fe2+和0.10 mol·L-1H2S,当溶液pH=
(3)常温下,将pH=a的醋酸溶液与pH=b的NaOH溶液等体积混合后,两者恰好完全反应,则该温度下醋酸的电离平衡常数约为
您最近一年使用:0次
【推荐2】一定量的 在恒压密闭容器中发生反应:
在恒压密闭容器中发生反应: 。平衡时,体系中各气体体积分数与温度的关系如图所示:
。平衡时,体系中各气体体积分数与温度的关系如图所示:
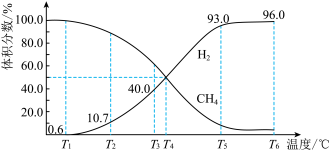
(1).已知甲烷、碳、氢气的燃烧热分别为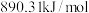 、
、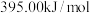 、
、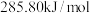 ,则该反应的反应热
,则该反应的反应热
__________ 。
(2).下列能说明反应一定达到平衡状态的是_______ 。
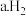 和
和 的体积分数相等
的体积分数相等
 混合气体的平均相对分子质量不变
混合气体的平均相对分子质量不变
 混合气体的密度不变
混合气体的密度不变
 气体总压强不再变化
气体总压强不再变化
 碳的质量不再改变
碳的质量不再改变
(3). 时,若在平衡体系中充入惰性气体,此时反应速率
时,若在平衡体系中充入惰性气体,此时反应速率____  填“变大”、“变小”或“不变”
填“变大”、“变小”或“不变” ,且
,且
_____ 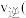 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。
(4).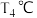 时,若在平衡体系中充入等体积的
时,若在平衡体系中充入等体积的 和
和 ,则平衡
,则平衡_____ 移动,其理由是_______ 。
(5).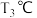 时,反应达平衡后
时,反应达平衡后 的转化率为
的转化率为____________ 。
 在恒压密闭容器中发生反应:
在恒压密闭容器中发生反应: 。平衡时,体系中各气体体积分数与温度的关系如图所示:
。平衡时,体系中各气体体积分数与温度的关系如图所示:
(1).已知甲烷、碳、氢气的燃烧热分别为
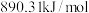 、
、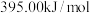 、
、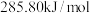 ,则该反应的反应热
,则该反应的反应热
(2).下列能说明反应一定达到平衡状态的是
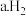 和
和 的体积分数相等
的体积分数相等  混合气体的平均相对分子质量不变
混合气体的平均相对分子质量不变 混合气体的密度不变
混合气体的密度不变  气体总压强不再变化
气体总压强不再变化  碳的质量不再改变
碳的质量不再改变(3).
 时,若在平衡体系中充入惰性气体,此时反应速率
时,若在平衡体系中充入惰性气体,此时反应速率 填“变大”、“变小”或“不变”
填“变大”、“变小”或“不变” ,且
,且
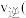 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。(4).
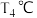 时,若在平衡体系中充入等体积的
时,若在平衡体系中充入等体积的 和
和 ,则平衡
,则平衡(5).
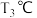 时,反应达平衡后
时,反应达平衡后 的转化率为
的转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】深入研究含碳、氮元素物质的转化有着重要的实际意义。
Ⅰ.合成尿素:如图所示是合成尿素反应的机理及能量变化(单位: ),
), 表示过渡态。
表示过渡态。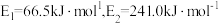 ,则总反应
,则总反应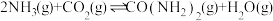

___________  。
。
(2)若向某恒温恒容的密闭容器中加入等物质的量的 和
和 发生上述反应。结合以上机理,下列叙述能说明反应已经达到平衡状态的是
发生上述反应。结合以上机理,下列叙述能说明反应已经达到平衡状态的是___________ (填标号)。
a. 的体积分数不再变化 b.平衡常数K不再变化
的体积分数不再变化 b.平衡常数K不再变化
c. d.断裂
d.断裂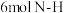 键的同时断裂
键的同时断裂 键
键
(3)图为使用不同催化剂①、②、③时,反应至相同时间,容器中尿素的物质的量随温度变化的曲线,A点___________ (填“是”或“不是”)平衡状态, 以上
以上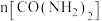 下降的原因可能是
下降的原因可能是___________ (答出一点即可,不考虑物质的稳定性)。 处理大气污染物
处理大气污染物
(4)① 、
、 在催化剂
在催化剂 的表面进行两步反应转化为无毒的气体,第一步为
的表面进行两步反应转化为无毒的气体,第一步为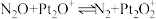 ;则第二步为
;则第二步为___________ 。
②已知: 的速率方程为
的速率方程为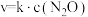 ,k为速率常数,只与温度有关。为提高反应速率,可采取的措施是
,k为速率常数,只与温度有关。为提高反应速率,可采取的措施是___________ (填标号)。
A.升温 B.恒容时,再充入 C.恒容时,再充入
C.恒容时,再充入 D.恒压时,再充入
D.恒压时,再充入
(5)在总压为 的恒容密闭容器中,充入一定量的
的恒容密闭容器中,充入一定量的 和
和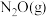 发生上述反应,在不同条件下达到平衡时,温度
发生上述反应,在不同条件下达到平衡时,温度 时
时 的转化率随
的转化率随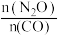 变化的曲线,以及在
变化的曲线,以及在 时
时 的转化率随
的转化率随 变化的曲线如图所示:
变化的曲线如图所示: 的转化率随
的转化率随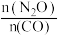 变化的曲线为
变化的曲线为___________ 曲线(填“Ⅰ”或“Ⅱ”);上述反应的
___________ 0(填“>”或“<”)。
②在 时,用平衡分压代替其平衡浓度表示的化学平衡常数
时,用平衡分压代替其平衡浓度表示的化学平衡常数
___________ (结果保留两位小数)[已知:气体分压( )=气体总压(
)=气体总压( )×该气体的物质的量分数]。
)×该气体的物质的量分数]。
Ⅰ.合成尿素:如图所示是合成尿素反应的机理及能量变化(单位:
 ),
), 表示过渡态。
表示过渡态。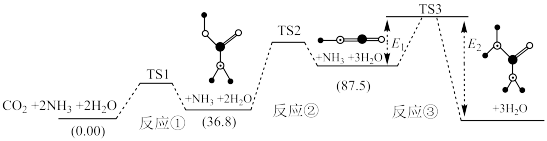
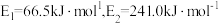 ,则总反应
,则总反应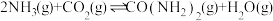

 。
。(2)若向某恒温恒容的密闭容器中加入等物质的量的
 和
和 发生上述反应。结合以上机理,下列叙述能说明反应已经达到平衡状态的是
发生上述反应。结合以上机理,下列叙述能说明反应已经达到平衡状态的是a.
 的体积分数不再变化 b.平衡常数K不再变化
的体积分数不再变化 b.平衡常数K不再变化c.
 d.断裂
d.断裂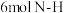 键的同时断裂
键的同时断裂 键
键(3)图为使用不同催化剂①、②、③时,反应至相同时间,容器中尿素的物质的量随温度变化的曲线,A点
 以上
以上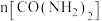 下降的原因可能是
下降的原因可能是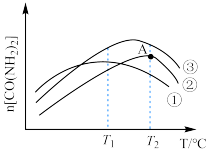
 处理大气污染物
处理大气污染物
(4)①
 、
、 在催化剂
在催化剂 的表面进行两步反应转化为无毒的气体,第一步为
的表面进行两步反应转化为无毒的气体,第一步为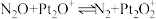 ;则第二步为
;则第二步为②已知:
 的速率方程为
的速率方程为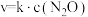 ,k为速率常数,只与温度有关。为提高反应速率,可采取的措施是
,k为速率常数,只与温度有关。为提高反应速率,可采取的措施是A.升温 B.恒容时,再充入
 C.恒容时,再充入
C.恒容时,再充入 D.恒压时,再充入
D.恒压时,再充入
(5)在总压为
 的恒容密闭容器中,充入一定量的
的恒容密闭容器中,充入一定量的 和
和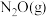 发生上述反应,在不同条件下达到平衡时,温度
发生上述反应,在不同条件下达到平衡时,温度 时
时 的转化率随
的转化率随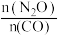 变化的曲线,以及在
变化的曲线,以及在 时
时 的转化率随
的转化率随 变化的曲线如图所示:
变化的曲线如图所示: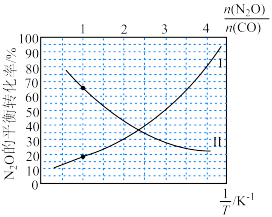
 的转化率随
的转化率随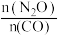 变化的曲线为
变化的曲线为
②在
 时,用平衡分压代替其平衡浓度表示的化学平衡常数
时,用平衡分压代替其平衡浓度表示的化学平衡常数
 )=气体总压(
)=气体总压( )×该气体的物质的量分数]。
)×该气体的物质的量分数]。
您最近一年使用:0次



