常压下羰基化法精炼镍的原理为:
 平衡常数
平衡常数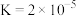 ,制备过程如下。
,制备过程如下。

已知: 的沸点为42.2℃,固体杂质不参与反应。
的沸点为42.2℃,固体杂质不参与反应。
下列判断正确的是

 平衡常数
平衡常数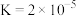 ,制备过程如下。
,制备过程如下。
已知:
 的沸点为42.2℃,固体杂质不参与反应。
的沸点为42.2℃,固体杂质不参与反应。下列判断正确的是
| A.及时分离出Ni,有利于平衡逆向移动,得到更多的高纯镍 |
B.其他条件不变,增加 ,平衡向正向移动,反应的平衡常数K增大 ,平衡向正向移动,反应的平衡常数K增大 |
| C.混合气体加热到230℃,反应的平衡常数很小,故Ni的产率很低 |
D.温度 若在30℃、50℃、80℃之间选择,应选50℃ 若在30℃、50℃、80℃之间选择,应选50℃ |
更新时间:2024-01-29 12:45:31
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
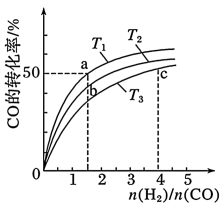
【推荐1】工业上以CO和H2为原料合成甲醇的反应: ,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是
,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是
 ,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是
,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是
| A.H2转化率:c>a>b |
| B.上述三种温度之间关系为T1>T2>T3 |
C.a点状态下再通入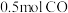 和 和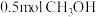 平衡向正方向移动 平衡向正方向移动 |
D.c点状态下再通入 和 和 ,新平衡中 ,新平衡中 的体积分数增大 的体积分数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知反应:N2(g)+3H2(g)  2NH3(g) ΔH=-92 kJ·mol-1温度不同(T2>T1)。下列图象正确的是
2NH3(g) ΔH=-92 kJ·mol-1温度不同(T2>T1)。下列图象正确的是
 2NH3(g) ΔH=-92 kJ·mol-1温度不同(T2>T1)。下列图象正确的是
2NH3(g) ΔH=-92 kJ·mol-1温度不同(T2>T1)。下列图象正确的是| 图象 | 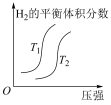 | 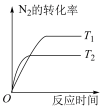 |  | 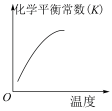 |
| 选项 | A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】一定条件下可利用甲烷消除氮氧化物的污染,例如:CH4+2NO2⇌N2+CO2+2H2O。在2L密闭容器中,控制在不同温度下,分别加入0.50molCH4和0.90molNO2,测得n(CH4)随时间变化的有关实验数据如下表所示。
下列说法不正确 的是
| 组别 | 温度 | n/mol | 时间/min | ||||
| 0 | 10 | 20 | 40 | 50 | |||
| ① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | x | 0.15 |
下列说法
| A.组别①中,0~20min内,NO2的降解速率为0.025mol·L-1·min-1 |
| B.该反应的△H<0 |
| C.40min时,x的数值应为0.15 |
| D.0~20min内NO2的降解百分数①<② |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知常温常压下,N2和H2生成2molNH3放出92.4KJ热量,在同温下向恒容密闭容器中通入1molN2和3molH2,达平衡时放出热量为Q1KJ,向另一体积相同的容器中通入0.5molN2、1.5molH2和1molNH3,相同条件下,达平衡时放出热量为Q2KJ,则下列正确 的是
| A.2Q2﹤Q1﹤92.4 | B.2Q2=Q1=92.4 | C.Q1﹤Q2﹤92.4 | D.Q1=Q2﹤92.4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于平衡体系mA(g)+nB(g) pC(g)+qD(g) ΔH<0。下列结论中错误的是
pC(g)+qD(g) ΔH<0。下列结论中错误的是
 pC(g)+qD(g) ΔH<0。下列结论中错误的是
pC(g)+qD(g) ΔH<0。下列结论中错误的是| A.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n |
| B.若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的1.8倍,则m+n>p+q |
| C.若m+n = p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a |
D.若温度不变缩小容器体积,达到新平衡时压强增大到原来的2倍,则体积一定小于原来的 |
您最近一年使用:0次

 xC(g)+2D(g),经2min后测得D的浓度为0.6mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.3mol•L-1•min-1,下列说法正确的是
xC(g)+2D(g),经2min后测得D的浓度为0.6mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.3mol•L-1•min-1,下列说法正确的是

