侯氏制碱法中,下列操作与回收母液中 无关的是
无关的是
 无关的是
无关的是A.通入 | B.通入 | C.降低温度 | D.添加 |
更新时间:2024-02-17 20:09:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】对于平衡体系mA(g)+nB(g) pC(g)+qD(g) ΔH=b kJ·mol-1,下列结论中正确的是
pC(g)+qD(g) ΔH=b kJ·mol-1,下列结论中正确的是
 pC(g)+qD(g) ΔH=b kJ·mol-1,下列结论中正确的是
pC(g)+qD(g) ΔH=b kJ·mol-1,下列结论中正确的是| A.若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n>p+q |
| B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n |
| C.保持其它条件不变,升高温度,D的体积分数增大说明该反应的ΔH<0 |
| D.若m+n=p+q,则向含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量大于2a mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在密闭容器中发生如下反应mA(g) + nB(g) pC(g) + qD(s),达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.8倍,下列说法正确的是
pC(g) + qD(s),达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.8倍,下列说法正确的是
 pC(g) + qD(s),达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.8倍,下列说法正确的是
pC(g) + qD(s),达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.8倍,下列说法正确的是| A.m+n < p+q | B.平衡向逆反应方向移动 |
| C.A的转化率提高 | D.C的体积分数增加 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在恒容密闭容器中充入一定量的CO2和H2,在不同温度下发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H <0。 CH3OH 的体积分数与起始时H2与CO2的投料比值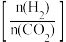 的关系如图甲所示,投料比值 一定时,CH3OH的浓度与温度的关系如图乙所示。
的关系如图甲所示,投料比值 一定时,CH3OH的浓度与温度的关系如图乙所示。
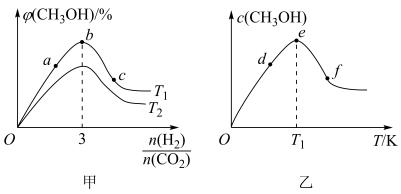
下列推断正确的是
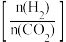 的关系如图甲所示,投料比值 一定时,CH3OH的浓度与温度的关系如图乙所示。
的关系如图甲所示,投料比值 一定时,CH3OH的浓度与温度的关系如图乙所示。
下列推断正确的是
| A.图甲中,T1>T2 |
| B.图甲中,CO2的转化率: b>a>c |
| C.图乙中,T1之前随着温度的升高,平衡正向移动 |
| D.图乙中,CO2的转化率: e>d>f |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列对化学平衡移动的分析中,不正确 的是
①已达平衡的反应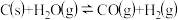 ,当增加反应物的物质的量时,平衡一定向正反应方向移动
,当增加反应物的物质的量时,平衡一定向正反应方向移动
②已达平衡的反应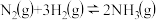 ,当增大
,当增大 的浓度时,平衡向正反应方向移动,
的浓度时,平衡向正反应方向移动, 的转化率一定升高
的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
①已达平衡的反应
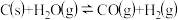 ,当增加反应物的物质的量时,平衡一定向正反应方向移动
,当增加反应物的物质的量时,平衡一定向正反应方向移动②已达平衡的反应
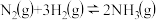 ,当增大
,当增大 的浓度时,平衡向正反应方向移动,
的浓度时,平衡向正反应方向移动, 的转化率一定升高
的转化率一定升高③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
| A.①④ | B.①②③ | C.②③④ | D.①②③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】近年来,将氯化氢转化为氯气的技术成为科学研究的热点。Deacon发明的催化氧化法为4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g)。下图为体积恒定不变的密闭容器中,进料总物质的量一定,c(HCl)∶c(O2)分别为1∶1、4∶1、7∶1时HCl的平衡转化率随温度变化的关系。下列说法正确的是


| A.图中x、y、z三点平衡常数的大小为:x=y<z |
| B.300℃,进料浓度比c(HCl)∶c(O2)=4∶1时,O2平衡转化率为88% |
| C.对于③表示的反应,与100℃时相比,用更高效的催化剂在常温下反应不能改变HCl的平衡转化率 |
| D.①对应的曲线表示的c(HCl)∶c(O2)=7∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 硝酸铵与水合碳酸钠可用于制作冰敷袋 | 该反应的反应物总能量高于生成物总能量 |
| B | 1mol•L-1NaCl溶液的导电性比同浓度醋酸强 | NaCl是强电解质、醋酸是弱电解质 |
| C | 装有NO2的密闭烧瓶冷却后颜色变浅 | NO2转化为N2O4的反应吸热 |
| D | FeCl3水解可生成Fe(OH)3胶体 | FeCl3可用作消毒剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

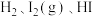 平衡时的混合气体加压后颜色变深
平衡时的混合气体加压后颜色变深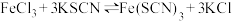 的平衡体系,加入少量
的平衡体系,加入少量 固体后溶液颜色加深
固体后溶液颜色加深 催化氧化成
催化氧化成 的反应,加入催化剂可以增大反应速率
的反应,加入催化剂可以增大反应速率 ,为提高
,为提高


