下列叙述正确的是
| A.稀醋酸中加少量醋酸钠能增大醋酸的电离程度 |
B.25℃时,将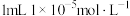 盐酸稀释至1000mL,所得溶液的pH为8 盐酸稀释至1000mL,所得溶液的pH为8 |
| C.蔗糖在水中溶解,这是熵增的过程 |
D.0.1molAgCl和0.1molAgI混合后加入1L水中所得溶液中 |
更新时间:2024-03-11 14:06:26
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法不正确 的是
A. 、 、 的反应在任何温度下都能自发进行 的反应在任何温度下都能自发进行 |
B. 能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C.凡是能量达到活化能的分子发生的碰撞均为有效碰撞 |
| D.对于同一物质来讲,熵值的大小与其状态有关,固态物质的熵值通常最小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.凡是放热反应都是自发的,因为吸热反应都是非自发的 |
| B.自发反应的现象一定非常明显,非自发反应的熵一定减小 |
C.常温下,反应C(s)+CO2(g) 2CO(g)不能自发进行,则该反应的ΔΗ>0 2CO(g)不能自发进行,则该反应的ΔΗ>0 |
| D.反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的ΔΗ>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列各组微粒在给定条件下能大量共存的是
A.澄清透明溶液中: |
B.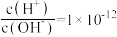 的溶液中: 的溶液中: |
C. 的 的 溶液中: 溶液中: |
D.能使甲基橙变红的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列溶液一定呈酸性的是 ( )
| A.c(H+)=10-6 mol·L-1的溶液 | B.pH<7的溶液 |
| C.c(H+)>c(OH-)的溶液 | D.含有H+的溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,向20 mL0.1 mol/L H2A溶液中逐滴加入0.1 mol/L NaOH溶液,H2A溶液中各粒子浓度分数δ(X)随溶液pH变化的关系如图所示。下列说法错误的是


| A.当溶液中A元素的主要存在形态为A2-时,溶液可能为弱酸性、中性或碱性 |
| B.当加入NaOH溶液至20 mL时,溶液中存在((Na+)=2c(A2-)+c(HA-) |
| C.室温下,反应A2-+H2A=2HA-的平衡常数的对数值lgK=3 |
| D.室温下,弱酸H2A的第一级电离平衡常数用Ka1表示,Na2A的第二级水解平衡常数用Kh2表示,则Kal>Kh2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在常温下,取一定量的蒸馏水,然后将Cl2缓慢通入水中至饱和,再向所得饱和氯水中滴加0.1mol/L的NaOH溶液。整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是


| A.实验进程中可用pH试纸测定溶液的pH |
| B.向a点所示溶液中能入SO2,溶液的酸性和漂白性均增强 |
C.由a点到b点的过程中,溶液中 减小 减小 |
| D.c点所示的溶液中,c(Na+)= c(ClO-) + c(Cl-) |
您最近一年使用:0次
【推荐1】下列实验操作、现象、结论均正确的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 向锌和稀硫酸反应的试管中滴加几滴CuSO4溶液 | 气泡生成速率加快 | CuSO4是该反应的催化剂 |
| B | 向含有酚酞的 溶液中滴入 溶液中滴入 溶液,观察溶液颜色的变化 溶液,观察溶液颜色的变化 | 溶液颜色变浅 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| C | 取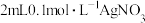 溶液,先后滴加3滴 溶液,先后滴加3滴 溶液和5滴 溶液和5滴 溶液,观察沉淀情况 溶液,观察沉淀情况 | 先生成白色沉淀,后变为黄色沉淀 |  > > |
| D | 已知H3BO3:Ka=5.8×10-10;H2CO3:Ka1=4.5×10-7、Ka2=4.7×10-11向饱和硼酸溶液中滴加碳酸钠溶液 | 无明显现象 | H3BO3与碳酸钠不反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在 和
和 的混合液中先加入过量的KI溶液,再加入足量
的混合液中先加入过量的KI溶液,再加入足量 溶液,最后所得沉淀是( )
溶液,最后所得沉淀是( )
 和
和 的混合液中先加入过量的KI溶液,再加入足量
的混合液中先加入过量的KI溶液,再加入足量 溶液,最后所得沉淀是( )
溶液,最后所得沉淀是( )A. 、 、 | B.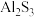 、 、 |
C. 、 、 | D.FeS、 、S 、S |
您最近一年使用:0次

 保持不变
保持不变
 的值减小
的值减小

