实验小组探究 溶液与KI溶液的反应及其速率,实验过程和现象如表。
溶液与KI溶液的反应及其速率,实验过程和现象如表。
已知:ⅰ. 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;
ⅱ.淀粉检测 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝;
即可快速变蓝;
ⅲ. 与
与 发生反应:
发生反应: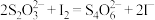
(1)实验1-1的目的是___________ ;
(2)实验1-2中 与KI反应的离子方程式为
与KI反应的离子方程式为___________ ;
为了探究 与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,实验结果如下表
与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,实验结果如下表
(3)加入 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
猜想1: 先与
先与 反应,使
反应,使 降低;
降低;
猜想2: 先与KI反应,___________。
先与KI反应,___________。
①甲同学提出猜想1的依据:由信息ⅲ推测, 的还原性
的还原性___________ (填“强于”或“弱于”)KI的;
②乙同学根据现有数据证明猜想1不成立,理由是实验2-2与 完全反应后的溶液中
完全反应后的溶液中
___________ 2-1中起始 ,溶液应立即变蓝(填“高于”或“低于”);
,溶液应立即变蓝(填“高于”或“低于”);
③补全猜想2:___________ ;
(4)查阅文献表明猜想2成立。根据实验2-2的数据,计算30s内的平均反应速率
___________  (列出计算式);
(列出计算式);
(5)实验2-2中,30s内未检测到 与
与 反应,可能的原因是
反应,可能的原因是___________ (写出两条)。
 溶液与KI溶液的反应及其速率,实验过程和现象如表。
溶液与KI溶液的反应及其速率,实验过程和现象如表。已知:ⅰ.
 具有强氧化性,能完全电离,
具有强氧化性,能完全电离, 易被还原为
易被还原为 ;
;ⅱ.淀粉检测
 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝;
即可快速变蓝;ⅲ.
 与
与 发生反应:
发生反应: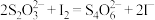
| 编号 | 1-1 | 1-2 |
| 实验操作 | 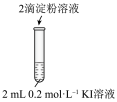 | 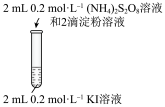 |
| 现象 | 无明显现象 | 溶液立即变蓝 |
(1)实验1-1的目的是
(2)实验1-2中
 与KI反应的离子方程式为
与KI反应的离子方程式为为了探究
 与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,实验结果如下表
与KI反应的速率,小组同学分别向两支试管中依次加入下列试剂,并记录变色时间,实验结果如下表| 编号 |  KI溶液/mL KI溶液/mL |   溶液/mL 溶液/mL | 蒸馏水/mL | 0.4%淀粉溶液/滴 |   溶液/mL 溶液/mL | 变色时间/s |
| 2-1 | 2 | 0 | 2.8 | 2 | 0.2 | 立即 |
| 2-2 | 2 | 0.8 | 0.2 | 2 | 2 | 30 |
(3)加入
 溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。
溶液后溶液变蓝的时间明显增长,甲同学对此提出两种猜想。猜想1:
 先与
先与 反应,使
反应,使 降低;
降低;猜想2:
 先与KI反应,___________。
先与KI反应,___________。①甲同学提出猜想1的依据:由信息ⅲ推测,
 的还原性
的还原性②乙同学根据现有数据证明猜想1不成立,理由是实验2-2与
 完全反应后的溶液中
完全反应后的溶液中
 ,溶液应立即变蓝(填“高于”或“低于”);
,溶液应立即变蓝(填“高于”或“低于”);③补全猜想2:
(4)查阅文献表明猜想2成立。根据实验2-2的数据,计算30s内的平均反应速率

 (列出计算式);
(列出计算式);(5)实验2-2中,30s内未检测到
 与
与 反应,可能的原因是
反应,可能的原因是
更新时间:2024-03-13 16:10:53
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
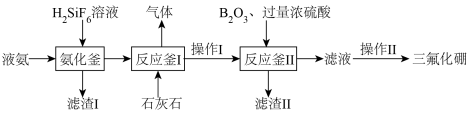
【推荐1】常温下 是一种无色气体、溶于浓硫酸、易水解,常用作火箭高能燃料。工业用液氨法制取
是一种无色气体、溶于浓硫酸、易水解,常用作火箭高能燃料。工业用液氨法制取 的流程如下:
的流程如下:
已知:①硼酐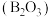 是一种难溶物;
是一种难溶物;
②石灰石中含有微量氧化铁、二氧化硅、硫单质等
回答下列问题:
(1)氨化釜中主要产物为 ,则滤渣Ⅰ的成分是
,则滤渣Ⅰ的成分是_______ ,操作Ⅱ的名称_______ 。
(2)反应釜Ⅰ中产生两种气体,发生反应的离子方程式为_______ 。
(3)经过必要的处理可循环利用的物质是_______ 。
(4)反应釜Ⅱ中发生反应的化学方程式_______ 。
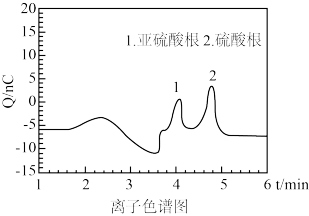
(5)利用离子色谱法可以检测三氟化硼中硫元素的含量,将 样品通过检测液,进行色谱分析,得到如图所示结果。出现曲线1的原因可能是
样品通过检测液,进行色谱分析,得到如图所示结果。出现曲线1的原因可能是_______ 。
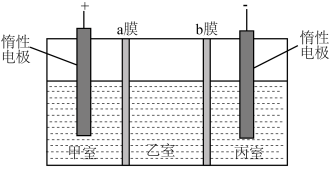
(6)利用电解氟硅酸钠 的方法可以制取高纯度
的方法可以制取高纯度 ,装置如图所示。甲室中加入的电解质为
,装置如图所示。甲室中加入的电解质为_______ ,a膜选用_______ (“阴离子”“阳离子”“质子”)交换膜。
 是一种无色气体、溶于浓硫酸、易水解,常用作火箭高能燃料。工业用液氨法制取
是一种无色气体、溶于浓硫酸、易水解,常用作火箭高能燃料。工业用液氨法制取 的流程如下:
的流程如下:
已知:①硼酐
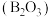 是一种难溶物;
是一种难溶物;②石灰石中含有微量氧化铁、二氧化硅、硫单质等
回答下列问题:
(1)氨化釜中主要产物为
 ,则滤渣Ⅰ的成分是
,则滤渣Ⅰ的成分是(2)反应釜Ⅰ中产生两种气体,发生反应的离子方程式为
(3)经过必要的处理可循环利用的物质是
(4)反应釜Ⅱ中发生反应的化学方程式
(5)利用离子色谱法可以检测三氟化硼中硫元素的含量,将
 样品通过检测液,进行色谱分析,得到如图所示结果。出现曲线1的原因可能是
样品通过检测液,进行色谱分析,得到如图所示结果。出现曲线1的原因可能是
(6)利用电解氟硅酸钠
 的方法可以制取高纯度
的方法可以制取高纯度 ,装置如图所示。甲室中加入的电解质为
,装置如图所示。甲室中加入的电解质为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】化学与生产、生活密切相关,请根据下列要求作答。
I.桂皮中含有的肉桂醛(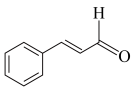 )是一种食用香料,广泛应用于牙膏、洗涤剂、糖果等,工业上可通过苯甲醛和乙醛为原料制得,研究发现实际反应要通过①②两步反应完成制备,如下图所示:
)是一种食用香料,广泛应用于牙膏、洗涤剂、糖果等,工业上可通过苯甲醛和乙醛为原料制得,研究发现实际反应要通过①②两步反应完成制备,如下图所示:
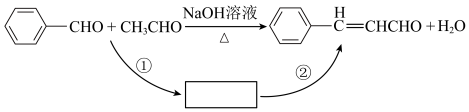
(1)已知反应①为加成反应,则反应②的反应类型为___________ 。
Ⅱ.蔗糖是重要的二糖,在一定条件下会发生水解反应。
(2)①为检验蔗糖的水解产物,需要配制银氨溶液,过程为:向试管中加入1mL2%AgNO3溶液,边振荡边滴加2%氨水到沉淀恰好完全溶解,写出配制银氨溶液总反应的离子方程式___________ 。
②补充完整验证蔗糖水解产物中含有葡萄糖的实验方案:取少量的10%的蔗糖溶液于试管中,___________ 。(实验中须使用的试剂有:10%的H2SO4溶液、10%的NaOH溶液、银氨溶液、pH试纸)
Ⅲ.硫化钠是重要的化工原料,大多采用无水芒硝(Na2SO4)一炭粉还原法制备,原理为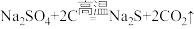 。其主要流程如下:
。其主要流程如下:
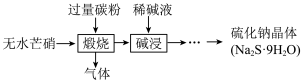
(3)上述流程中采用稀碱液比用热水更好,理由是___________ 。
(4)已知: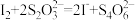 。上述所制得的Na2S·9H2O晶体中含有NaS2S2O3·5H2O(相对质量为248)等杂质。为测定产品的成分,进行下列实验:
。上述所制得的Na2S·9H2O晶体中含有NaS2S2O3·5H2O(相对质量为248)等杂质。为测定产品的成分,进行下列实验:
a.取试样10.00g配成500.00ml溶液。
b.取所配溶液25.00mL于碘量瓶中,加入过量ZnCO3悬浊液除去Na2S后,过滤,向滤液中滴入2~3滴淀粉溶液,用0.05000mo1·L-1I2溶液滴定至终点,用去5.00mLI2溶液。
①步骤b中用ZnCO3除去Na2S的离子方程式为___________ 。
②判断步骤b中滴定终点的现象为___________ 。
③计算试样中Na2S2O3·5H2O的质量分数(写出计算过程)。___________ 。
I.桂皮中含有的肉桂醛(
 )是一种食用香料,广泛应用于牙膏、洗涤剂、糖果等,工业上可通过苯甲醛和乙醛为原料制得,研究发现实际反应要通过①②两步反应完成制备,如下图所示:
)是一种食用香料,广泛应用于牙膏、洗涤剂、糖果等,工业上可通过苯甲醛和乙醛为原料制得,研究发现实际反应要通过①②两步反应完成制备,如下图所示:
(1)已知反应①为加成反应,则反应②的反应类型为
Ⅱ.蔗糖是重要的二糖,在一定条件下会发生水解反应。
(2)①为检验蔗糖的水解产物,需要配制银氨溶液,过程为:向试管中加入1mL2%AgNO3溶液,边振荡边滴加2%氨水到沉淀恰好完全溶解,写出配制银氨溶液总反应的离子方程式
②补充完整验证蔗糖水解产物中含有葡萄糖的实验方案:取少量的10%的蔗糖溶液于试管中,
Ⅲ.硫化钠是重要的化工原料,大多采用无水芒硝(Na2SO4)一炭粉还原法制备,原理为
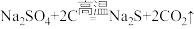 。其主要流程如下:
。其主要流程如下:
(3)上述流程中采用稀碱液比用热水更好,理由是
(4)已知:
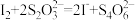 。上述所制得的Na2S·9H2O晶体中含有NaS2S2O3·5H2O(相对质量为248)等杂质。为测定产品的成分,进行下列实验:
。上述所制得的Na2S·9H2O晶体中含有NaS2S2O3·5H2O(相对质量为248)等杂质。为测定产品的成分,进行下列实验:a.取试样10.00g配成500.00ml溶液。
b.取所配溶液25.00mL于碘量瓶中,加入过量ZnCO3悬浊液除去Na2S后,过滤,向滤液中滴入2~3滴淀粉溶液,用0.05000mo1·L-1I2溶液滴定至终点,用去5.00mLI2溶液。
①步骤b中用ZnCO3除去Na2S的离子方程式为
②判断步骤b中滴定终点的现象为
③计算试样中Na2S2O3·5H2O的质量分数(写出计算过程)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
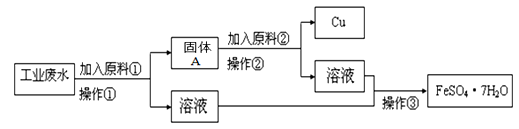
【推荐3】某工厂的工业废水中含有大量的“FeSO4”、较多的Cu2+和少量的Na+。为了减少污染变废为宝,工厂计划从该废水中回收硫酸亚铁和铜。根据流程图,完成回收硫酸亚铁和铜的简单实验方案。回答下列问题:
(1)加入原料①为____________ ;操作②的名称为___________ ,该操作所用到的玻璃仪器主要有______ 。
(2)固体A为____________ ;
(3)写出加入原料①和②有关反应的离子方程式__________________ 、________________________ 。
(4)操作③获得FeSO4·7H2O,需要经过_____ 、_____ 、过滤等操作。
(1)加入原料①为
(2)固体A为
(3)写出加入原料①和②有关反应的离子方程式
(4)操作③获得FeSO4·7H2O,需要经过
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】过氧化锶(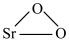 )通常用作分析试剂、氧化剂、漂白剂等。SrO2是一种白色粉末,加热条件下可与CO2、水蒸气反应,室温时在水中逐渐形成无色晶体SrO2·8H2O,与酸作用生成H2O2。
)通常用作分析试剂、氧化剂、漂白剂等。SrO2是一种白色粉末,加热条件下可与CO2、水蒸气反应,室温时在水中逐渐形成无色晶体SrO2·8H2O,与酸作用生成H2O2。
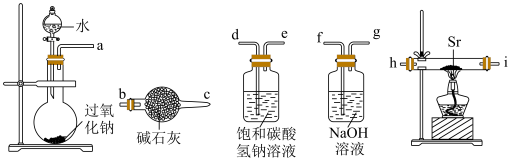
②SrO2在空气中会变质生成碳酸盐,写出该反应的化学方程式
③连接好装置进行实验,实验步骤如下,正确的操作顺序为
a、打开分液漏斗活塞,将水滴入烧瓶中b、检查装置气密性c、在相应装置中装入药品d、加热e、关闭分液漏斗活塞f、停止加热
(2)乙同学在通入氨气的条件下,在水溶液中可制备得到SrO2·8H2O,实验装置如图:
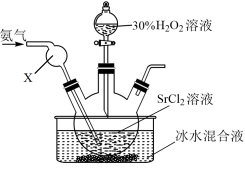
②写出该方法制备SrO2·8H2O的离子方程式
③实验结束后,得到SrO2·8H2O的操作为
(3)除SrO2·8H2O外,请选择下列试剂:FeCl2溶液、HCl溶液、HNO3溶液、KSCN溶液、H2O2溶液设计实验证明SrO2的氧化性比FeCl3的氧化性强:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某小组同学用下图1装置制取氯气并探究其性质(夹持装置和加热仪器略)。
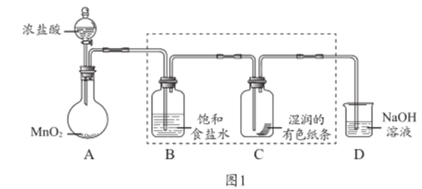
请回答:
(1)装置A中制取氯气的化学方程式是 ,反应中利用了
,反应中利用了 的
的_______ (填字母)。
a.氧化性 b.还原性
若生成 的物质的量是0.2mol,该气体在标准状况下的体积为
的物质的量是0.2mol,该气体在标准状况下的体积为_______ L。
(2)装置C中的现象是_______ 。
(3)装置D的作用是_______ 。
(4)氯气溶解在石灰乳中可以制漂白粉,发生反应的化学方程式为_______ 。
(5)若将上述图1中B和C分别换成图2中的M和N,则:
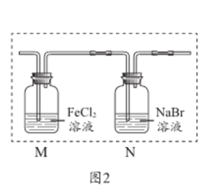
①M中发生反应的离子方程式为_______ 。
②取一支试管,加入2mLN中变橙黄色的溶液。再滴入几滴淀粉KI溶液,观察到溶液变为蓝色。通过以上实验,能否 得出结论: 的氧化性强于
的氧化性强于 ,的。理由
,的。理由_______ 。

请回答:
(1)装置A中制取氯气的化学方程式是
 ,反应中利用了
,反应中利用了 的
的a.氧化性 b.还原性
若生成
 的物质的量是0.2mol,该气体在标准状况下的体积为
的物质的量是0.2mol,该气体在标准状况下的体积为(2)装置C中的现象是
(3)装置D的作用是
(4)氯气溶解在石灰乳中可以制漂白粉,发生反应的化学方程式为
(5)若将上述图1中B和C分别换成图2中的M和N,则:

①M中发生反应的离子方程式为
②取一支试管,加入2mLN中变橙黄色的溶液。再滴入几滴淀粉KI溶液,观察到溶液变为蓝色。通过以上实验,
 的氧化性强于
的氧化性强于 ,的。理由
,的。理由
您最近一年使用:0次
【推荐3】I.溴有“海洋元素”之称,海水中溴含量为65mg•L-1。空气吹出法工艺是目前“海水提溴”的最主要方法之一,其步骤如下:
(1)步骤①中获得Br2的离子方程式为___________ 。
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是___________ 。
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2,共有___________ 个电子转移(用a和 的代数式表示)。
的代数式表示)。
Ⅱ.碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的实验流程如下:___________ 、___________ 。
(5)“试剂a”通常应具有一定的___________ 性。
(6)由于“溶液B”中I2的含量较低,“操作Ⅱ”能将I2 “富集、浓缩”到“有机溶液X”中。已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___________ (填试剂标号)。
(7)“操作Ⅱ”宜选用的装置是___________ (填标号)。___________ 。

(1)步骤①中获得Br2的离子方程式为
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2,共有
 的代数式表示)。
的代数式表示)。Ⅱ.碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的实验流程如下:

(5)“试剂a”通常应具有一定的
(6)由于“溶液B”中I2的含量较低,“操作Ⅱ”能将I2 “富集、浓缩”到“有机溶液X”中。已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.氯仿 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶,不与I2反应 | 与水不互溶,不与 I2反应 | 与水不互溶,不与I2反应 | 与水不互溶,与I2反应 |
(7)“操作Ⅱ”宜选用的装置是
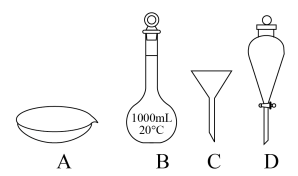
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】汽车尾气中含有 、CO,排气管内的催化转化器可实现将污染性气体转化为
、CO,排气管内的催化转化器可实现将污染性气体转化为 和
和 。
。
(1)已知:①

②

③
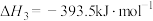
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。该反应在___________ (填“高温”或“低温”)下可自发进行。
(2)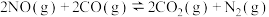 的反应历程如图(图中所有物质均为气态)。
的反应历程如图(图中所有物质均为气态)。
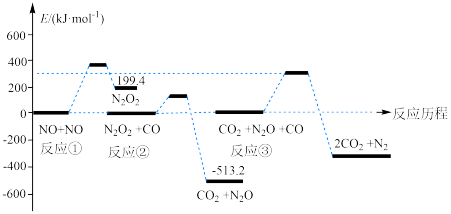
该反应的决速步骤是反应___________ (填对应序号);中间产物的化学式为___________ 。
(3)利用如图装置可测定汽车尾气中CO的含量,电解质为氧化钇 和氧化钠,该电池中
和氧化钠,该电池中 可以在固体介质
可以在固体介质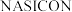 (固熔体)内自由移动。
(固熔体)内自由移动。
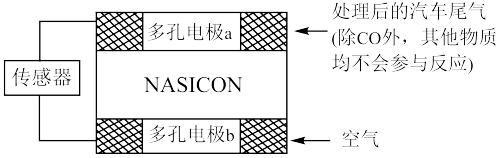
工作时,多孔电极a为___________ 极,多孔电极b处发生的电极反应为___________ 。
(4)一定温度下,起始时向 的恒容密闭容器中充入
的恒容密闭容器中充入 、
、 ,仅发生反应
,仅发生反应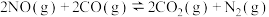 ,起始气体总压强为
,起始气体总压强为 ,
, 时反应达到平衡,此时气体总压强为起始压强的
时反应达到平衡,此时气体总压强为起始压强的 。
。
①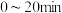 内,
内,
________  ,NO转化率=
,NO转化率=________ (保留三位有效数字)%。
②此温度下,该反应的平衡常数
_______  (
( 是用平衡分压代替平衡浓度计算的平衡常数)。
是用平衡分压代替平衡浓度计算的平衡常数)。
 、CO,排气管内的催化转化器可实现将污染性气体转化为
、CO,排气管内的催化转化器可实现将污染性气体转化为 和
和 。
。(1)已知:①


②


③

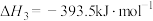
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)
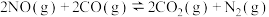 的反应历程如图(图中所有物质均为气态)。
的反应历程如图(图中所有物质均为气态)。
该反应的决速步骤是反应
(3)利用如图装置可测定汽车尾气中CO的含量,电解质为氧化钇
 和氧化钠,该电池中
和氧化钠,该电池中 可以在固体介质
可以在固体介质 (固熔体)内自由移动。
(固熔体)内自由移动。
工作时,多孔电极a为
(4)一定温度下,起始时向
 的恒容密闭容器中充入
的恒容密闭容器中充入 、
、 ,仅发生反应
,仅发生反应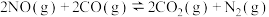 ,起始气体总压强为
,起始气体总压强为 ,
, 时反应达到平衡,此时气体总压强为起始压强的
时反应达到平衡,此时气体总压强为起始压强的 。
。①
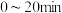 内,
内,
 ,NO转化率=
,NO转化率=②此温度下,该反应的平衡常数

 (
( 是用平衡分压代替平衡浓度计算的平衡常数)。
是用平衡分压代替平衡浓度计算的平衡常数)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】甲醇是一种理想的液体燃料,工业上可利用CO与H2反应合成甲醇,即CO(g)+2H2(g)⇌CH3OH(g),该反应是放热反应。若在体积为2L的密闭容器中加入5molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间的变化情况如图所示。
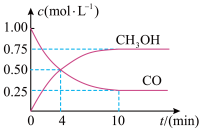
(1)该反应在0-4min内用H2表示的反应速率为:v(H2) =_____ mol·L-1·s-1;10min末H2的转化率______ ; CO的体积分数________ 。
(2)该反应进行10min后,若体积不变,通入惰性气体则正应速率将______ ;在其他条件不变时,只升高体系的温度,则该反应的逆反应速率将______ 。 (填“增大”、“减小”或“不变”)
(3)当温度和体积一定时,该反应达到平衡状态的标志是______
A.混合气体的密度不变
B.CO、H2、CH3OH的反应速率之比为1: 2: 1
C.混合气体的平均相对分子质量不变
D.混合气体的质量不变
E.混合气体的压强不变
F.单位时间内生成a mol CH3OH,同时消耗2a mol H2
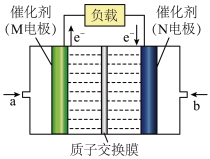
(4)如图是某研究机构开发的给笔记本电脑供电的甲醇燃料电池,甲醇在催化剂作用下提供质子(H+)和电子,M应作为原电池的_____ (填“正极”或“负极”);H+通过质子交换膜移向____ (填M电极或N电极);其负极的电极反应式为_______ 。

(1)该反应在0-4min内用H2表示的反应速率为:v(H2) =
(2)该反应进行10min后,若体积不变,通入惰性气体则正应速率将
(3)当温度和体积一定时,该反应达到平衡状态的标志是
A.混合气体的密度不变
B.CO、H2、CH3OH的反应速率之比为1: 2: 1
C.混合气体的平均相对分子质量不变
D.混合气体的质量不变
E.混合气体的压强不变
F.单位时间内生成a mol CH3OH,同时消耗2a mol H2
(4)如图是某研究机构开发的给笔记本电脑供电的甲醇燃料电池,甲醇在催化剂作用下提供质子(H+)和电子,M应作为原电池的

您最近一年使用:0次
【推荐3】上海建有以“液态阳光”甲醇为氢源,集制氢、储氢、加氢为一体的新型加氢站。甲醇水蒸气重整制氢的部分原理如下:
反应①:CH3OH(g)+H2O(g) CO2(g)+3H2(g) ∆H1=49kJ·mol−1
CO2(g)+3H2(g) ∆H1=49kJ·mol−1
反应②:H2(g)+CO2(g) CO(g)+H2O(g) ∆H2=41kJ·mol−1
CO(g)+H2O(g) ∆H2=41kJ·mol−1
(1)对反应①的下列判断正确的是___________。
(2)一定条件下,向2L恒容密闭容器中充入2mol CH3OH(g)和4mol H2O(g)发生反应①,2min时测得混合气体的压强是反应前的1.5倍,则2min内的υ(CH3OH)=___________ 。
(3)下列事实不能说明反应①已达到平衡状态的是___________。
(4)向某密闭容器中按下列比例通入CO和H2O发生反应②,在不同温度下,CO的平衡转化率如下表所示:
①比较大小:T1___________ T2(填写“大于”、“小于”或“等于”),判断理由是___________ 。
②T2℃时,反应②的化学平衡常数K =___________ 。
反应①:CH3OH(g)+H2O(g)
 CO2(g)+3H2(g) ∆H1=49kJ·mol−1
CO2(g)+3H2(g) ∆H1=49kJ·mol−1反应②:H2(g)+CO2(g)
 CO(g)+H2O(g) ∆H2=41kJ·mol−1
CO(g)+H2O(g) ∆H2=41kJ·mol−1(1)对反应①的下列判断正确的是___________。
| A.ΔS大于0,低温能自发进行 | B.ΔS小于0,高温能自发进行 |
| C.ΔS小于0,低温能自发进行 | D.ΔS大于0,高温能自发进行 |
(3)下列事实不能说明反应①已达到平衡状态的是___________。
| A.混合气体的平均相对分子质量不变 | B.υ正(CH3OH)=3υ逆(H2) |
| C.CH3OH的浓度不再变化 | D.绝热容器内的温度保持不变 |
| 反应温度(℃) | 进气比[n(CO):n(H2O)] | CO的平衡转化率 |
| T1 | 0.5 | 50% |
| T1 | 1 | 36.67% |
| T2 | 0.5 | 66.67% |
| T2 | 1 | 50% |
②T2℃时,反应②的化学平衡常数K =
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】影响化学反应速率的因素有很多方面。请回答下列问题:
(一)某学习小组同学根据影响化学反应速率的因素进行实验验证,其设计的实验方案如下:请你帮他们把表填写完整,并做出评价。
(1)甲同学验证还原性:I->Br-
(2)(评价)甲同学设计的实验方案是___________ (填“合理”或“不合理”),理由是___________ 。
(3)乙同学验证固体反应物的颗粒大小对反应速率的影响
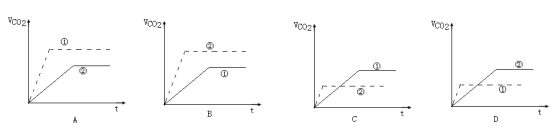
实验步骤:在试管①中加入1g粉末状大理石,加入4mol/L盐酸20mL(过量);在试管②中加入2g颗粒状大理石,加入4mol/L盐酸20mL(过量)。他根据实验过程,绘制出的生成CO2生成体积(折算成标准状况)V(CO2)同反应时间t的关系曲线图,你认为___________ 是符合的。
(二)某同学做浓度对化学反应速率的影响的实验时,将3支试管编号为①②③,并按下表中物质的量进行实验,记录下的时间数据是:16 s、28 s、33 s。请将3个数据填入下表的适当位置,并写出实验结论。
(1)将对应①、②、③的时间分别写出:
(a)___________ ,(b)___________ ,(c)___________ 。
(2)实验结论:___________ 。
(一)某学习小组同学根据影响化学反应速率的因素进行实验验证,其设计的实验方案如下:请你帮他们把表填写完整,并做出评价。
| 实验步骤 | 实验现象 | 实验结论及离子反应式 |
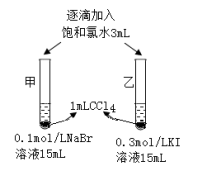 | 逐滴加入的同时振荡,观察CCl4层的颜色: 甲 乙 乙中CCl4层颜色明显变化的快。 | 离子方程式: 甲 乙 结论:验证成立,还原性,I->Br- |
(2)(评价)甲同学设计的实验方案是
(3)乙同学验证固体反应物的颗粒大小对反应速率的影响
实验步骤:在试管①中加入1g粉末状大理石,加入4mol/L盐酸20mL(过量);在试管②中加入2g颗粒状大理石,加入4mol/L盐酸20mL(过量)。他根据实验过程,绘制出的生成CO2生成体积(折算成标准状况)V(CO2)同反应时间t的关系曲线图,你认为

(二)某同学做浓度对化学反应速率的影响的实验时,将3支试管编号为①②③,并按下表中物质的量进行实验,记录下的时间数据是:16 s、28 s、33 s。请将3个数据填入下表的适当位置,并写出实验结论。
| 试管编号 | 加3%Na2S2O3 | 加H2O | 加H2SO4(1∶5) | 出现浑浊时间 |
| ① | 3 mL | 3 mL | 5滴 | (a)_____ |
| ② | 4 mL | 2 mL | 5滴 | (b)_____ |
| ③ | 5 mL | 1 mL | 5滴 | (c)_____ |
(a)
(2)实验结论:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ.某探究性学习小组利用 溶液和酸性
溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
(1)通过实验A、B可探究___________ (填外部因素)的改变对反应速率的影响,其中
___________ ;
___________ ;通过实验___________ 可探究温度变化对化学反应速率的影响。
(2)若 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是___________ ;利用实验B中数据计算,用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为___________ mol/(L·min)。
Ⅱ.在2L密闭容器中进行反应:mX(g)+nY(g)=pZ(g)+qQ(g),式中 为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
已知2min内v(Q)=0.3mol·L−1·min−1,v (Z):v (Y)=2:3。
(3)化学方程式中m=___________ ,n=___________ ,p=___________ ,q=___________ 。
 溶液和酸性
溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。| 实验序号 | 实验温度/K |  溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | 溶液颜色褪至无色时所需时间/s | ||
 |  |  | 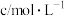 |  | |||
| A | 293 | 2 | 0.02 | 5 | 0.1 | 5 |  |
| B |  | 2 | 0.02 | 4 | 0.1 |  | 8 |
| C | 313 | 2 | 0.02 |  | 0.1 | 6 |  |


(2)若
 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为Ⅱ.在2L密闭容器中进行反应:mX(g)+nY(g)=pZ(g)+qQ(g),式中
 为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:| X | Y | Z | Q | |
| 起始/mol | 1.2 | 0 | ||
| 2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3min末/mol | 0.8 |
(3)化学方程式中m=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】Ⅰ.温度为T时,某容积为 的密闭容器内,A、B两种气态物质的物质的量随时间变化的曲线如图所示,回答下列问题:
的密闭容器内,A、B两种气态物质的物质的量随时间变化的曲线如图所示,回答下列问题:
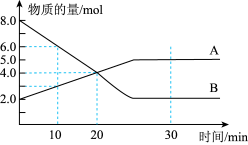
(1)该反应的化学方程式为___________ 。
(2) ,用B表示的平均反应速率
,用B表示的平均反应速率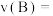
___________  。
。
(3)下列措施能增大反应速率的是___________(填字母)。
Ⅱ.纸电池是未来电池发展的重要研究方向。某学生在课外活动时,根据如图纸电池结构示意图,利用实验室中的稀硫酸、蒸馏水和滤纸制作电解液,用铜片与镁片作为电极材料。

(4)电池工作时 向
向___________ (填a或b)极作定向移动。
(5)某学生用硫酸铜溶液替代稀硫酸,正极发生的电极反应式为___________ 。
 的密闭容器内,A、B两种气态物质的物质的量随时间变化的曲线如图所示,回答下列问题:
的密闭容器内,A、B两种气态物质的物质的量随时间变化的曲线如图所示,回答下列问题:
(1)该反应的化学方程式为
(2)
 ,用B表示的平均反应速率
,用B表示的平均反应速率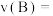
 。
。(3)下列措施能增大反应速率的是___________(填字母)。
| A.升高温度 | B.减小A的浓度 |
| C.缩小容器体积 | D.恒温恒容条件下充入氦气 |
Ⅱ.纸电池是未来电池发展的重要研究方向。某学生在课外活动时,根据如图纸电池结构示意图,利用实验室中的稀硫酸、蒸馏水和滤纸制作电解液,用铜片与镁片作为电极材料。

(4)电池工作时
 向
向(5)某学生用硫酸铜溶液替代稀硫酸,正极发生的电极反应式为
您最近一年使用:0次



