原子序数小于36的X、Y、Z、W、J、G六种元素,原子序数依次增大,其中X元素的原子在所有原子中半径最小,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,J元素原子核外的3p能级有两个电子,G元素原子核外有6个未成对电子(用元素符号或化学式表示)。
(1)写出G元素的基态原子的价电子排布式___________ ; 分子中σ键与π键数目之比为
分子中σ键与π键数目之比为___________ 。
(2)Y、Z、W三种元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
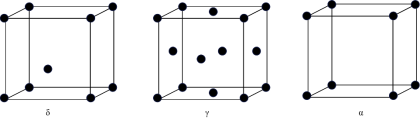
(3)G元素有δ、γ、α三种同素异形体,晶胞结构如图所示。三种晶体的晶胞中所含有的G原子数之比为___________ 。
(1)写出G元素的基态原子的价电子排布式
 分子中σ键与π键数目之比为
分子中σ键与π键数目之比为(2)Y、Z、W三种元素第一电离能由大到小的顺序为
(3)G元素有δ、γ、α三种同素异形体,晶胞结构如图所示。三种晶体的晶胞中所含有的G原子数之比为

更新时间:2024-03-16 21:23:15
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】锌在工业中有重要作用,也是人体必需的微量元素。
(1)基态Zn的核外电子排布式为_______ 。
(2)《中华本草》等中医典籍中记载了炉甘石(ZnCO3)处方药,可用于治疗皮肤炎症或表面创伤。ZnCO3中阴离子空间结构为_______ ,C的杂化方式为_______ 。
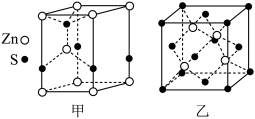
(3)硫化锌有两种常见的晶体,分别是六方硫化锌(晶胞结构如图甲所示)和立方硫化锌(晶胞结构如图乙所示)。每个六方硫化锌晶胞中含_______ 个S原子,立方硫化锌中锌的配位数为_______ 。
(4)Zn2+能与NH3形成配离子[Zn(NH3)4]2+,该配离子的中心离子是_______ ,1mol该离子有含σ键的数目为_______ NA。
(1)基态Zn的核外电子排布式为
(2)《中华本草》等中医典籍中记载了炉甘石(ZnCO3)处方药,可用于治疗皮肤炎症或表面创伤。ZnCO3中阴离子空间结构为
(3)硫化锌有两种常见的晶体,分别是六方硫化锌(晶胞结构如图甲所示)和立方硫化锌(晶胞结构如图乙所示)。每个六方硫化锌晶胞中含

(4)Zn2+能与NH3形成配离子[Zn(NH3)4]2+,该配离子的中心离子是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】原子序数依次递增的A、B、C、D、E、F五种元素,其中A、B、C属于同一周期,A原子最外层p能级中的电子数等于次外层的电子总数,C原子最外层中有2个不成对的电子;元素D的焰色试验呈紫色;E原子的最高能层为N层,且在同周期元素的基态原子中不成对电子数最多;F的原子序数为26。请回答下列问题:
(1)A、B、C三种元素的第一电离能由大到小的顺序为_______ 。
(2)说明元素D具有焰色试验的原因:_______ 。
(3)E的基态原子的外围电子排布式为_______ 。
(4)F在元素周期表中的位置是_______ 。
(1)A、B、C三种元素的第一电离能由大到小的顺序为
(2)说明元素D具有焰色试验的原因:
(3)E的基态原子的外围电子排布式为
(4)F在元素周期表中的位置是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钙钛矿(主要成分是CaTiO3)太阳能薄膜电池制备工艺简单、成本低、效率高,引起了科研工作者的广泛关注,科学家认为钙钛矿太阳能电池将取代硅基太阳能电池的统治地位。
(1)基态Ti原子的价电子排布式为__ ,能量最高的能级有__ 个空轨道;Si、P、S第一电离能由小到大顺序是__ 。
(2)碳和硅的有关化学键键能如表所示:
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是___ 。
(3)一种新型熔融盐燃料电池以Li2CO3和Na2CO3的熔融盐混合物作电解质,则CO32-的空间构型为___ 。
(4)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图:
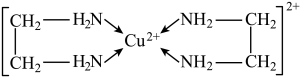
该配离子中含有的化学键类型有__ (填字母)。
a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有__ 个σ键,C原子的杂化方式为__ 。
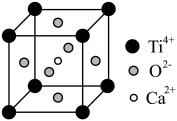
(5)CaTiO3的晶胞为立方晶胞,结构如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角)Ca2+的配位数为__ ,与Ti4+距离最近且相等的O2-有__ 个;晶体的密度为ρg/cm3,最近的Ti4+和O2-之间的距离为__ nm(填计算式)。(CaTiO3的摩尔质量为136g/mol,NA为阿伏加 德罗常数)。
(1)基态Ti原子的价电子排布式为
(2)碳和硅的有关化学键键能如表所示:
| 化学键 | C−C | C−H | C−O | Si−Si | Si−H | Si−O |
| 键能/kJ▪mol-1 | 356 | 413 | 336 | 226 | 318 | 452 |
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是
(3)一种新型熔融盐燃料电池以Li2CO3和Na2CO3的熔融盐混合物作电解质,则CO32-的空间构型为
(4)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图:

该配离子中含有的化学键类型有
a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有
(5)CaTiO3的晶胞为立方晶胞,结构如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角)Ca2+的配位数为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】镍钴锰三元材料LiNixCoyMnzO2是一类新型锂离子电池正极材料,具有容量高、循环稳定性好等优点。
(1)锰元素基态原子的电子排布式为___________ ,镍钴锰三种基态原子中未成对电子数最多的是___________ 。
(2)镍可以形成多种配合物,如Ni(CO)4、[Ni(NH3)6]SO4等。
①上述两种配合物都存在的化学键的是___________
a. 离子键 b. 配位键 c. 极性键 d. 非极性键。
②Ni(CO)4常温下难溶于水,易溶于CCl4中,可推知其为___________ 。(填“极性分子”或“非极性分子”)
③[Ni(NH3)6]SO4中阴离子的空间构型为___________ 。
(3)MnO和CoO具有相同的晶体构型,其熔点大小顺序为___________
(4)锂离子电池目前广泛采用溶有LiPF6的碳酸酯作为电解液。
①LiPF6各元素的第一电离能从大到小的顺序为___________ 。
②常见溶剂碳酸乙烯酯(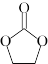 )中碳原子的杂化方式是
)中碳原子的杂化方式是___________ 。
(5)LiCoO2的晶胞是六棱柱,其结构如图所示,镍钴锰三元材料中Ni和Mn取代了部分Co的位置:
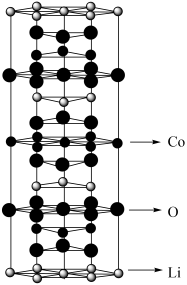
晶胞中含Li原子数为___________ ,若晶胞的底边边长为a nm,高为c nm,x:y:z=1:1:1,则LiNixCoyMnzO2晶胞的密度为___________ g/cm3(列出计算式)。
(1)锰元素基态原子的电子排布式为
(2)镍可以形成多种配合物,如Ni(CO)4、[Ni(NH3)6]SO4等。
①上述两种配合物都存在的化学键的是
a. 离子键 b. 配位键 c. 极性键 d. 非极性键。
②Ni(CO)4常温下难溶于水,易溶于CCl4中,可推知其为
③[Ni(NH3)6]SO4中阴离子的空间构型为
(3)MnO和CoO具有相同的晶体构型,其熔点大小顺序为
(4)锂离子电池目前广泛采用溶有LiPF6的碳酸酯作为电解液。
①LiPF6各元素的第一电离能从大到小的顺序为
②常见溶剂碳酸乙烯酯(
 )中碳原子的杂化方式是
)中碳原子的杂化方式是(5)LiCoO2的晶胞是六棱柱,其结构如图所示,镍钴锰三元材料中Ni和Mn取代了部分Co的位置:

晶胞中含Li原子数为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的有____________ 。
(1)每一周期元素都是从碱金属开始,以稀有气体结束
(2)f区都是副族元素,s区和p区的都是主族元素
(3)铝的第一电离能大于K的第一电离能
(4)B电负性和Si相近
(5)Ge的电负性为1.8,则其是典型的非金属
(6)半径:K+>Cl—
(7)酸性 HClO>H2SO4,碱性:NaOH > Mg(OH)2
(8)元素的最高正化合价=其最外层电子数=族序数
(1)每一周期元素都是从碱金属开始,以稀有气体结束
(2)f区都是副族元素,s区和p区的都是主族元素
(3)铝的第一电离能大于K的第一电离能
(4)B电负性和Si相近
(5)Ge的电负性为1.8,则其是典型的非金属
(6)半径:K+>Cl—
(7)酸性 HClO>H2SO4,碱性:NaOH > Mg(OH)2
(8)元素的最高正化合价=其最外层电子数=族序数
您最近半年使用:0次
【推荐3】有A、B、C、D、E、F六种元素,已知:
①它们位于三个不同短周期,核电荷数依次增大
②E元素的电离能数据见下表(kJ·mol-1):
③B与F分别同主族
④A、E分别都能与D按原子个数比1﹕1或2﹕l形成化合物
⑤B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学式_____________ 、______________
(2)B2A2分子中存在____ 个σ键,____ 个π键
(3)E2D2电子式____________
①它们位于三个不同短周期,核电荷数依次增大
②E元素的电离能数据见下表(kJ·mol-1):
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
④A、E分别都能与D按原子个数比1﹕1或2﹕l形成化合物
⑤B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学式
(2)B2A2分子中存在
(3)E2D2电子式
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、R、W五种前四周期元素,原子序数依次增大:X、Y、Z三种元素的基态原子位于同一周期,且其中基态Y原子的2p轨道处于半充满状态,Y和Z的单质可以通过分离液态空气的方法制得, 和
和 的电子数目相同;R为周期表前四周期中电负性最小的元素;W的原子序数为29.请回答下列问题。(如需表示具体元素请用相应的元素符号)
的电子数目相同;R为周期表前四周期中电负性最小的元素;W的原子序数为29.请回答下列问题。(如需表示具体元素请用相应的元素符号)
(1)写出 的电子式
的电子式_______ ;基态W原子的外围电子排布式为_______
(2)画出基态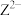 的价电子轨道表示式
的价电子轨道表示式_______
(3)X的一种氢化物的相对分子质量为26,其分子中 键与
键与 键的键数之比为
键的键数之比为_______
(4)Z的简单氢化物的沸点大于X的简单氢化物沸点的主要原因是_______
(5)化合物M由Z、R两种元素组成,其晶胞结构如图:
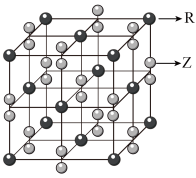
①则M的化学式为_______ 。
②下列有关该晶体的说法正确的是_______ (填字母编号)。
A.每个晶胞中含有14个 和13个
和13个
B.晶体中每个 周围距离
周围距离 最近的
最近的 有8个
有8个
C.晶体中与每个 距离最近的
距离最近的 有12个
有12个
D.该晶体属于离子晶体
 和
和 的电子数目相同;R为周期表前四周期中电负性最小的元素;W的原子序数为29.请回答下列问题。(如需表示具体元素请用相应的元素符号)
的电子数目相同;R为周期表前四周期中电负性最小的元素;W的原子序数为29.请回答下列问题。(如需表示具体元素请用相应的元素符号)(1)写出
 的电子式
的电子式(2)画出基态
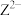 的价电子轨道表示式
的价电子轨道表示式(3)X的一种氢化物的相对分子质量为26,其分子中
 键与
键与 键的键数之比为
键的键数之比为(4)Z的简单氢化物的沸点大于X的简单氢化物沸点的主要原因是
(5)化合物M由Z、R两种元素组成,其晶胞结构如图:

①则M的化学式为
②下列有关该晶体的说法正确的是
A.每个晶胞中含有14个
 和13个
和13个
B.晶体中每个
 周围距离
周围距离 最近的
最近的 有8个
有8个C.晶体中与每个
 距离最近的
距离最近的 有12个
有12个D.该晶体属于离子晶体
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)钛原子核外有_______ 种空间运动状态不同的电子, 电子占据的最高能层的电子排布式为
电子占据的最高能层的电子排布式为_______ 。
(2)硫酸氧钛晶体中阳离子为如图1所示为链状聚合形式的离子,写出该晶体的化学式_______ 。

(3)钛酸钡是一种重要的压电材料,熔融状态的 和
和 均可导电,则等量的两物质同时开始加热,优先导电的是
均可导电,则等量的两物质同时开始加热,优先导电的是_______ (填化学式),阴离子 的立体构型是
的立体构型是_______ ,写出与 互为等电子体的两种由主族元素构成的分子
互为等电子体的两种由主族元素构成的分子_______ 。(填分子式)
(4)金红石为四方晶系晶体、晶胞参数为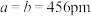 ,
, 。在金红石结构中,
。在金红石结构中, 原子处在变形的
原子处在变形的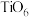 八面体中,
八面体中, 距离有4个较近,2个较远。
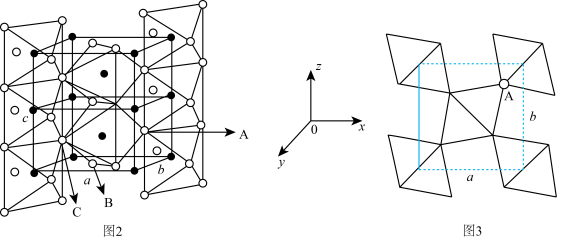
距离有4个较近,2个较远。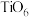 八面体沿着c轴共边连接成链,这些链再通过共顶点连接成晶体,结构如图2;晶体沿c轴方向的投影如图3。已知其中原子A、B的分数坐标分别为
八面体沿着c轴共边连接成链,这些链再通过共顶点连接成晶体,结构如图2;晶体沿c轴方向的投影如图3。已知其中原子A、B的分数坐标分别为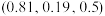 、
、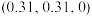 ,则原子C的分数坐标
,则原子C的分数坐标_______ 。用 代表阿伏加德罗常数的值,该晶体的密度可表示为
代表阿伏加德罗常数的值,该晶体的密度可表示为_______  (只要求列出计算式,不必化简)。
(只要求列出计算式,不必化简)。
(1)钛原子核外有
 电子占据的最高能层的电子排布式为
电子占据的最高能层的电子排布式为(2)硫酸氧钛晶体中阳离子为如图1所示为链状聚合形式的离子,写出该晶体的化学式

(3)钛酸钡是一种重要的压电材料,熔融状态的
 和
和 均可导电,则等量的两物质同时开始加热,优先导电的是
均可导电,则等量的两物质同时开始加热,优先导电的是 的立体构型是
的立体构型是 互为等电子体的两种由主族元素构成的分子
互为等电子体的两种由主族元素构成的分子(4)金红石为四方晶系晶体、晶胞参数为
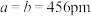 ,
, 。在金红石结构中,
。在金红石结构中, 原子处在变形的
原子处在变形的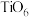 八面体中,
八面体中, 距离有4个较近,2个较远。
距离有4个较近,2个较远。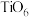 八面体沿着c轴共边连接成链,这些链再通过共顶点连接成晶体,结构如图2;晶体沿c轴方向的投影如图3。已知其中原子A、B的分数坐标分别为
八面体沿着c轴共边连接成链,这些链再通过共顶点连接成晶体,结构如图2;晶体沿c轴方向的投影如图3。已知其中原子A、B的分数坐标分别为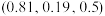 、
、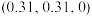 ,则原子C的分数坐标
,则原子C的分数坐标 代表阿伏加德罗常数的值,该晶体的密度可表示为
代表阿伏加德罗常数的值,该晶体的密度可表示为 (只要求列出计算式,不必化简)。
(只要求列出计算式,不必化简)。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】FeCl3溶液中的Fe3+可用KSCN溶液检验,还可与苯酚发生显色反应,用于酚羟基的检验。
(1)Fe3+基态核外电子排布式为______ 。
(2)与SCN-互为等电子体且为非极性分子的化学式为______ 。(填化学式)。
(3)苯酚中碳原子与氧原子的轨道杂化类型分别是______ ;1mol苯酚分子中含有的 键的数目为
键的数目为______ 。
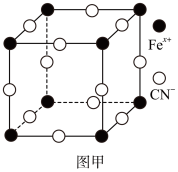
(4)普鲁士蓝俗称铁蓝,结构如图甲所示(K+未画出),平均每两个立方体中含有一个K+,又知该晶体中铁元素有+2价和+3价两种,则Fe3+与Fe2+的个数比为______ 。

(5)血红素铁(图乙)用作铁强化剂,其吸收率比一般铁剂高3倍,在图乙中画出Fe2+与N原子间的化学键(若是配位键,需要用箭头加以表示)。_______________
(1)Fe3+基态核外电子排布式为
(2)与SCN-互为等电子体且为非极性分子的化学式为
(3)苯酚中碳原子与氧原子的轨道杂化类型分别是
 键的数目为
键的数目为(4)普鲁士蓝俗称铁蓝,结构如图甲所示(K+未画出),平均每两个立方体中含有一个K+,又知该晶体中铁元素有+2价和+3价两种,则Fe3+与Fe2+的个数比为


(5)血红素铁(图乙)用作铁强化剂,其吸收率比一般铁剂高3倍,在图乙中画出Fe2+与N原子间的化学键(若是配位键,需要用箭头加以表示)。
您最近半年使用:0次



