金属镓有“电子工业脊梁”的美誉,镓与铝的化学性质类似.从刚玉渣(含钛、镓的低硅铁合金,还含有少量氧化铝)回收镓的一种流程如图所示:
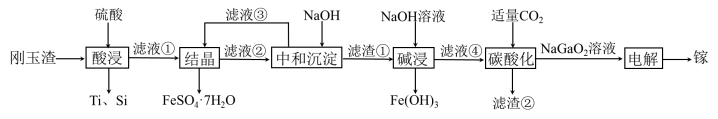
回答下列问题:
(1)镓原子结构示意图为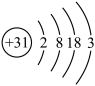 ,则其在元素周期表第
,则其在元素周期表第_________ 周期__________ 族。
(2)“酸浸”过程中禁止明火加热,原因是___________________________ ;为提高镓的浸出率,可采用的措施是__________________ (填一种即可)。
(3)“结晶”过程中得到 的操作主要为
的操作主要为__________________________ 。
(4)滤渣②的主要成分为_________________ 。
(5)“碳酸化”过程中不能通入过量 的原因为
的原因为______________________ (用离子方程式表示)。
(6)氮化镓具有优异的光电性能.工业上常采用在1100℃条件下,利用Ga与 反应可制备
反应可制备 ,该反应的化学方程式为
,该反应的化学方程式为_____________________________ 。
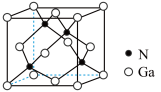
(7) 晶体的一种立方晶胞如图所示,已知晶胞参数为
晶体的一种立方晶胞如图所示,已知晶胞参数为 ,
, 的摩尔质量为
的摩尔质量为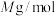 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。

回答下列问题:
(1)镓原子结构示意图为
 ,则其在元素周期表第
,则其在元素周期表第(2)“酸浸”过程中禁止明火加热,原因是
(3)“结晶”过程中得到
 的操作主要为
的操作主要为(4)滤渣②的主要成分为
(5)“碳酸化”过程中不能通入过量
 的原因为
的原因为(6)氮化镓具有优异的光电性能.工业上常采用在1100℃条件下,利用Ga与
 反应可制备
反应可制备 ,该反应的化学方程式为
,该反应的化学方程式为(7)
 晶体的一种立方晶胞如图所示,已知晶胞参数为
晶体的一种立方晶胞如图所示,已知晶胞参数为 ,
, 的摩尔质量为
的摩尔质量为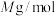 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
更新时间:2024-03-19 09:59:29
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】某化合物A由两种短周期元素组成,可以发生如下的转化。

已知:煤矿中的爆炸事故多与气体B有关。请回答:
(1)A的化学式是___________ ,气体 B在标准状况下的密度是___________  。(保留两位小数)
。(保留两位小数)
(2)写出反应②的离子方程式___________ ;
(3)A可用于金属的冶炼,请写出A与 的化学反应方程式
的化学反应方程式___________ 。

已知:煤矿中的爆炸事故多与气体B有关。请回答:
(1)A的化学式是
 。(保留两位小数)
。(保留两位小数)(2)写出反应②的离子方程式
(3)A可用于金属的冶炼,请写出A与
 的化学反应方程式
的化学反应方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】锂离子电池在我们日常生活中随处可见,随之而来的是废旧电池的合理处理,否则会造成新的环境污染。从废旧锂离子电池正极材料(主要含LiCoO2、Al等)中回收Co并制取CoC2O4·2H2O的工艺流程如图所示:
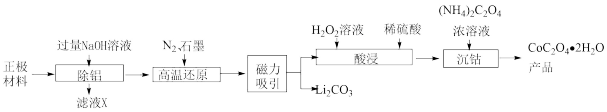
已知:①LiCoO2与NaOH溶液不反应;
②金属Co易被磁铁吸引,与稀硫酸反应生成大量氢气。
回答下列问题:
(1)“除铝”前需将废旧锂离子电池经过放电、破碎处理,其中破碎的目的是______ ,滤液X的主要溶质是______ (填化学式)。
(2)“高温还原”时,有CO生成,发生反应的化学方程式为______ ;“高温还原”时,通入N2的目的是______ 。
(3)从安全性角度考虑,“酸浸”时先加入过氧化氢溶液,再加入稀硫酸的原因是______ ,“酸浸”发生的总离子反应方程式为_______ 。
(4)“沉钴”时,检验钴离子已沉淀完全的方法是______ ,已知钴离子恰好完全沉淀(离子浓度等于10-5mol•L-1)时,c(C2O )=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=
)=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=______ 。

已知:①LiCoO2与NaOH溶液不反应;
②金属Co易被磁铁吸引,与稀硫酸反应生成大量氢气。
回答下列问题:
(1)“除铝”前需将废旧锂离子电池经过放电、破碎处理,其中破碎的目的是
(2)“高温还原”时,有CO生成,发生反应的化学方程式为
(3)从安全性角度考虑,“酸浸”时先加入过氧化氢溶液,再加入稀硫酸的原因是
(4)“沉钴”时,检验钴离子已沉淀完全的方法是
 )=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=
)=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】形状记忆陶瓷目前尚处于研究阶段,其中一种形状记忆陶瓷的主要原材料是纳米级ZrO2,用锆石(ZrSiO4,含少量FeO、Al2O3和制备纳米级ZrO2的流程设计如图1:
回答下列问题。
(1)锆石“粉碎过筛”的目的是___________ 。
(2)“酸浸”过程中发生的氧化还原反应的离子方程式为___________ 。滤渣1的主要成分是 ___________ 。若室温下Ksp[Cu(CN)2]=4×10﹣11,则为了使溶液中的c(Cu2+)≤1×10﹣5mol•L﹣1,则溶液中CN﹣的浓度不能低于 ___________ 。
(3)工业生产中常常用无水乙醇洗涤Zr(OH)4,除了可以使纳米级ZrO2纯度更高、颗粒更细外,还可以___________ 。
(4)酸浸时,得到的溶质主要是ZrOCl2,而不是预想中的ZrCl4,说明ZrCl4很容易水解,则ZrCl4水解产生ZrOCl2的化学方程式是___________ 。
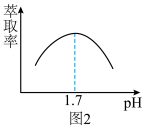
(5)除Fe3+也可以用合适的萃取剂,Fe3+的萃取率与pH的关系如图2所示,pH>1.7后,随pH增大3+萃取率下降的原因是___________ 。

回答下列问题。
(1)锆石“粉碎过筛”的目的是
(2)“酸浸”过程中发生的氧化还原反应的离子方程式为
(3)工业生产中常常用无水乙醇洗涤Zr(OH)4,除了可以使纳米级ZrO2纯度更高、颗粒更细外,还可以
(4)酸浸时,得到的溶质主要是ZrOCl2,而不是预想中的ZrCl4,说明ZrCl4很容易水解,则ZrCl4水解产生ZrOCl2的化学方程式是
(5)除Fe3+也可以用合适的萃取剂,Fe3+的萃取率与pH的关系如图2所示,pH>1.7后,随pH增大3+萃取率下降的原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】氮及其化合物在工业、农业、生活中有着重要的应用。如二元氮化物( 、CrN等)、三元锂过渡金属氮化物(
、CrN等)、三元锂过渡金属氮化物( 等)等在储氢领域、化学电源领域都有着重要的应用。
等)等在储氢领域、化学电源领域都有着重要的应用。
(1)Cr原子的核外电子排布式为_______ ;第一电离能:N_______ (填“>”或“<”)0。
(2) 可用于制备许多其他的含氮化合物{如
可用于制备许多其他的含氮化合物{如 、
、 、
、 、
、 等}以满足我们生产、生活的需要。
等}以满足我们生产、生活的需要。 中N的杂化类型为
中N的杂化类型为_______ , 中Fe的配位数为
中Fe的配位数为_______ 。
(3) 是很好的储氢材料,与
是很好的储氢材料,与 发生反应生成
发生反应生成 和LiH,写出该反应的化学方程式:
和LiH,写出该反应的化学方程式:_______ ,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(4) 晶体中,
晶体中, 为面心立方堆积,
为面心立方堆积, 填充了其中一半的四面体空隙,晶胞如图1所示,则一个
填充了其中一半的四面体空隙,晶胞如图1所示,则一个 晶胞中共含有
晶胞中共含有_______ 个共价键;设该晶胞的边长为acm,用NA表示阿伏加德罗常数的值,则该晶体的密度为_______ (用含a和NA的代数式表示) 。
。

(5) 、
、 和
和 形成立方晶体,其结构可以看作NaCl型结构,其中
形成立方晶体,其结构可以看作NaCl型结构,其中 和
和 分别占据体心和棱心,
分别占据体心和棱心, 占据面心,立方晶胞如图2所示,该晶体的化学式为
占据面心,立方晶胞如图2所示,该晶体的化学式为_______ 。

 、CrN等)、三元锂过渡金属氮化物(
、CrN等)、三元锂过渡金属氮化物( 等)等在储氢领域、化学电源领域都有着重要的应用。
等)等在储氢领域、化学电源领域都有着重要的应用。(1)Cr原子的核外电子排布式为
(2)
 可用于制备许多其他的含氮化合物{如
可用于制备许多其他的含氮化合物{如 、
、 、
、 、
、 等}以满足我们生产、生活的需要。
等}以满足我们生产、生活的需要。 中N的杂化类型为
中N的杂化类型为 中Fe的配位数为
中Fe的配位数为(3)
 是很好的储氢材料,与
是很好的储氢材料,与 发生反应生成
发生反应生成 和LiH,写出该反应的化学方程式:
和LiH,写出该反应的化学方程式:(4)
 晶体中,
晶体中, 为面心立方堆积,
为面心立方堆积, 填充了其中一半的四面体空隙,晶胞如图1所示,则一个
填充了其中一半的四面体空隙,晶胞如图1所示,则一个 晶胞中共含有
晶胞中共含有 。
。
(5)
 、
、 和
和 形成立方晶体,其结构可以看作NaCl型结构,其中
形成立方晶体,其结构可以看作NaCl型结构,其中 和
和 分别占据体心和棱心,
分别占据体心和棱心, 占据面心,立方晶胞如图2所示,该晶体的化学式为
占据面心,立方晶胞如图2所示,该晶体的化学式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】Ⅰ.现有以下物质:①饱和氯化铁溶液 ②氨气 ③冰醋酸 ④亚硫酸钠晶体 ⑤液态氯化氢 ⑥纯蔗糖 ⑦氯化钠晶体 ⑧硫酸氢钠溶液。
(1)能导电的是:_______ (填序号,下同);
(2)属于电解质的是:_______ ;
(3)硫酸氢钠在熔融状态的电离方程式_______ 。
(4)简述用①制备氢氧化铁胶体的操作_______ 。
Ⅱ.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据如图所示,回答下列问题:
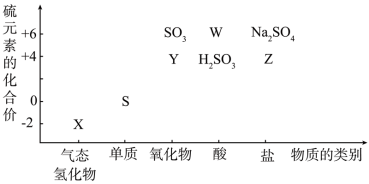
(5)Y的化学式为_______ ,检验Y常用的试剂是_______ 。
(6)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为_______ 。
(7)欲制备 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是_______ (填序号)。
a. b.
b. c.
c. d.
d.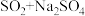
(8)将X与 混合,可生成淡黄色固体。该反应的还原剂与氧化剂的物质的量之比为
混合,可生成淡黄色固体。该反应的还原剂与氧化剂的物质的量之比为_______ 。
(1)能导电的是:
(2)属于电解质的是:
(3)硫酸氢钠在熔融状态的电离方程式
(4)简述用①制备氢氧化铁胶体的操作
Ⅱ.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据如图所示,回答下列问题:

(5)Y的化学式为
(6)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
(7)欲制备
 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是a.
 b.
b. c.
c. d.
d.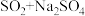
(8)将X与
 混合,可生成淡黄色固体。该反应的还原剂与氧化剂的物质的量之比为
混合,可生成淡黄色固体。该反应的还原剂与氧化剂的物质的量之比为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】过渡金属元素铬( )是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)请写出基态铬( )原子价电子的轨道表示式
)原子价电子的轨道表示式___________ 。
(2)超分子的定义是广义的,包括离子。一种羟甲基酚钠盐形成的含铁超分子的化学式为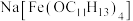 ,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:
,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:___________ 。
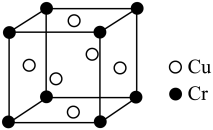
(3)某铜铬合金的立方晶胞结构如图所示。该铜铬合金的化学式为___________ ;离 原子最近的
原子最近的 原子数目为
原子数目为___________ ,离 原子最近的
原子最近的 原子数目为
原子数目为___________ 。若该晶胞参数为apm,则该晶体的密度为___________  。
。___________ 种。其同主族元素Si可形成硅酸盐,下图中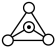 表示硅氧四面体,则该硅酸盐结构的通式为
表示硅氧四面体,则该硅酸盐结构的通式为___________ 。
 )是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:(1)请写出基态铬(
 )原子价电子的轨道表示式
)原子价电子的轨道表示式(2)超分子的定义是广义的,包括离子。一种羟甲基酚钠盐形成的含铁超分子的化学式为
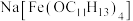 ,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:
,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:(3)某铜铬合金的立方晶胞结构如图所示。该铜铬合金的化学式为
 原子最近的
原子最近的 原子数目为
原子数目为 原子最近的
原子最近的 原子数目为
原子数目为 。
。
 表示硅氧四面体,则该硅酸盐结构的通式为
表示硅氧四面体,则该硅酸盐结构的通式为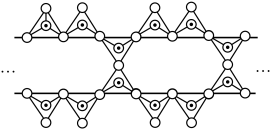
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】晶体X是一种在生产生活中得到广泛应用的化工产品。
(1)向 溶液中,滴加
溶液中,滴加 溶液,可观察到
溶液,可观察到___________ 。
(2)将(1)中所得混合物过滤。取滤液提纯、结晶可得到纯净的晶体X。通过___________ 实验,可确定X的晶体结构。
a.核磁共振 b.红外光谱 c.X射线衍射 d.质谱
(3)实验表明, 、
、 、
、 通过配位键构成了X晶体的骨架。其局部结构如图1,记为I型立方结构。
通过配位键构成了X晶体的骨架。其局部结构如图1,记为I型立方结构。

① 的电子式为
的电子式为___________ , 能与
能与 、
、 形成配位键的原因是
形成配位键的原因是___________ 。
②I型立方结构不是晶体X的晶胞,判断依据是___________ 将I型立方结构平移、旋转、并置,可得到晶体X的晶胞(如图2,下层左后的小立方体g未标出),图2中,I型立方结构分别是a、_______ 。
③结晶时,小立方体a内部会填入1个 (未画出)。小立方体b内部
(未画出)。小立方体b内部___________  。
。
a.不会填入 b.会填入1个 c.会填入2个 d.会填入4个
(4)已知晶体X晶胞的棱长为anm,以 表示阿伏加德罗常数的值,则晶体X密度的计算式为
表示阿伏加德罗常数的值,则晶体X密度的计算式为___________  。
。
(1)向
 溶液中,滴加
溶液中,滴加 溶液,可观察到
溶液,可观察到(2)将(1)中所得混合物过滤。取滤液提纯、结晶可得到纯净的晶体X。通过
a.核磁共振 b.红外光谱 c.X射线衍射 d.质谱
(3)实验表明,
 、
、 、
、 通过配位键构成了X晶体的骨架。其局部结构如图1,记为I型立方结构。
通过配位键构成了X晶体的骨架。其局部结构如图1,记为I型立方结构。
①
 的电子式为
的电子式为 能与
能与 、
、 形成配位键的原因是
形成配位键的原因是②I型立方结构不是晶体X的晶胞,判断依据是
③结晶时,小立方体a内部会填入1个
 (未画出)。小立方体b内部
(未画出)。小立方体b内部 。
。a.不会填入 b.会填入1个 c.会填入2个 d.会填入4个
(4)已知晶体X晶胞的棱长为anm,以
 表示阿伏加德罗常数的值,则晶体X密度的计算式为
表示阿伏加德罗常数的值,则晶体X密度的计算式为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值。
(1)在基态Ti原子中,核外存在_______ 对自旋相反的电子,核外电子占据最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(2) 可用作烯烃定向聚合的催化剂,例如丙烯用三乙基铝和三氯化钛做催化剂时,可以发生下列聚合反应:nCH3CH=CH2
可用作烯烃定向聚合的催化剂,例如丙烯用三乙基铝和三氯化钛做催化剂时,可以发生下列聚合反应:nCH3CH=CH2
 ,该反应中涉及的物质中碳原子的杂化轨道类型有
,该反应中涉及的物质中碳原子的杂化轨道类型有_______ ;反应中涉及物质的元素中电负性最大的是_______ 。三乙基铝是一种易燃物质,在氧气中三乙基铝完全燃烧所得产物中分子的立体构型是直线形的是_______ 。
(3)高分子纳米活性钛无霸是借助紫外线或太阳光的照射,在其表面产生氧化性极强的活性离子,这种活性离子可以分解生活中的一些有害物质(如苯、甲醛、丙酮等)。
①丙酮( )分子中含有π键与σ键数目之比为
)分子中含有π键与σ键数目之比为_______ 。
②甲醛易溶于水,原因是:a.甲醛和水都是极性分子,b._______ 。
(4) 配离子呈黄色。配体之一
配离子呈黄色。配体之一 分子中氧原子的价层电子对互斥模型是
分子中氧原子的价层电子对互斥模型是_______ 。
(5)有一种氮化钛晶体的晶胞如图所示,该晶体中Ti原子周围与Ti原子距离最近且相等的N原子的个数为_______ 。已知晶体的密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为_______ cm(用含 、
、 的式子表示)。
的式子表示)。

(1)在基态Ti原子中,核外存在
(2)
 可用作烯烃定向聚合的催化剂,例如丙烯用三乙基铝和三氯化钛做催化剂时,可以发生下列聚合反应:nCH3CH=CH2
可用作烯烃定向聚合的催化剂,例如丙烯用三乙基铝和三氯化钛做催化剂时,可以发生下列聚合反应:nCH3CH=CH2
 ,该反应中涉及的物质中碳原子的杂化轨道类型有
,该反应中涉及的物质中碳原子的杂化轨道类型有(3)高分子纳米活性钛无霸是借助紫外线或太阳光的照射,在其表面产生氧化性极强的活性离子,这种活性离子可以分解生活中的一些有害物质(如苯、甲醛、丙酮等)。
①丙酮(
 )分子中含有π键与σ键数目之比为
)分子中含有π键与σ键数目之比为②甲醛易溶于水,原因是:a.甲醛和水都是极性分子,b.
(4)
 配离子呈黄色。配体之一
配离子呈黄色。配体之一 分子中氧原子的价层电子对互斥模型是
分子中氧原子的价层电子对互斥模型是(5)有一种氮化钛晶体的晶胞如图所示,该晶体中Ti原子周围与Ti原子距离最近且相等的N原子的个数为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为 、
、 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】某油脂厂废弃的催化剂主要含有金属Pb、Al、Fe及其氧化物,采用如图工艺流程回收其中的铝并制备绿矾晶体( )。
)。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)废催化剂“酸浸”前,先用热的 溶液除去表面的油污,然后粉碎,用离子方程式表示
溶液除去表面的油污,然后粉碎,用离子方程式表示 溶液显碱性的原因:
溶液显碱性的原因:_______ 。粉碎的主要目的为_______ 。
(2)滤渣1的主要成分为_______ (填化学式),加入M发生反应的离子方程式为_______ 。
(3)“沉铝”时pH应该控制的范围为_______ ,若“沉铝”时用 溶液代替NaOH溶液,则滤渣2为碱式碳酸铝[
溶液代替NaOH溶液,则滤渣2为碱式碳酸铝[ ],同时有
],同时有 逸出,写出该反应的离子方程式:
逸出,写出该反应的离子方程式:_______ 。
(4)“控制pH”后从溶液中得到绿矾晶体,包含的操作是_______ 、过滤、洗涤及干燥。
(5)铝电池有广泛应用前景,一种可充放电的铝离子电池工作原理如图所示,电解质为 离子液体,CuS在电池反应后转化为
离子液体,CuS在电池反应后转化为 和
和 。
。

放电时,负极每消耗 ,有
,有_______ g Al溶解。该电池充电时,阳极反应式为_______ 。
 )。
)。
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |
| 开始沉淀时(c=0.01mol/L)的pH | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol/L)的pH | 4.7 | 3.2 | 9.0 |
(1)废催化剂“酸浸”前,先用热的
 溶液除去表面的油污,然后粉碎,用离子方程式表示
溶液除去表面的油污,然后粉碎,用离子方程式表示 溶液显碱性的原因:
溶液显碱性的原因:(2)滤渣1的主要成分为
(3)“沉铝”时pH应该控制的范围为
 溶液代替NaOH溶液,则滤渣2为碱式碳酸铝[
溶液代替NaOH溶液,则滤渣2为碱式碳酸铝[ ],同时有
],同时有 逸出,写出该反应的离子方程式:
逸出,写出该反应的离子方程式:(4)“控制pH”后从溶液中得到绿矾晶体,包含的操作是
(5)铝电池有广泛应用前景,一种可充放电的铝离子电池工作原理如图所示,电解质为
 离子液体,CuS在电池反应后转化为
离子液体,CuS在电池反应后转化为 和
和 。
。
放电时,负极每消耗
 ,有
,有
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】蛇纹石是一种天然富镁矿物,主要成分为 Mg3Si2O5(OH)4,还含有少量 Al2O3、Fe2O3、FeO 等杂质。现用蛇纹石来制取碱式碳酸镁[Mg2(OH)2CO3],其工艺流程如下:

回答下列问题:
(1)镁元素在元素周期表中的位置是_______ ;
(2)加入的 H2O2可将溶液中的 Fe2+氧化成 Fe3+,该步骤操作时应严格控制反应在较低温度下进行,其目的是_______ ;
(3)通入 NH3调节 pH,得到的滤渣主要充分是 Fe(OH)3和_______ ;
(4)沉镁时先加入氨水进行预氨化处理,但氨水的加入量不宜过多,原因是_______ ;
(5)写出加热 MgCO3·3H2O 生成碱式碳酸镁的化学方程式_______ 。

回答下列问题:
(1)镁元素在元素周期表中的位置是
(2)加入的 H2O2可将溶液中的 Fe2+氧化成 Fe3+,该步骤操作时应严格控制反应在较低温度下进行,其目的是
(3)通入 NH3调节 pH,得到的滤渣主要充分是 Fe(OH)3和
(4)沉镁时先加入氨水进行预氨化处理,但氨水的加入量不宜过多,原因是
(5)写出加热 MgCO3·3H2O 生成碱式碳酸镁的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】 是优良的催化剂和水处理剂,工业上利用难溶于水的固体阴离子交换树脂(可表示为
是优良的催化剂和水处理剂,工业上利用难溶于水的固体阴离子交换树脂(可表示为 ),采用离子交换法制备超细
),采用离子交换法制备超细 ,流程如下:
,流程如下:

已知:
Ⅰ.合成均匀的纳米 胶体
胶体
在图1装置中加入60mL 0.02
 (纯度99%以上)溶液,水浴加热下分批加入稍过量的阴离子交换树脂,搅拌,反应结束后,过滤,得
(纯度99%以上)溶液,水浴加热下分批加入稍过量的阴离子交换树脂,搅拌,反应结束后,过滤,得 胶体。
胶体。

实验中随着树脂的加入,测得刚开始pH值上升较快,pH值达到8.0附近后,上升开始变得极度缓慢,pH值达到9.0附近后,又开始有较明显小幅上升。
(1)图1中搅拌器的作用为:_______ 。
(2)下列说法正确的是_______。
Ⅱ. 碎粉焙烧
碎粉焙烧
(3)步骤⑤在图2高温悬浮煅烧炉中进行。写出该焙烧反应方程式:_______ ;

若煅烧炉下方通入预热空气的流速过小,带来的后果是:_______ 。
Ⅲ.实验并计算阴离子交换树脂用量
本次制备 实验中,交换树脂最佳加入量为反应所需用量的1.2倍。采用以下滴定法测定单位质量树脂所能交换的阴离子的量。已知:
实验中,交换树脂最佳加入量为反应所需用量的1.2倍。采用以下滴定法测定单位质量树脂所能交换的阴离子的量。已知: 为砖红色沉淀。实验过程中,溶液体积变化忽略不计。
为砖红色沉淀。实验过程中,溶液体积变化忽略不计。
(4)从下列选项中选择最佳操作并排序:_______ 。
称取阴离子交换树脂2.000g→a→→→→→重复滴定2-3次→计算
a.加入80.00ml 0.1 盐酸浸泡,盖上瓶塞并充分摇匀,静置、过滤
盐酸浸泡,盖上瓶塞并充分摇匀,静置、过滤
b.向浸泡液中加 调pH,同时稀释至100mL
调pH,同时稀释至100mL
c.向浸泡液中加稀硝酸调pH,同时稀释至100mL
d.用移液管移取25.00ml稀释后的浸泡液于锥形瓶中
e.用移液管移取25.00ml 0.1
 溶液于锥形瓶中
溶液于锥形瓶中
f.滴加2-3滴 溶液
溶液
g.用稀释后的浸泡液滴定
h.用0.1
 溶液滴定
溶液滴定
(5)滴定过程中调pH的目的是_______ ;滴定中平均消耗滴定管中溶液15.00mL。则本次制备 实验中交换树脂的最佳加入量为:
实验中交换树脂的最佳加入量为:_______ g
 是优良的催化剂和水处理剂,工业上利用难溶于水的固体阴离子交换树脂(可表示为
是优良的催化剂和水处理剂,工业上利用难溶于水的固体阴离子交换树脂(可表示为 ),采用离子交换法制备超细
),采用离子交换法制备超细 ,流程如下:
,流程如下:
已知:

Ⅰ.合成均匀的纳米
 胶体
胶体在图1装置中加入60mL 0.02

 (纯度99%以上)溶液,水浴加热下分批加入稍过量的阴离子交换树脂,搅拌,反应结束后,过滤,得
(纯度99%以上)溶液,水浴加热下分批加入稍过量的阴离子交换树脂,搅拌,反应结束后,过滤,得 胶体。
胶体。
实验中随着树脂的加入,测得刚开始pH值上升较快,pH值达到8.0附近后,上升开始变得极度缓慢,pH值达到9.0附近后,又开始有较明显小幅上升。
(1)图1中搅拌器的作用为:
(2)下列说法正确的是_______。
A.步骤②,所得滤渣的主要成分为 |
B.步骤①,总反应为: |
C.步骤①,当 时,交换反应基本完成 时,交换反应基本完成 |
| D.步骤①,水浴温度过高,离子交换速度过快,可能导致所得胶粒不均匀 |
Ⅱ.
 碎粉焙烧
碎粉焙烧(3)步骤⑤在图2高温悬浮煅烧炉中进行。写出该焙烧反应方程式:

若煅烧炉下方通入预热空气的流速过小,带来的后果是:
Ⅲ.实验并计算阴离子交换树脂用量
本次制备
 实验中,交换树脂最佳加入量为反应所需用量的1.2倍。采用以下滴定法测定单位质量树脂所能交换的阴离子的量。已知:
实验中,交换树脂最佳加入量为反应所需用量的1.2倍。采用以下滴定法测定单位质量树脂所能交换的阴离子的量。已知: 为砖红色沉淀。实验过程中,溶液体积变化忽略不计。
为砖红色沉淀。实验过程中,溶液体积变化忽略不计。(4)从下列选项中选择最佳操作并排序:
称取阴离子交换树脂2.000g→a→→→→→重复滴定2-3次→计算
a.加入80.00ml 0.1
 盐酸浸泡,盖上瓶塞并充分摇匀,静置、过滤
盐酸浸泡,盖上瓶塞并充分摇匀,静置、过滤b.向浸泡液中加
 调pH,同时稀释至100mL
调pH,同时稀释至100mLc.向浸泡液中加稀硝酸调pH,同时稀释至100mL
d.用移液管移取25.00ml稀释后的浸泡液于锥形瓶中
e.用移液管移取25.00ml 0.1

 溶液于锥形瓶中
溶液于锥形瓶中f.滴加2-3滴
 溶液
溶液g.用稀释后的浸泡液滴定
h.用0.1

 溶液滴定
溶液滴定(5)滴定过程中调pH的目的是
 实验中交换树脂的最佳加入量为:
实验中交换树脂的最佳加入量为:
您最近一年使用:0次

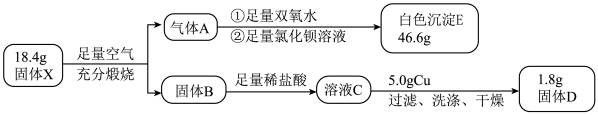
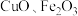 。
。 白色沉淀E的离子方程式是
白色沉淀E的离子方程式是

