根据下列实验操作和现象,得到的结论正确的是
实验操作和现象 | 实验结论 | |
A | 向 |
|
B | 向 |
|
C | 往 | 非金属性: |
D | 向 |
|
| A.A | B.B | C.C | D.D |
更新时间:2024-03-26 08:28:23
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列实验目的对应的方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入2~3mL蒸馏水 | 若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2 |
| B | Fe2+是否具有还原性 | 向2mL1.0mol·L−1FeSO4溶液中滴加几滴0.5mol·L−1酸性KMnO4溶液 | 若溶液不变紫红色,则Fe2+具有还原性;若溶液变紫红色,则Fe2+不具有还原性 |
| C | 比较Cl2、Br2、I2的氧化性 | 向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色,证明氧化性:Cl2>Br2>I2 |
| D | 比较H2CO3与CH3COOH的酸性 | 用pH计测定pH:①NaHCO3溶液②CH3COONa溶液 | pH①>②,证明H2CO3酸性弱于CH3COOH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用 代表阿伏加德罗常数的值。下列说法不正确的是
代表阿伏加德罗常数的值。下列说法不正确的是_______ 。
A.(2023·海南卷)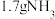 完全溶于
完全溶于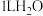 所得溶液,
所得溶液, 微粒数目为
微粒数目为
B.(2023·浙江卷)向1L0.1mol/LCH3COOH溶液通氨气至中性,铵根离子数为0.1NA
C.(2023·浙江卷)标准状况下,11.2LCl2通入水中,溶液中氯离子数为0.5NA
D.(2023·广东卷)体积为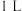 的
的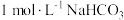 溶液中,
溶液中, 数目为
数目为
E.(2021·天津卷)1mol/LHCl溶液中,HCl分子的数目为NA
F.(2021·浙江卷) 的
的 水溶液中含有氧原子数为
水溶液中含有氧原子数为
 代表阿伏加德罗常数的值。下列说法不正确的是
代表阿伏加德罗常数的值。下列说法不正确的是A.(2023·海南卷)
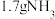 完全溶于
完全溶于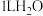 所得溶液,
所得溶液, 微粒数目为
微粒数目为
B.(2023·浙江卷)向1L0.1mol/LCH3COOH溶液通氨气至中性,铵根离子数为0.1NA
C.(2023·浙江卷)标准状况下,11.2LCl2通入水中,溶液中氯离子数为0.5NA
D.(2023·广东卷)体积为
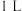 的
的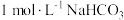 溶液中,
溶液中, 数目为
数目为
E.(2021·天津卷)1mol/LHCl溶液中,HCl分子的数目为NA
F.(2021·浙江卷)
 的
的 水溶液中含有氧原子数为
水溶液中含有氧原子数为
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】 代表阿伏加德罗常数的值,下列叙述不正确的是
代表阿伏加德罗常数的值,下列叙述不正确的是
 代表阿伏加德罗常数的值,下列叙述不正确的是
代表阿伏加德罗常数的值,下列叙述不正确的是A.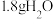 中含有的质子数为 中含有的质子数为 |
B.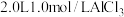 溶液中 溶液中 的数目小于 的数目小于 |
C. 时, 时, 为12的 为12的 溶液中含有 溶液中含有 数目为 数目为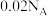 |
D. 和 和 于密闭容器中充分反应后,容器中分子总数为 于密闭容器中充分反应后,容器中分子总数为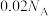 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,将11.65gBaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽略溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子浓度变化曲线如图所示,下列说法中正确的是
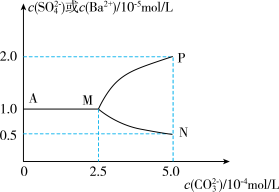

| A.相同温度时,Ksp(BaSO4)>Ksp(BaCO3) |
| B.BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大 |
| C.若使0.05molBaSO4全部转化为BaCO3,至少要加入1.30molNa2CO3 |
D.0.05molBaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小为:c(Ba2+)>c( )>c( )>c( ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度时, 悬浊液中存在:
悬浊液中存在: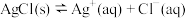 沉淀溶解平衡,其平衡曲线如图所示。下列说法错误的是
沉淀溶解平衡,其平衡曲线如图所示。下列说法错误的是
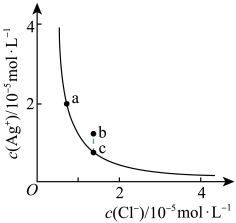
 悬浊液中存在:
悬浊液中存在: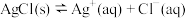 沉淀溶解平衡,其平衡曲线如图所示。下列说法错误的是
沉淀溶解平衡,其平衡曲线如图所示。下列说法错误的是
A.加入 ,可以使溶液由c点变到a点 ,可以使溶液由c点变到a点 |
B.加入少量水,平衡右移, 浓度不变 浓度不变 |
C.b点对应溶液中没有 沉淀生成 沉淀生成 |
D.c点对应的 等于a点对应的 等于a点对应的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时,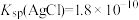 ,
,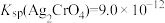 ,下列说法正确的是
,下列说法正确的是
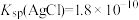 ,
,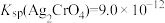 ,下列说法正确的是
,下列说法正确的是A.AgCl和 共存的悬浊液中, 共存的悬浊液中,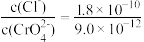 |
B.向 悬浊液中加入NaCl浓溶液, 悬浊液中加入NaCl浓溶液, 不可能转化为AgCl 不可能转化为AgCl |
C.向AgCl饱和溶液中加入NaCl固体,有AgCl析出且溶液中 |
D.向浓度均为0.1mol/L的 和NaCl混合溶液中滴加 和NaCl混合溶液中滴加 溶液,AgCl先析出 溶液,AgCl先析出 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某小组同学进行如下实验探究沉淀转化:
①向20mL0.1mol·L-1Na2CO3溶液中滴加20mL0.1mol·L-1BaCl2溶液,得浊液Ⅰ;
②向浊液Ⅰ中继续滴加20mL0.1mol·L-1Na2SO4溶液,充分振荡,得浊液Ⅱ;
③将浊液Ⅱ过滤,向滤渣中加入过量盐酸产生气体,过滤、洗涤、干燥,测得剩余固体a的质量大于0.233g。
下列说法不正确 的是
①向20mL0.1mol·L-1Na2CO3溶液中滴加20mL0.1mol·L-1BaCl2溶液,得浊液Ⅰ;
②向浊液Ⅰ中继续滴加20mL0.1mol·L-1Na2SO4溶液,充分振荡,得浊液Ⅱ;
③将浊液Ⅱ过滤,向滤渣中加入过量盐酸产生气体,过滤、洗涤、干燥,测得剩余固体a的质量大于0.233g。
下列说法
A.Na2CO3溶液显碱性的原因: |
| B.固体a的成分为BaSO4 |
| C.c(Ba2+)大小关系:浊液Ⅰ<浊液Ⅱ |
D.由该实验可以推断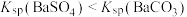 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】根据下列实验操作和现象,得出的结论及推理均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 光照时甲烷与氯气反应后的混合气体能使紫色石蕊溶液变红 | 生成的氯甲烷具有酸性 |
| B | 向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀 | X一定具有氧化性 |
| C | 两支盛0.1 mol·L−1 醋酸和次氯酸的试管中分别滴加等浓度NaHCO3溶液,观察到前者有气泡、后者无气泡 | Ka(CH3COOH)>Ka1(H2CO3)>Ka(HClO) |
| D | 向10 mL0.1 mol·L−1 AgNO3 溶液中先加入0.1 mol·L−1 KCl 溶液5 mL,再加入0.1 mol·L−1 的KI溶液5 mL,先出现白色沉淀,后出现黄色沉淀。 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W、Q为短周期主族元素,原子序数依次增大且原子序数总和等于49。它们的化合物在常温下有如下转化关系:已知:乙、戊分子都含有10个电子。甲为三元化合物,其他化合物均为二元化合物。下列说法正确的是
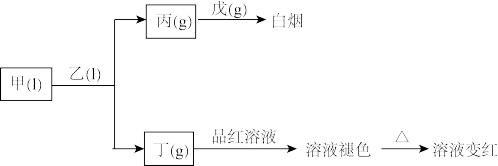

| A.原子半径从大到小顺序:W>Z>Y |
| B.简单氢化物的稳定性:Q>W>Z>Y |
| C.最高价氧化物对应水化物的酸性:Q>W |
| D.化合物W2Q2中含极性键、非极性键和离子键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】短周期主族元素X、Y、Z、U、V、W在元素周期表中的相对位置如图所示。已知:常温常压下,W的单质为黄绿色气体。下列说法错误的是
| Y | Z | U | ||
| X | V | W |
A.简单离子半径: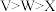 |
B.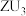 分子中所有原子均达到了8电子稳定结构 分子中所有原子均达到了8电子稳定结构 |
C.最高价氧化物对应水化物的酸性: |
| D.Z的最简单氢化物的水溶液呈酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】据氧族元素的性质推断,硒不可能具有的性质是( )
| A.单质易溶于水 | B.最高价氧化物对应水化物是酸 |
| C.单质既有氧化性又有还原性 | D.气态氢化物的稳定性较H2S弱 |
您最近一年使用:0次

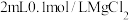 溶液中滴加3滴
溶液中滴加3滴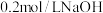 溶液,再滴加4滴
溶液,再滴加4滴 溶液,白色沉淀转化为红褐色
溶液,白色沉淀转化为红褐色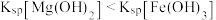
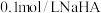 溶液中滴加酚酞溶液,溶液变为浅红色
溶液中滴加酚酞溶液,溶液变为浅红色 (
( 和
和 为
为 的电离平衡常数)
的电离平衡常数)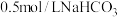 溶液中加入盐酸,将产生的气体通入
溶液中加入盐酸,将产生的气体通入 溶液中,
溶液中,
 和
和 的饱和溶液中,金属阳离子的物质的量浓度的负对数
的饱和溶液中,金属阳离子的物质的量浓度的负对数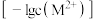 ,已知该温度下,
,已知该温度下, ,下列说法正确的是
,下列说法正确的是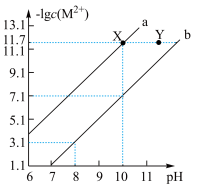
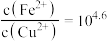
 线表示
线表示 点对应的饱和溶液中加入少量
点对应的饱和溶液中加入少量 点对应的溶液
点对应的溶液 溶液中含有的少量
溶液中含有的少量 ,可加入适量
,可加入适量


