利用含钴废料(主要成分为 ,还含有少量的铝箔、
,还含有少量的铝箔、 等杂质)制备碳酸钴的工艺流程如图:
等杂质)制备碳酸钴的工艺流程如图:
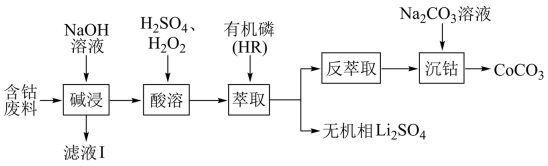
已知:萃取 的反应原理:
的反应原理: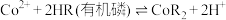 。下列说法错误的是
。下列说法错误的是
A.“滤液Ⅰ”中溶质的主要成分是 |
B.“酸溶”反应中 做氧化剂 做氧化剂 |
C.“反萃取”中可加入 分离出 分离出 |
D.“沉钴”时 溶液滴加速率不宜过快,目的是防止生成 溶液滴加速率不宜过快,目的是防止生成 |
更新时间:2024-03-24 17:19:39
|
相似题推荐
【推荐1】 是一种铁盐,由于兼具消毒和净水功能具有很大的利用价值,与盐酸可发生反应
是一种铁盐,由于兼具消毒和净水功能具有很大的利用价值,与盐酸可发生反应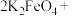
 ,下列说法错误的是
,下列说法错误的是
 是一种铁盐,由于兼具消毒和净水功能具有很大的利用价值,与盐酸可发生反应
是一种铁盐,由于兼具消毒和净水功能具有很大的利用价值,与盐酸可发生反应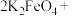
 ,下列说法错误的是
,下列说法错误的是| A.产物Q为一种黄绿色有毒气体 |
B. 中铁的化合价为+6 中铁的化合价为+6 |
| C.反应中氧化剂与还原剂的物质的量之比为1∶8 |
D.8 mol HCl参与反应,电子转移总数为: |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列变化过程中,加入还原剂才能实现的是
| A.Clˉ→Cl2 | B.FeO→Fe | C.SO2→SO32- | D.Fe2+→Fe3+ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
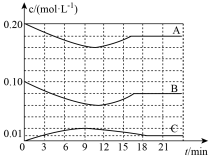
【推荐1】将0.20molA和0.10molB充入1L恒容密闭容器中发生反应: 。反应过程中部分物质的浓度变化如图所示。则第12min时改变的条件是
。反应过程中部分物质的浓度变化如图所示。则第12min时改变的条件是
 。反应过程中部分物质的浓度变化如图所示。则第12min时改变的条件是
。反应过程中部分物质的浓度变化如图所示。则第12min时改变的条件是
| A.增大A的浓度 | B.增大压强 | C.升高温度 | D.加入催化剂 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氯化硫酰(SO2Cl2)常用作氧化剂,它是一种无色液体,熔点:-54.1℃,沸点:69.1℃,可用干燥的SO2和Cl2在活性炭作催化剂的条件下制取:SO2(g)+Cl2(g)⇌SO2Cl2(l) ΔH=-97.3kJ·mol-1。下列有关SO2Cl2制取的说法正确的是
| A.该反应在高温下能自发进行 |
| B.使用活性炭作催化剂能缩短该反应达平衡的时间 |
| C.化学平衡发生移动,该反应平衡常数必发生变化 |
| D.使SO2Cl2液化从平衡体系中分离,能加快正反应速率,增大Cl2转化率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】溴化苄是重要的有机合成工业原料,可以苯甲醇为原料合成,实验原理及装置如图所示。反应结束后,反应液可按下列步骤分离和纯化:静置→分液→水洗→纯碱洗→水洗→干燥→减压蒸馏。下列有关说法错误的是
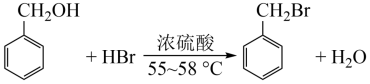



| A.实验时,应先从冷凝管接口b处通水,后加热至反应温度 |
| B.该实验适宜用水浴加热 |
| C.浓硫酸作催化剂和脱水剂 |
| D.纯碱洗的目的是除去氢溴酸等酸性物质 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】为了除去粗盐中的Ca2+、Mg2+、SO42- 及泥沙,可将粗盐溶于水,然后进行下列五项操作,其中正确的操作顺序是( )
①加适量盐酸 ②过滤 ③加过量Na2CO3溶液
④加过量NaOH溶液 ⑤加过量BaCl2溶液
①加适量盐酸 ②过滤 ③加过量Na2CO3溶液
④加过量NaOH溶液 ⑤加过量BaCl2溶液
| A.⑤④③②① | B.⑤④③①② | C.②⑤④③① | D.③⑤④②① |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】氮化钡( Ba3N2)是一种重要的化学试剂。高温下,向氢化钡(BaH2)中通入氮气反应生成氮化钡,在实验室可用如图装置制备(每个装置只用一次)。已知: Ba3N2遇水反应; BaH2在潮湿空气中能自燃,遇水反应。下列说法不正确的是
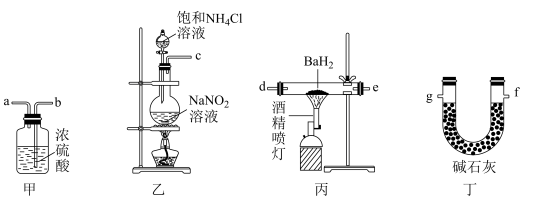

| A.实验时,先点燃装置丙中的酒精喷灯,后点燃装置乙中的酒精灯 |
| B.该实验装置中缺少尾气处理装置 |
| C.按气流方向,装置的连接顺序可为c→b→a→d→e→g |
| D.装置甲中的浓硫酸和装置丁中的碱石灰均可防止水蒸气进入装置丙中 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】铵明矾[ NH4Al(SO4)2·12H2O为无色、透明晶体,工业常用于制造颜料,媒染剂、净水剂等,其制备过程如图所示,下列观点不正确的是
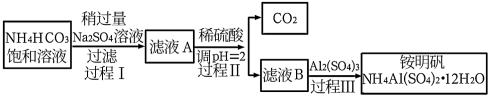

| A.向铵明矾溶液中逐滴加入NaOH 溶液至过量,先后发生若干简单离子反应,其中第二个离子反应为:Al3+ +3OH-= Al(OH)3↓ |
| B.过程Ⅰ所得滤渣可用于制备工业用纯碱 |
C.过程Ⅱ中调节pH 使滤液B显酸性的目的是为了除去 提高铵明矾的产率 提高铵明矾的产率 |
| D.过程Ⅲ中向滤液B添加一定比例的Al2(SO4)3,经蒸发浓缩、冷却结晶、过滤、洗涤干燥可得铵明矾 |
您最近半年使用:0次

 。针对上述反应,在其它条件不变时,下列说法正确的是
。针对上述反应,在其它条件不变时,下列说法正确的是 是一种重要的化工原料,可以用来制备一系列物质(如下图所示)。下列说法错误的是
是一种重要的化工原料,可以用来制备一系列物质(如下图所示)。下列说法错误的是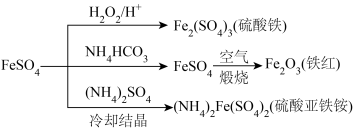
 胶体可用作净水剂
胶体可用作净水剂 分解,制备
分解,制备 需在较低温度下进行
需在较低温度下进行 是否被氧化
是否被氧化

