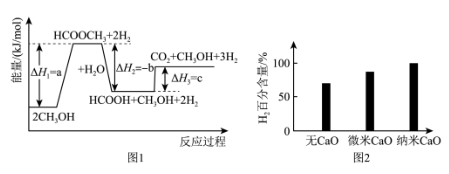
采用热分解法脱除沼气中的 过程中涉及的主要反应为
过程中涉及的主要反应为
反应Ⅰ:
 kJ⋅mol
kJ⋅mol
反应Ⅱ: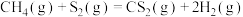
 kJmol
kJmol
保持100kPa不变,将 与
与 按2∶1体积比投料,并用
按2∶1体积比投料,并用 稀释,在不同温度下反应达到平衡时,所得
稀释,在不同温度下反应达到平衡时,所得 、
、 与
与 的体积分数如题13图所示。下列说法正确的是
的体积分数如题13图所示。下列说法正确的是
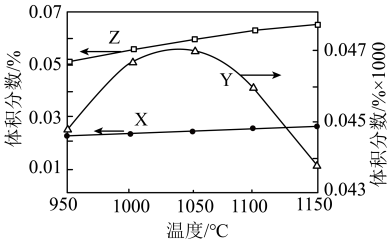
题13图
A.反应 的 的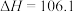 kJ⋅mol kJ⋅mol |
B.曲线Y代表的是 的平衡体积分数 的平衡体积分数 |
C.高于1050℃时, 平衡转化率与 平衡转化率与 平衡转化率的差值随温度升高减小 平衡转化率的差值随温度升高减小 |
| D.1050℃下反应,增大体系的压强,平衡后H₂的体积分数可能达到0.07 |
更新时间:2024-03-26 22:05:44
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知:①Zn(s)+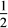 O2(g)=ZnO(s)ΔH=-348.3kJ·mol-1
O2(g)=ZnO(s)ΔH=-348.3kJ·mol-1
②2Ag(s)+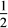 O2(g)=Ag2O(s)ΔH=-31.0kJ·mol-1
O2(g)=Ag2O(s)ΔH=-31.0kJ·mol-1
则Zn与Ag2O反应生成ZnO和Ag的热化学方程式为
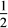 O2(g)=ZnO(s)ΔH=-348.3kJ·mol-1
O2(g)=ZnO(s)ΔH=-348.3kJ·mol-1②2Ag(s)+
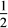 O2(g)=Ag2O(s)ΔH=-31.0kJ·mol-1
O2(g)=Ag2O(s)ΔH=-31.0kJ·mol-1则Zn与Ag2O反应生成ZnO和Ag的热化学方程式为
| A.2Zn(s)+2Ag2O(s)===2ZnO(s)+4Ag(s)ΔH=-634.6 kJ·mol-1 |
| B.Zn+Ag2O===ZnO+2Ag ΔH=+317.3kJ·mol-1 |
| C.Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)ΔH=-317.3kJ |
| D.Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)ΔH=+317.3kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知化学反应的热效应只与反应物的初始状态和生成物的最终状态有关,如图Ⅰ所示:ΔHa=ΔHb+ΔHc。根据上述原理和图Ⅱ所示,判断下列各项对应的反应热关系中不正确 的是


| A.A→F的ΔH=-ΔH6 |
| B.A→D的ΔH=ΔH1+ΔH2+ΔH3 |
| C.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=0 |
| D.ΔH1+ΔH6=ΔH2+ΔH3+ΔH4+ΔH5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】反应2SO2+O2 2SO3达到平衡后,再向反应器中充入由18O组成的氧气,经一段时间后,18O可能存在于。
2SO3达到平衡后,再向反应器中充入由18O组成的氧气,经一段时间后,18O可能存在于。
 2SO3达到平衡后,再向反应器中充入由18O组成的氧气,经一段时间后,18O可能存在于。
2SO3达到平衡后,再向反应器中充入由18O组成的氧气,经一段时间后,18O可能存在于。| A.生成的SO3中 | B.O2和SO3中 |
| C.剩余的SO3中 | D.O2、SO2和SO3中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】探究铜单质及其化合物的性质,下列实验操作和现象能得出相应结论的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将2mL0.5mol•L-1的CuCl2溶液加热后置于冷水中,溶液黄色变为蓝色 | 说明降温,[Cu(H2O)4]2++4Cl- [CuCl4]2-+4H2O向正反应方向移动 [CuCl4]2-+4H2O向正反应方向移动 |
| B | 向2mL2%CuSO4溶液中加入几滴1%NaOH溶液,振荡后加入几滴有机物X溶液,加热未出现砖红色沉淀 | X不可能是含有醛基官能团的有机化合物 |
| C | 常温下,铜与浓硝酸反应后溶液呈绿色,加热后,溶液绿色消失 | 加热条件下,铜与绿色物质发生化学反应 |
| D | 在5mL0.1mol•L-1CuSO4溶液中,逐滴加入30mL0.10mol•L-1氨水溶液,再滴加少量Na2S溶液,先产生蓝色沉淀,后出现深蓝色,最后为黑色沉淀 | Cu(OH)2转化为[Cu(NH3)4]2+,说明[Cu(NH3)4]2+比Cu(OH)2更难电离;最后转化为CuS,能说明Ksp(CuS)小于Ksp[Cu(OH)2] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法中不正确的有( )个
①反应速率用于衡量化学反应进行的快慢
②可逆反应达到化学平衡状态时,正、逆反应速率都为0
③决定反应速率的主要因素是反应物的性质
④适当增大反应物浓度,提高反应温度都能增大反应速率
⑤不管什么反应使用催化剂,都可以加快反应速率 ,并可以使平衡移动。
⑥可逆反应A(g) B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大
①反应速率用于衡量化学反应进行的快慢
②可逆反应达到化学平衡状态时,正、逆反应速率都为0
③决定反应速率的主要因素是反应物的性质
④适当增大反应物浓度,提高反应温度都能增大反应速率
⑤不管什么反应使用催化剂,都可以加快反应速率 ,并可以使平衡移动。
⑥可逆反应A(g)
 B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大
| A.2 个 | B.3 个 | C.4 个 | D.5个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】汽车尾气中的 和
和 在一定温度和催化剂条件下可发生反应
在一定温度和催化剂条件下可发生反应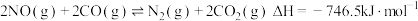 。将
。将 和
和 以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中的NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图所示,下列说法错误的是
以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中的NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图所示,下列说法错误的是

 和
和 在一定温度和催化剂条件下可发生反应
在一定温度和催化剂条件下可发生反应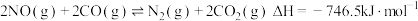 。将
。将 和
和 以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中的NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图所示,下列说法错误的是
以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中的NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图所示,下列说法错误的是
A.温度低于 ,图中曲线脱氮率随温度升高而变化不大的主要原因是催化剂活性偏低 ,图中曲线脱氮率随温度升高而变化不大的主要原因是催化剂活性偏低 |
B.图中 点是反应的平衡点 点是反应的平衡点 |
C.催化剂 的最适温度为 的最适温度为 |
| D.温度高于450摄氏度,脱氮率下降的原因可能是反应已达到平衡,升高温度平衡逆移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定条件下,某可逆反应的正反应速率和逆反应速率随时间变化的曲线如图所示。下列有关说法正确的是
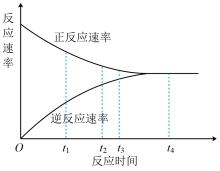
| A.t1时刻,反应逆向进行 |
| B.t2时刻,正反应速率小于逆反应速率 |
| C.t3时刻,达到反应进行的限度 |
| D.t4时刻,反应处于平衡状态 |
您最近一年使用:0次