联合制碱法利用食盐水、氨气和二氧化碳制纯碱,涉及的反应之一为 。设
。设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 。设
。设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.常温常压下, 含氧原子的数目为 含氧原子的数目为 |
B.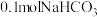 中含离子数目为 中含离子数目为 |
C. 溶液中含 溶液中含 数目为 数目为 |
D.标准状况下,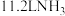 通入水中,溶液中 通入水中,溶液中 数目为 数目为 |
更新时间:2024-04-18 22:47:36
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.常温下,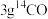 与 与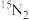 混合物,含电子的数目为 混合物,含电子的数目为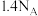 |
B.标准状况下, 的 的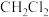 中 中 原子数目为 原子数目为 |
C.室温下,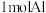 与足量浓硝酸充分反应,转移电子数目为 与足量浓硝酸充分反应,转移电子数目为 |
D.密闭容器中, 与 与 充分反应后,分子的数目为 充分反应后,分子的数目为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值,下列说法错误的是
| A.1L0.1mol•L-1Fe2(SO4)3溶液中含有的阳离子数目大于0.2NA |
| B.0.24gMg在O2和CO2的混合气体中完全燃烧,转移电子数为0.02NA |
| C.12.0g NaHSO4晶体中阴阳离子数目为0.3NA |
| D.3g由CO2和SO2组成的混合气体中含有的质子数为1.5NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】人们从冰箱中取出的“常态冰”仅是冰存在的多种可能的形式之一。目前,科学家发现了一种全新的多孔、轻量级的“气态冰”,可形成气凝胶。下列有关说法正确的是
| A.“常态冰”和“气态冰”结构不同,是同素异形体 |
| B.“气态冰”因其特殊的结构而具有比“常态冰”更活泼的化学性质 |
| C.18g“气态冰”的体积为22.4L |
| D.构成“气态冰”的分子中含有极性共价键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1mol NH4F晶体中含有的共价键数目为3NA |
| B.2.24L C2H2完全燃烧,则消耗O2分子数目一定为0.25NA |
| C.向100mL 0.10mol/L FeCl3溶液中加入足量Cu粉充分反应,转移电子数目为0.01NA |
| D.0.1mol SO2与足量O2在V2O5作用下受热充分反应,生成的SO3分子数目为0.1NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】设NA为阿伏加德罗常数的值,下列叙述错误的是


| A.含16 g氧原子的二氧化硅晶体中含有的σ键数目为2NA |
| B.58.5 g NaCl晶体中含有0.25NA个如上图所示的结构单元 |
| C.18 g冰中含有氢键数为2NA |
| D.标准状况下,2.24 LHF中含有的共价键的数目为0.1NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NA代表阿伏加德罗常数的值。下列说法正确的是
| A.1L1mol/L的葡萄糖溶液中,溶质所含羟基的个数为5NA |
| B.33.6L丙烯(标准状况)与足量HCl发生加成反应,生成1-氯丙烷个数为1.5NA |
| C.在反应KClO4+8HCl=KCl+4Cl2↑+4H2O中,每生成4molCl2转移的电子数为8NA |
| D.H2S的燃烧热是QkJ/mol。充分燃烧H2S,当有0.5QkJ热量放出时,转移的电子数为6NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某溶液中可能含有 、
、 、
、 、
、 、
、 、
、 中的几种,且各种离子浓度相等。加入铝片,产生H2。下列说法正确的是( )
中的几种,且各种离子浓度相等。加入铝片,产生H2。下列说法正确的是( )
 、
、 、
、 、
、 、
、 、
、 中的几种,且各种离子浓度相等。加入铝片,产生H2。下列说法正确的是( )
中的几种,且各种离子浓度相等。加入铝片,产生H2。下列说法正确的是( )A.向原溶液中加入Cu片发生:3Cu+8 +2 +2 =3 =3 +4H2O+2NO↑ +4H2O+2NO↑ |
B.向原溶液中加入过量氨水发生: + + +4NH3∙H2O=Fe(OH)3↓+4 +4NH3∙H2O=Fe(OH)3↓+4 |
C.向原溶液中加入过量Ba(OH)2溶液发生:Ba2++2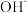 + + + + + + =NH3∙H2O +BaSO4↓+H2O =NH3∙H2O +BaSO4↓+H2O |
D.向原溶液中加入BaCl2溶液发生:2 + + + + =BaCO3↓+BaSO4↓ =BaCO3↓+BaSO4↓ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,已知: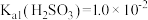 、
、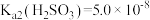 ,通过下列实验研究
,通过下列实验研究 溶液的性质。
溶液的性质。
实验1:向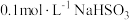 溶液中滴加一定量的
溶液中滴加一定量的 溶液,测得混合溶液
溶液,测得混合溶液 为7。
为7。
实验2:向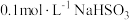 溶液中通入一定量的
溶液中通入一定量的 ,测得溶液
,测得溶液 为7。
为7。
实验3:向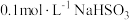 溶液中逐滴加入等体积
溶液中逐滴加入等体积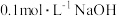 溶液,测得溶液
溶液,测得溶液 约为10。
约为10。
实验4:向 溶液中滴加少量
溶液中滴加少量 溶液,产生白色沉淀。
溶液,产生白色沉淀。
下列说法正确的是
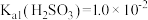 、
、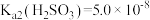 ,通过下列实验研究
,通过下列实验研究 溶液的性质。
溶液的性质。实验1:向
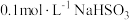 溶液中滴加一定量的
溶液中滴加一定量的 溶液,测得混合溶液
溶液,测得混合溶液 为7。
为7。实验2:向
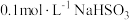 溶液中通入一定量的
溶液中通入一定量的 ,测得溶液
,测得溶液 为7。
为7。实验3:向
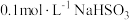 溶液中逐滴加入等体积
溶液中逐滴加入等体积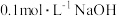 溶液,测得溶液
溶液,测得溶液 约为10。
约为10。实验4:向
 溶液中滴加少量
溶液中滴加少量 溶液,产生白色沉淀。
溶液,产生白色沉淀。下列说法正确的是
A.实验1混合溶液中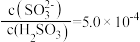 |
B.实验2所得溶液中存在 |
| C.实验3操作过程中水的电离程度逐渐减小 |
D.实验4中反应的离子方程式为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】25℃时,向10mL0.10mol/L的一元弱酸HA(Ka=1.0×10-3)中逐滴加入0.10mol/LNaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如图所示。下列说法不正确的是
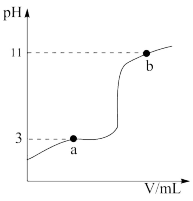

| A.V=10mL时,c(OH-)=c(HA)+c(H+) |
| B.b点时,c(Na+)>c(A-)>c(OH-)>c(H+) |
| C.溶液在a点和b点时水的电离程度相同 |
| D.a点时,c(HA)+c(OH-)=c(Na+)+c(H+) |
您最近半年使用:0次

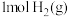 和
和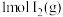 反应后气体分子总数等于
反应后气体分子总数等于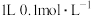 的
的 溶液中,
溶液中, 的数目为
的数目为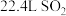 含有的原子总数为
含有的原子总数为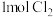 与铁完全反应生成
与铁完全反应生成 时转移的电子数为
时转移的电子数为
 的总数为
的总数为 NA
NA

